SISTEMAS BICROMOFÓRICOS EM TRANSFERÊNCIA DE ENERGIA EM FASE HOMOGÊNEA E MICROHETEROGÊNEA
Idalina M. M de Carvalho (PG)*, Ícaro de S. Moreira (PQ)** e Marcelo H. Gehlen (PQ)*
*Instituto
de Química de São Carlos - Universidade de São
Paulo
** Depto.
Química Orgânica e Inorgânica - Universidade
Federal do Ceará
palavras-chave: transferência de energia, luminescentes, MLCT
Complexos bicromofóricos consistindo de Ru(bpy)32+ e um segundo cromóforo-supressor covalentemente ligado a um dos ligantes bipiridina tem sido largamente utilizado para elucidar os mecanismos dos processos de tranferência de energia e de elétron em complexos de metais de transição1.
Considerando que os processos de transferência eletrônica dependem de vários fatores nos quais se incluem a distância molecular entre centro receptor e doador, grau de acoplamento eletrônico e efeito de solvente, sistemas modelos contendo receptor-doador espaçados por grupos moleculares rígidos ou flexíveis possibilitam uma investigação mais detalhada dos fatores que controlam a eficiência do processo.
Um dos objetivos da nossa pesquisa é o estudo de sistemas misto inorgânico-orgânico no qual um dos ligantes do metal é funcionalizado com um cromóforo orgânico do tipo corante, vindo então a acrescentar novas propriedades espectroscópicas e possibilidades de estudo de processos de transferência de energia ou elétron intramolecular, dependendo das características do sistema.
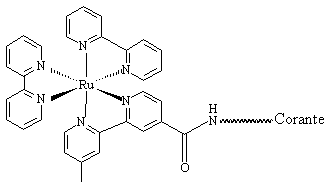
Os compostos modelos utilizados em nosso estudo consistem do [Ru(bpy)3]2+ (ET = 49,0 kcal/mol) no qual um dos ligantes bpy é derivatizado com grupo ácido COOH (Figura 1). Como cromóforo orgânico usou-se 9-aminoantraceno (ET ~42,7 kcal/mol), 9-aminoacridina (ET = 46,3 kcal/mol), 2-aminonaftaleno (ET = 54,3 kcal/mol) e 1-aminopireno (ET ~ 48,2 kcal/mol). Os espaçadores utilizados foram a ligação amida e o aminoácido prolina. O objetivo específico deste trabalho é a investigação de processos de transferência de energia pelo mecanismo de troca eletrônica.
Os compostos foram sintetizados via ativação do grupo ácido pela carbodiimida e posterior ligação com o composto orgânico2.
Os sistemas fotofísicos foram estudados em fase homogênea e microheterogênea, através das técnicas de fluorescência fotoestacionária e resolvida no tempo, utilizando-se o espectrofotômetro CD-900 Edinburg.

Figura 1. Estutura esquematizada dos compostos sintetizados.
O espectro de absorção eletrônica UV-visível de todos os complexos estudados apresentam o perfil espectral típico da unidade Ru-bpy, indicando que os ligantes orgânicos não pertubam significativamente a unidade cromofórica central; contudo, os espectros de excitação mostram evidências da presença do composto orgânico (corante aromático).
Todos os compostos são luminescentes apresentando uma emissão de natureza MLCT característica dos compostos contendo Ru-bpy, porém com os máximos de emissão deslocados. Esses deslocamentos são dependentes do tipo de substituinte ligado ao complexo via um grupo amida ou grupo prolina. Em uma primeira análise podemos atribuir este efeito a delocalização e interação do cromóforo ligado com o estado MLCT formado e, possivelmente, modificando o envelope vibracional da transição de luminescência.
Os tempos de vida aumentam com a distância entre o doador e o receptor. Isto indica a diminuição da interação entre os orbitais moleculares do doador e receptor, com redução da taxa de transferência de energia intramolecular.
Para o complexo de rutênio coordenado ao corante 9-aminopireno em sistema micelar de SDS na presença de dimetilanilina, observa-se a formação de exciplexo com pireno com tempo de vida de aproximadamente 4,5 ns, bem como supressão por transferência de elétron do estado MLCT do complexo de Ru-Pireno com uma constante de velocidade de 2,7 x 107 M-1s-1. Este valor é levemente superior ao da supressão de [Ru(bpy)3]2+ no mesmo sítio onde a constante de velocidade encontrada foi de 1,7 x 107 M-1s-1.
1. Balzani, V.; Juris, A.; Venturi, M.; Campagna, S.; Serroni, S. Chem. Rev. 96, 759, 1996.
2. McCafferty, D. G.; Bishop, B. M.; Wall, C. G.; Hughes, S.G.; Mecklenberg, S. L.; Meyer, T. J.; Erickson, B. W. Tetrahedron 51, 4, 1093, 1995.
CAPES