2,2´-BISBENZIMIDAZÓIS: UMA PREPARAÇÃO ALTERNATIVA
Evandro Luiz Dall´Oglio1 (PG), César Zucco1 (PQ) e Marcos Caroli Rezende2 (PQ)
1Departamento de Química, Universidade Federal de Santa catarina, 88040-900 Florianópolis, SC
2Facultad de Quimica Y Biologia, Universidad de Santiago de Chile, Casila 40, Correo 33, Santiago, Chile
Palavras-Chave: 2,2’-bisbenzimidazóis, hexacloroacetona, ultra-som
Introdução:
2,2´-bisbenzimidazóis constituem uma família de heterociclos de interesse, principalmente, como ligantes metálicos1-3. Um método tradicional para a sua preparação envolve a reação de o-fenilendiaminas com derivados do ácido oxálico1,2,4.
A reação clássica de Phillips entre uma diamina aromática e o ácido tricloroacético, em meio fortemente acídico, também, pode fornecer bisbenzimidazóis3. Derivados do ácido tricloroacético, como ésteres de tricloroacetamida e tricloroacetimidato5, podem, também, ser empregados. O uso do tricloroacetimidato5, sensível à água, fornece bisbenzimidazóis, mas o método é limitado a o-fenilendiaminas ativadas e produz baixos rendimentos. Em adição, ésteres tricloroacetimidatos ou seus sais não são disponíveis comercialmente, requerendo sua preparação a partir de tricloroacetonitrila e um álcool.
O emprego de tricloroacetona e hexacloroacetona como agentes acilantes de nucleófilos sulforados, oxigenados e nitrogenados tem sido profundamente estudado pelo nosso grupo.6-9
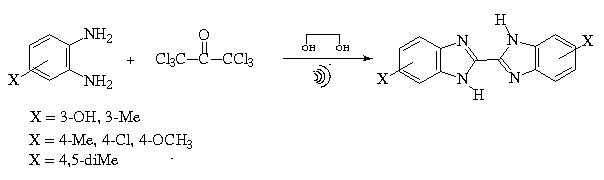
Neste trabalho, descreve-se um novo método para a preparação de 2,2´-bisbenzimidazóis, baseado nas reações entre 1,2-fenilenodiaminas substituídas com hexacloroacetona em etilenoglicol com posterior sonicação da mistura reacional, conforme esquema.

Método:
Em todas as reações utilizou-se um sonicador tipo B. Braun Labsonic, equipado com um probe ultra-sônico de 600-Watt, frequência de 20 KHz e um probe de aço inoxidável para medida da temperatura. O controle da temperatura foi realizado utilizando-se banho termostatizado. Todos os reagentes utilizados tinham pureza analítica. As estruturas dos produtos foram determinadas via análises espectroscópicas.
Resultados:
A reação de hexacloroacetona com excesso de 1,2-fenilendiaminas substituídas (3-metil-, 3-hidroxi-, 4-metil-, 4-cloro-, 4-metoxi- e 4,5-dimetil) foi realizada em etilenoglicol, entre 40-50°C, com a formação do correspondente bisbenzimidazol substituído, com bons rendimentos.
Em todos os casos, observou-se que o uso de ultra-som diminui o tempo reacional, aumentando os rendimentos dos produtos no processo. A boa nucleofilicidade da diamina aromática, determinada pela natureza dos substituíntes no anel, é um requisito essencial para o método; grupos sacadores de elétrons (4,5-dicloro, 3-nitro e 4-nitro) não reagem nessas condições.
Conclusões:
i) as reações de 1,2-fenilendiaminas substituídas com hexacloroacetona, na presença de energia na faixa do ultra-som, demonstrou ser um bom método alternativo para a obtenção de 2,2´-bisbenzimidazóis;
ii) diaminas aromáticas substituídas com grupos doadores de eletróns favorecem estas reações.
Bibliografia:
1. Fieselman, B.F., Hendrickson, D.N., Stucky, G.D., Inorg. Chem. 1978, 17, 2078-
2084; 2. Boinnard, D., Cassoux, P., Petrouleas, V., Savariault, J.-M. and Tuchagues, J.-P., Inorg. Chem. 1990, 29, 4114-4122; 3. Mueller, E., Bernardinelli, G. and Reedijk, J., Inorg. Chem. 1995, 34, 5979-5988; 4. Lane, E.S., J. Chem. Soc. 1953, 2238; 5. Holan, G., Samuel, E. L., Ennis, B.C. and Hinde, R.W. J. Chem. Soc. (C) 1967, 20-25; 6. Dall´Oglio, E.L., Rezende, M.C. and Zucco, C., Tet. Letters, 1996, 37, 5265-5268; 7. Dall´Oglio, E. L., Rezende, M. C., Marques, C. A. and Zucco, C. Liebigs Ann. / Recueil, 1997, 925-929; 8. R. A. Rebelo, M. C. Rezende, F. Nome, C. Zucco, Synth. Comm., 1987, 17, 1741-8; 9. J. R. Salim, M. C. Rezende, F. Nome, Synth. Comm., 1989, 19, 1181-7.
CAPES, PRONEX, CONICYT