PROPRIEDADES CATALÍTICAS DE FERRO E MANGANÊSPORFIRINAS PENTAFLUOROFENIL E SULFONATOFENIL SUBSTITUÍDAS EM SISTEMAS HETEROGÊNEOS
Ana Paula Masson (IC)1, Daniela G. Abreu (PG)1 e Yassuko Iamamoto (PQ)1
1Departamento de Química da Faculdade de Filosofia, Ciências e Letras de Ribeirão Preto. Avenida Bandeirantes, 3900, CEP: 14040-901, Ribeirão Preto, SP.
'palavras-chave': metaloporfirinas, catalisadores, oxidação
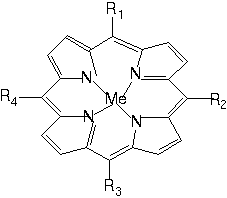
[Me(TF15PPSO3Na)]Cl
R1=R2=R3=
-C6F5 R4=
-C6H4SO3Na Me=
Fe ou Mn Neste
trabalho , foram realizadas as sínteses das metaloporfirinas
assimétricas [Fe(TF15PPSO3Na)]Cl,
[Mn(TF15PPSO3Na)]Cl, e sua ancoragem a uma
matriz sólida. As propriedades catalíticas destes
sistemas foram estudadas em reações de oxidação,
utilizando-se iodosilbenzeno como doador de oxigênio e
(Z)-cicloocteno como substrato.

A síntese foi realizada utilizando-se a proporção pirrol : F5PhCHO : PhCHO de (4 : 2,5 : 1,5), e p-cloranil como oxidante. Foi obtida a mistura de porfirinas mono, bis, tris e tetrapentafluorofenil substituídas. A separação e purificação por cromatografia em coluna foi conseguida para as espécies mono e bissubstituídas. A semelhança das estruturas da H2(TF15PP) e H2(TF20PP) dificultou a separação das mesmas por cromatografia em coluna convencional. A introdução de um grupo carregado (-SO3-) na posição meta do grupo fenil da H2(TF15PP) possibilitou a separação da H2TF15PPSO3H da H2(TF20PP). A sulfonação foi conseguida pela reação do ácido clorossulfônico com a H2P dissolvida em diclorometano (DCM). A identificação das diferentes H2P foi feita por cromatografia em camada delgada (CCD) e RMN 1H. Ferro foi inserido na porfirina base-livre segundo metodologia descrita em [4] utilizando-se cloreto de ferro como sal fornecedor de metal. Já a inserção de manganês na H2P foi realizada segundo procedimento descrito em [5], utilizando-se acetato de manganês como sal fornecedor de metal. Após tratamentos em colunas de resina de troca iônica, obteve-se a [Fe(TF15PPSO3Na)]Cl e [Mn(TF15PPSO3Na )]Cl. As MeP sulfonadas foram ancoradas em sílica (SiN+) contendo trimetilamônio em sua superfície. Foram feitos estudos sobre a eficiência catalítica destes sistemas em meio heterogêneo. Os dados encontram-se abaixo.
|
Catalisador |
Ciclooctenóxido, % |
|
[Fe(TF15PPSO3Na)]Cl * |
92 |
|
FeTF15PPSO3-SiN+ ** |
79 |
|
[Mn(TF15PPSO3Na)]Cl * |
100 |
|
MnTF15PPSO3-SiN+ ** |
95 |
Condições: 25°C, agitação magnética, solvente = DCE, presença de O2. *PhIO/MeP~20, tempo de reação = 1h, [MePs] ~3 x 10-4 mol.L-1. ** MeP/PhIO/Cicloocteno = 1/20/60555 (MeP-SiN+), tempo de reação = 7h.
Apesar da FeP e MnP em sistemas homogêneos e heterogêneos terem apresentado bons rendimentos de produto na epoxidação do (Z)-cicloocteno, as reações com os catalisadores suportados são mais lentas (aproximadamente 7 horas) que com o respectivo catalisador em sistema homogêneo (aproximadamente 1 hora). As reações em meio heterogêneo são mais lentas porque o sítio catalítico da MeP suportada é mais polar que o sítio da MeP em 1,2-dicloroetano (DCE). Isto dificulta o acesso do oxidante (PhIO) e substrato, que são pouco polares, ao sítio catalítico, bem como a difusão do produto oxidado (que é mais polar) formado no sítio catalítico para o interior da solução.
A
MnPS, em meio homogêneo (C-ox= 100%) e em meio heterogêneo
(C-ox=95%), apresentou-se mais eficiente que a FePS (C-ox=92% e
79%, respectivamente).
[1] D. R. Leonard and J. R. L. Smith, J. Chem. Soc., Perkin Trans. 2 (1990) 1917.
[2] M.S. Chorghade, D.R. Hill, E.C. Lee, R.J. Pariza, D.H. Dolphin, F. Hino and L.Y. Zhang, Pure and Appl. Chem. 68 (1996) 753.
[3] a) D. Pattou, G. Labat, S. Defrance, J.L. Seris and B.Meunier, Bull. Soc. Chim. Fr. 131 (1994) 78.
[4] K.M. Kadish; C- Araullo-McAdams; B.C. Han; M.M. Franzen, J. Chem. Soc. Faraday Trans 88 (1992), 3197.
[5] A.D. Adler, F.R. Longo, J. Org. Chem. 32 (1967) 476.