
ESTUDO DA DECOMPOSIÇÃO DE NITRATOS NA PREPARAÇÃO DE CATALISADORES ÓXIDOS DO TIPO ALUMINATO
Angela Sanches Rocha1 (PG) e Heloysa Martins Carvalho Andrade2 (PQ)
1Departamento de Físico-Química, Instituto de Química, Universidade Federal do Rio de Janeiro
2Departamento de Química Geral e Inorgânica, Instituto de Química, Universidade Federal da Bahia
Palavras-chave: nitrato, termogravimetria, estabilidade térmica
Catalisadores óxidos mistos são utilizados em alguns processos industriais, nos quais as condições de operação são severas, por exemplo os aluminatos no hidroprocessamento do petróleo.
Estes catalisadores devem ser estáveis na temperatura e pressão de trabalho e ser resistentes a venenos bem como ao vapor d’água. Desta maneira este materiais geralmente possuem baixa área específica, devido às elevadas temperaturas de calcinação as quais são submetidos durante a preparação.
Os catalisadores em estudo possuem diferentes proporções de MgO, CaO, ZnO e K2O em alumina e foram testados na reforma a vapor de óleos residuais e geração de hidrogênio, numa faixa de temperatura de 600 a 800°C. Desta maneira, o estudo da estabilidade térmica destes materiais é de fundamental importância para determinar a temperatura de calcinação e a faixa de operação em que são estáveis.
A metodologia empregada para esta avaliação, consiste em analisar a perda de massa e a entalpia envolvida nos eventos associados às reações térmicas que os precursores sofrem. As mesmas análises foram efetuadas com os sais, nitratos, utilizados na preparação dos precursores, para identificação de cada evento.
Por FTIR foram identificadas as bandas de cada nitrato separadamente e dos precursores contendo diferentes misturas dos sais.
Experimentalmente cinco famílias de precursores foram preparadas mediante mistura dos nitratos em diferentes proporções, quais sejam: Ca(NO3)2.4H2O, Al(NO3)3.9H2O, Mg(NO3)2.6H2O, Zn(NO3)2.6H2O e KNO3, seguido de pastilhamento. E as composições normalizadas em óxido estão na Tabela 01.
Tabela 01: Composição química em percentagem de óxido no precursor
Precursor |
%Al2O3 |
%CaO |
%MgO |
%ZnO |
%K2O |
|
PRE01 |
55 |
40 |
- |
- |
4 |
|
PRE02 |
60 |
20 |
20 |
- |
- |
|
PRE03 |
40 |
40 |
20 |
- |
- |
|
PRE04 |
60 |
20 |
- |
20 |
- |
|
PRE05 |
60 |
- |
40 |
- |
- |

As curvas TG/DTG e DTA foram obtidas através da termobalança TGA-H50 e célula DTA-50, respectivamente, ambas da Shimadzu, sob fluxo ar sintético (50 mL/min), cadinho de platina, razão de aquecimento de 10°C/min até 1100°C.
Com a utilização de um espectrofotômetro JASCO, Valor-III, realizou-se as análises de FTIR na região de 4000 a 400 cm-1.
Com base nos ensaios termogravimétricos e DTA foi observado que todos os precursores, exceto o PRE01, apresentam pequena perda de massa acima de 700°C, sendo que esta perda é menor nos materiais que contém magnésio. Isto se deve a completa decomposição dos nitratos até 700°C, com exceção do KNO3 que se decompõe a uma temperatura mais elevada.
A pequena perda a temperaturas mais elevadas pode ser atribuída à água estrutural associada à alumina, já que foi observada apenas na decomposição do Al(NO3 )3.9H2O, e foi confirmada por FTIR dos precursores calcinados até 1000°C.
 A
decomposição dos nitratos em óxidos ocorrem
segundo a reação (1), por polarização do
íon nitrato pelo cátion, quebrando-se em O2-
e NOx. O poder polarizante do cátion é muito
importante, já que NO3- é uma base dura e,
portanto, não é facilmente polarizável.
A
decomposição dos nitratos em óxidos ocorrem
segundo a reação (1), por polarização do
íon nitrato pelo cátion, quebrando-se em O2-
e NOx. O poder polarizante do cátion é muito
importante, já que NO3- é uma base dura e,
portanto, não é facilmente polarizável.
MNO3
![]() MO + NOx (1)
MO + NOx (1)
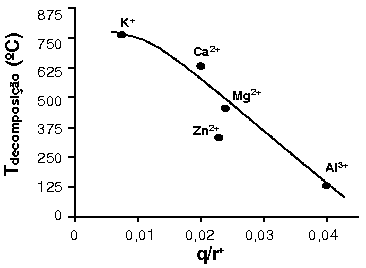
Como o ânion é o mesmo, quanto mais polarizante o cátion, mais fácil será a decomposição do nitrato. Isto eqüivale a uma elevada relação carga/raio .
Figura
1: Temperatura de decomposição de nitratos em função
da relação carga/raio (q/r+)
A baixa temperatura de decomposição do Zn(NO3)2 se deve a presença dos orbitais d que afetam a blindagem do núcleo, consequentemente afetando o seu poder polarizante.
Pelas curvas TG, a decomposição de cada nitrato pode então ser identificada nos precursores, sendo que, de forma geral, a temperatura em que ocorrem, muda em relação ao sais puros, o que é confirmado pelo FTIR, pelo deslocamento da banda atribuída ao nitrato (1385 cm-1).
Assim sendo, pode-se concluir que para os catalisadores serem utilizados na reforma a vapor de pesados, na faixa de temperatura desejada, estes devem ser calcinados pelo menos a 800°C, para garantir que não sofreram nenhuma modificação mensurável durante a reação, devida a temperatura.
(CAPES)