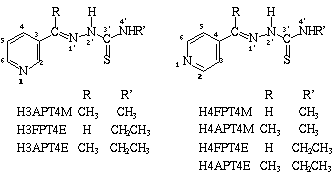
COMPLEXOS DE ZINCO(II) DE TIOSSEMICARBAZONAS HETEROCÍCLICAS N(4’)-SUBSTITUÍDAS DERIVADAS DE FORMIL E ACETILPIRIDINA
Wanderlene Ferreira Nacif (PG), Ricardo França Furtado da Costa (PG) e Heloisa Beraldo (PQ)
Departamento de Química – Instituto de Ciências Exatas
Universidade Federal de Minas Gerais
palavras-chave: formilpiridina tiossemicarbazona, acetilpiridina tiossemicarbazona, zinco(II)
Tiossemicarbazonas e seus complexos metálicos são compostos que apresentam uma ampla faixa de aplicações biológicas como bactericidas, anti-inflamatórios, fungicidas, antimaláricos, antitumorais e antivirais(1,2). Vários estudos foram feitos com complexos metálicos de tiossemicarbazonas derivadas de 2-formil e 2-acetilpiridina(3). Em alguns casos a mudança da cadeia lateral para as posições 3- e 4- do anel provoca uma diminuição da capacidade quelante e da atividade biológica, mas são conhecidos exemplos de tiossemicarbazonas bidentadas cuja atividade foi comprovada, como a tiacetazona empregada na clínica no tratamento da tuberculose(4). Por outro lado, sabe-se que substituintes no nitrogênio terminal fazem aumentar a atividade desses compostos. Nesse trabalho preparamos os complexos de zinco(II) de tiossemicarbazonas N(4’)-metil e N(4’)-etil substituídas derivadas de 3- e 4-formilpiridina (H4FPT4M, H3FPT4E e H4FPT4E) e 3- e 4-acetilpiridina (H3APT4M, H4APT4M, H3APT4E e H4APT4E) (Fig. 1).
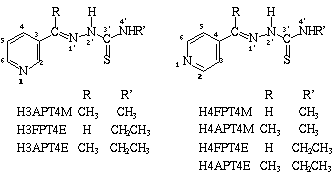
Figura 1: Estrutura dos ligantes 3- e 4-formilpiridina e
3- e 4-acetilpiridina tiossemicarbazona N(4’)-substituídas
Os ligantes foram sintetizados conforme descrito na literatura(5). Os complexos foram preparados reagindo-se os ligantes com ZnCl2, na proporção 2:1, em etanol, sob agitação magnética e refluxo. Os sólidos obtidos foram filtrados e lavados com etanol e éter etílico e em seguida secados sob vácuo. Os complexos formados foram caracterizados por microanálise, medidas de condutimetria, espectrometria de absorção na região do infravermelho e ressonância magnética de 1H e de 13C.
Os resultados de microanálise (Tabela 1) sugerem a formação de complexos do tipo [Zn(HL2)Cl2] com H4FPT4M, H4FPT4E e H3APT4E e [Zn(HL)Cl2] com H3APT4M, H4APT4M, H3FPT4E e H4APT4E. De acordo com medidas de condutimetria (Tabela 1) os complexos são não-eletrólitos, confirmando as estruturas propostas.
Tabela 1: Análise elementar e medidas de condutimetria dos complexos metálicos
|
Complexo |
% C Exp. (Calc.) |
% H Exp. (Calc.) |
% N Exp. (Calc.) |
LM (ohm-1.cm2.mol-1) |
|
[Zn(H4FPT4M)2Cl2] |
36,36 (35,39) |
4,09 (4,08) |
21,07 (20,64) |
6,07 |
|
[Zn(H3APT4M)Cl2] |
32,03 (31,37) |
2,88 (3,51) |
16,16 (16,26) |
7,70 |
|
[Zn(H4APT4M)Cl2] |
31,25 (31,36) |
2,96 (3,48) |
15,92 (16,26) |
6,45 |
|
[Zn(H3FPT4E)Cl2] |
31,73 (31,37) |
3,46 (3,51) |
16,10 (16,26) |
5,72 |
|
[Zn(H4FPT4E)2Cl2] |
35,24 (36,71) |
3,85 (4,79) |
18,02 (19,02) |
6,60 |
|
[Zn(H3APT4E)2Cl2] |
38,63 (38,93) |
4,54 (5,23) |
17,66 (18,16) |
7,48 |
|
[Zn(H4APT4E)Cl2] |
33,60 (33,48) |
3,62 (3,93) |
15,06 (15,62) |
5,72 |
Os espectros de RMN de 1H dos complexos apresentam um sinal que varia de d=10,28 a d=11,84, atribuído ao hidrogênio N(2’)-H da cadeia lateral das tiossemicarbazonas com ligação de hidrogênio com o solvente (DMSO). Os espectros de absorção na região do infravermelho dos ligantes apresentam bandas em 1585-1590 cm-1 e 780-810cm-1 atribuídas às vibrações n(C=N) e n(C=S), respectivamente. Essas absorções deslocam-se para 1570-1610 cm-1 e 815-740 cm-1 nos espectros dos complexos de [Zn(H3APT4M)Cl2], [Zn(H4APT4M)Cl2], [Zn(H3FPT4E)Cl2] e [Zn(H4APT4E)Cl2] indicando a coordenação do ligante de modo bidentado, através do nitrogênio imínico N(1’) e do enxofre da tiona(6). Nestes casos, as vibrações referentes às ligações Zn-Cl e Zn-N(1’) encontram-se na região entre 260-280 cm-1 e 270-290 cm-1, respectivamente. Já para os complexos em que os ligantes estão coordenados de forma monodentada, observa-se um deslocamento na absorção referente ao modo de deformação da piridina fora do plano de 595-610 cm-1 nos ligantes para 625-640 cm-1 nos respectivos complexos. As vibrações referentes às ligações Zn-Cl e Zn-N(pi) encontram-se na região entre 290-320 cm-1 e 260-310 cm-1, respectivamente(6).
(1)Kovala-Demertzi, D. et al. J. Inorg. Biochemistry, 68, 147-155 (1997)
(2)Diaz, A. et al. Inorg. Chim. Acta, 275-276, 552-556 (1998)
(3)Padheyé and Kauffman, G. B., Coord. Chem. Rev, 63, 127 (1985)
(4)Colebls, R. L., et al. Am. Ver. Respir. Dis., 139, 1082 (1989)
(5)Lima, R. L., “Complexos metálicos de novas tiossemicarbazonas e ligantes de estrutura relacionada”, ICEx-Departamento de Química/UFMG (Dissertação),1997
(6) Lima, R. L. et al., no prelo
(CNPq)