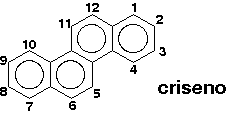
EFEITO DA POSIÇÃO DO SUBSTITUINTE METIL
NA AÇÃO CARCINOGÊNICA DO CRISENO
Marcelo Brito Carneiro Leão (PQ)1 e Antonio Carlos Pavão (PQ)2.
Departamento de Química. Universidade Federal Rural de Pernambuco
Departamento de Química Fundamental. Universidade Federal de Pernambuco
palavras-chave: carcinogênese, criseno, orbital molecular
O criseno é um carcinógeno fraco, entretanto o seu derivado 5-metilcriseno é altamente potente em relação à ação carcinogênica. Já um outro derivado, o 1-metilcriseno, é inativo. Em um estudo completo do criseno e seus derivados metilados, Kimri e Gayoso1 quantificaram esta ação por meio de um índice de carcinogenicidade relacionado ao número de tumores induzidos em ratos.

Neste trabalho foram realizados cálculos de orbitais moleculares do criseno e de seus derivados substituídos. A análise da ação carcinogênica foi baseada em um modelo teórico proposto por Leão e Pavão2, que relaciona a ação carcinogênica dos compostos químicos com parâmetros eletrônicos obtidos destes cálculos.
Tabela 1. Parâmetros AM1 e índice de carcinogenicidade do criseno e derivados
|
Compostos |
EA (eV) |
DH-L(eV) |
Dq |
m |
Hf (Kcal/mol) |
DHf (Kcal/mol) |
Carcinogenicidade1 |
|
5-metil-criseno |
1,121 |
7,997 |
0,311 |
0,237 |
75,256 |
23,661 |
4,5 |
|
2-metil-criseno |
1,083 |
8,016 |
0,305 |
0,350 |
68,406 |
23,328 |
1,1 |
|
criseno |
1,093 |
7,995 |
0,303 |
0,000 |
76,004 |
25,804 |
0,5 |
|
3-metil-criseno |
1,089 |
8,014 |
0,307 |
0,335 |
68,446 |
22,077 |
0,3 |
|
4-metil-criseno |
1,119 |
7,983 |
0,308 |
0,247 |
74,970 |
27,014 |
0,3 |
|
6-metil-criseno |
1,109 |
7,999 |
0,307 |
0,319 |
69,578 |
27,125 |
0,3 |
|
1-metil-criseno |
1,093 |
8,004 |
0,305 |
0,297 |
69,539 |
29,006 |
0,0 |
Neste modelo a interação do carcinógeno com o DNA é descrita como um processo de transferência de elétrons do HOMO da guanina para o LUMO do carcinógeno. Utilizamos neste trabalho cálculos semiempíricos AM13, realizados no programa computacional MOPAC934 Os resultados obtidos destes cálculos são apresentados na tabela 1.
Foi realizado ainda, um tratamento multivariado dos dados, através da análise de componentes principais (ACP)5. Nesta etapa do trabalho observamos que PC1, que teve como variáveis de maior peso AE, energia de interação (DH-L) e o calor de formação (Hf), e PC2 que teve como variável de maior peso a atração eletrostática (Dq), não conseguiram ordenar corretamente a ação carcinogênica dos compostos estudados. Entretanto, PC3 revelou-se bastante importante para uma correta separação dos compostos segundo sua ação carcinogênica. Esta componente apresentou como variável de maior peso a diferença entre o calor de formação do composto e do seu metabólito efetivo (DHf), que neste caso é o cátion epóxido. Observou-se que quanto menor o DHf, mais ativo será o composto. Isto reflete a maior facilidade na formação do carcinógeno efetivo.
Esta conclusão reforça a necessidade do conhecimento da rota metabólica para a caracterização da ação de carcinógenos, em especial no caso de isômeros, onde as diferenças de EA, Dq e DH-L são em geral muito pequenas. Assim, o parâmetro DHf nos casos de isômeros torna-se essencial para uma boa descrição da ação carcinogênica. Este resultado comprova ainda, pela correta reprodução do índice experimental, a adequação deste modelo teórico na análise da ação carcinogênica do criseno
Referências Bibliográficas
S. Kimri and J. Gayoso. J. Mol. Struct. (Theochem). 362, 141(1996).
M. B. C. Leão and A. C. Pavão. Int. J. Quantum Chem. 62, 323(1997).
M. J. S. Dewar, E.G. Zoebisch, E.F. Healy and J.J.P. Stewart; J. Am. Chem. Soc. 107, 3902(1985).
“MOPAC 93.00 Manual”, J.J.P. Stewart, Fujitsu Limited, Tokyo, Japan (1993).
D. L. Massart at al. Evaluation and optimization of laboratory methods and analytical procedures. Elsevier. New York – 1978.