NOVOS
DERIVADOS TIAZOLIDINÔNICOS: PREPARAÇÃO E
AVALIAÇÃO DA ATIVIDADE ANTIINFLAMATÓRIA
Isabele Cristine B. Moraes (IC); Fabíola Soraia Vital
Campos Barbosa da Silva (PG);
Ivone Antônia de Sousa (PQ); Maria do Carmo Alves de Lima
(PQ);
Suely Lins Galdino (PQ) e Ivan da Rocha Pitta (PQ)
Departamento de Antibióticos – CCB –
Universidade Federal de Pernambuco
Cidade Universitária – 50.670-901 – Recife –
PE
Palavras-chave:
atividade antiinflamatória, arilideno-tiazolidinonas.
Introdução:
O
ensaio farmacológico de uma substância envolve uma série
de etapas, muitas vezes surpreendente através de seu estudo
dinâmico, cujas propriedades correlacionam-se com o campo da
medicina pré-clínica. A presença do anel
tiazolidínico em penicilinas e derivados relacionados foi o
primeiro reconhecimento de sua ocorrência na natureza. Este
fato levou Labouta e colaboradores (1987) a desenvolver um extensivo
estudo da relações entre estrutura química e
atividade biológica. De acordo com trabalhos anteriores (Singh
e cols. – 1986; Boschelli e cols. – 1992), também
podemos afirmar que compostos que possuem o núcleo
tiazolidinônico apresenta uma potencial atividade
antiinflamatória e analgésica.
Objetivos:
O
presente trabalho tem por objetivos a síntese, caracterização
química e avaliação da atividade
antiinflamatória de derivados
3-(4-metilbenzil)-5-arilideno-tiazolidinônicos.
Métodos:
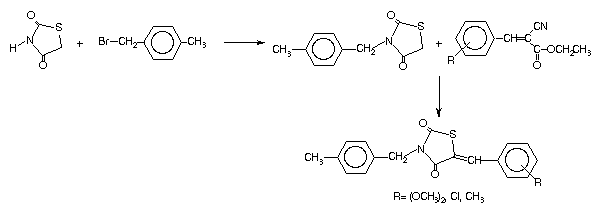 Os
derivados 3-(4-metilbenzil)-5-arilideno-tiazolidinônicos foram
obtidos em duas etapas. Inicialmente obteve-se a
3-(4-metilbenzil)-tiazolidina-2,4-diona a partir da reação
N-alquilação da tiazolidina-2,4-diona com o brometo de
4-metilbenzil. Na segunda etapa, o intermediário N-alquilado
sofre uma reação de condensação com
2-arilideno-cianacetato de etila substituídos, em etanol e na
presença de piperidina como catalisador. Todos os compostos
sintetizados foram purificados e caracterizados por métodos
físico-químicos e espectrométricos usuais.
Os
derivados 3-(4-metilbenzil)-5-arilideno-tiazolidinônicos foram
obtidos em duas etapas. Inicialmente obteve-se a
3-(4-metilbenzil)-tiazolidina-2,4-diona a partir da reação
N-alquilação da tiazolidina-2,4-diona com o brometo de
4-metilbenzil. Na segunda etapa, o intermediário N-alquilado
sofre uma reação de condensação com
2-arilideno-cianacetato de etila substituídos, em etanol e na
presença de piperidina como catalisador. Todos os compostos
sintetizados foram purificados e caracterizados por métodos
físico-químicos e espectrométricos usuais.
Na determinação da
atividade antiinflamatória utilizou-se o método de
Winter e colaboradores (1962), que se baseia na inibição
do edema de pata induzido pela carragenina. Para cada via de
administração, oral e intra-peritoneal, utilizou-se 6
grupos de 8 ratos machos dos quais, 4 grupos para avaliação
da atividade antiinflamatória, 1 grupo padrão tratado
com a indometacina e 1 grupo controle, tratado com solução
salina a 0,9%. Trinta minutos após a administração
das substâncias, injetou-se por via subcutânea (plantar),
0,1mL de carragenina a 1% na pata esquerda e igual volume de solução
salina a 0,9% na pata direita. O edema de pata foi medido através
de imersão até o mielóide lateral. Esta medida
foi tomada em intervalos de 30 minutos, durante 6 horas.
Resultados
e Discussão:
Os
compostos
3-(4-metilbenzil)-5-(2,4-dimetoxiarilideno)-tiazolidina-2,4-diona
(GQ-6),
3-(4-metilbenzil)-5-(3-cloroarilideno)-tiazolidina-2,4-diona (GQ-7)
e 3-(4-metilbenzil)-5-(4-metilarilideno)-tiazolidina-2,4-diona (GQ-8)
foram purificados, apresentando, respectivamente, rendimentos de
85, 65 e 43% e pontos de fusão de 161, 145 e 141ºC. Suas
estruturas foram comprovadas por análises no infravermelho,
por ressonância magnética nuclear protônica e por
espectrometria de massa.
A
injeção plantar da carragenina produziu edema e aumento
gradativo da pata esquerda, com pico máximo em 180 minutos
após a injeção. As três substâncias
citadas, com uma dose fixa de 20mg/Kg de peso, foram administradas 30
minutos antes da injeção da carragenina. Os grupos
tratados apresentaram inibição similar ao grupo padrão
tratado com a indometacina, variando o tempo de início da
inibição. Tanto na via de adminstração
oral como na via intra-peritoneal, com inibições
respectivas de 32% e 43% do edema de pata, destacou-se o composto GQ7
como mais ativo.
Conclusões:
A
presente investigação demonstra que a substância
3-(4-metilbenzil)-5-(3-cloroarilideno)-tiazolidina-2,4-diona (GQ-7)
apresenta potencialidade de ação quando no tratamento
de edema localizado em ratos. Tais resultados motivam estudos
posteriores para validação de outros compostos mais
eficazes, estruturalmente análogos aos fármacos
tiazolidinônicos já utilizados na terapêutica como
antiinflamatórios.
Bibliografia:
Labouta,
I.M., Salama, H.M., Eshba, N.H., Kader, O., El-Chrbini, E. Eur.
J. Med. Chem., 22, 485-489. 1987.
Singh,
I.P., Saxena, A.K. , Shanker, K. Indian J. of Chem. 25B,
838-843. 1986.
3. Boschelli,
D.H., Connor, D.T., Kuipers, P.J., Wright, C.D. Bioorg. & Med.
Chem. Letters. 2(7), 705-708. 1992.
Winter,
C.A., Risley, E.A., Nuss, G.W., Proc. Soc. Exp. Biol. Med.
111, 544-547, 1962.
-
Apoio: CNPq e CAPES
 Os
derivados 3-(4-metilbenzil)-5-arilideno-tiazolidinônicos foram
obtidos em duas etapas. Inicialmente obteve-se a
3-(4-metilbenzil)-tiazolidina-2,4-diona a partir da reação
N-alquilação da tiazolidina-2,4-diona com o brometo de
4-metilbenzil. Na segunda etapa, o intermediário N-alquilado
sofre uma reação de condensação com
2-arilideno-cianacetato de etila substituídos, em etanol e na
presença de piperidina como catalisador. Todos os compostos
sintetizados foram purificados e caracterizados por métodos
físico-químicos e espectrométricos usuais.
Os
derivados 3-(4-metilbenzil)-5-arilideno-tiazolidinônicos foram
obtidos em duas etapas. Inicialmente obteve-se a
3-(4-metilbenzil)-tiazolidina-2,4-diona a partir da reação
N-alquilação da tiazolidina-2,4-diona com o brometo de
4-metilbenzil. Na segunda etapa, o intermediário N-alquilado
sofre uma reação de condensação com
2-arilideno-cianacetato de etila substituídos, em etanol e na
presença de piperidina como catalisador. Todos os compostos
sintetizados foram purificados e caracterizados por métodos
físico-químicos e espectrométricos usuais.