

INFLUÊNCIA DE FENÓIS NA BACIA DO RIO TIBAGI
Maria Josefa Santos Yabe (PQ)1, Sônia Maria Nobre Gimenez (PQ)1, Márcia Cristina Bisinoti (IC)1, Márcia Alessandra Azevedo Paes (IC)1, Rosana da Rocha Lobo (IC)1, Edilene Sarge Figueiredo (IC)1
1Departamento de química – Universidade Estadual de Londrina CP6001, 86051-970, Londrina- Pr
email: mjyabe@npd.uel.br
Palavras chaves: fenóis, bacia do rio tibagi e águas interiores
Introdução
Um grande número de compostos fenólicos pode ser formado naturalmente por processos biogeoquímicos (Hoekstra, et all, 1999). São encontrados em pequenas concentrações em águas naturais por serem constituintes das plantas, podendo também ser formados durante os processos de humificação no solo. Compostos fenólicos são amplamente usados na indústria e estão presentes em águas de despejo como subprodutos de indústria de papel e celulose, devido à composição de lignina e tanino; de tintas, farmacêutica e agroquímica (Johnson et all, 1999, Svitel e Miertus, 1998). São também liberados no ambiente pela degradação de pesticidas com estrutura fenólica. Fenóis e clorofenóis têm sido definidos como poluentes devido à sua toxicidade e persistência à biodegradação. Legislação ambiental recente restringe quantidades de fenóis no ambiente. A concentração máxima de fenol na água, para proteção da saúde pública é de 3,5 mg L-1 (EPA, 1980), e a faixa de concentração de compostos fenólicos em águas superficiais para propósitos de potabilização varia de 1 a 10 mg L-1. Devido à grande interferência agroindustrial na bacia do rio Tibagi, foram desenvolvidos estudos para a avaliar a contribuição de fenóis na água desta bacia de drenagem.
Experimental
Foram realizadas amostragens mensais em oito pontos ao longo do rio Tibagi, de maio/98 a abril/99: Mn– Manancial, exceto setembro/98; Va- Varanal, Su- Surubi, LM- Limoeiro, BF- Barra Funda, IB- Imbituva, UV- Uvaia e CP- Capivara. As amostras de água foram coletadas em garrafas de água mineral, reservadas em geladeira e analisadas o mais rápido possível. Foi realizada extração com sulfato de cobre à pH 4,0 e em seguida ajuste de pH a 10,0 com hidróxido de sódio na presença de aminoantipirina e peróxido dissulfato., A fase clorofórmio foi filtrada em sulfato de sódio anidro. As determinações foram feitas em triplicata em um espectrofotômetro Femto, modelo 482 no comprimento de onda de 460 nm, usando clorofórmio no caminho óptico.
Resultados e discussões
De acordo com o gráfico dos escores das componentes principais 1 e 2 (fig. 1) é possível observar que as amostras sofreram interferência de fenol dependendo das chuvas e da sua localização na bacia de drenagem, relacionando a sua origem: vegetação ou agroindustrial. São formados quatro grupos de amostras distintos pela origem dos compostos fenólicos. Um dos grupos é formado pelas amostras coletadas nos pontos SU, CP e UV, com influência agroindustrial e de maior pluviosidade, de acordo com o gráfico dos escores (fig. 1). As amostras coletadas nos pontos BF e LM, de região agrícola, sofreram interferência de fenol em épocas de pouca chuva no BF e muita chuva no LM. O ponto VA está em um afluente preservado do Tibagi , com vegetação densa em uma grande área na mata da Klabin- cidade de Telêmaco Borba. De características diferentes, separou-se das demais amostras, demonstrando origem provável dos compostos fenólicos na vegetação. Considerados referência, os pontos MN e IB são áreas preservadas, região de campos em Ponta Grossa- Pr, com origem de matéria orgânica de mata ciliar semelhante. Os pontos SU, CP e UV são os pontos que sofrem maior interferência antrópica devido à sua localização na bacia do rio Tibagi, sendo separados dos demais pontos quanto à origem dos compostos fenólicos.


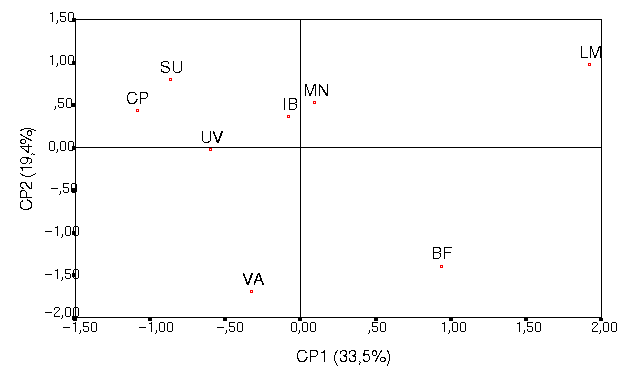



Figura
1: Gráfico dos escores das componentes principais 1 e 2
das amostras da bacia do rio Tibagi-Pr.
Johnson, S. K.; Houk, L.L; Feng, J.; Houk, R. S.; Johnson, D C. 1999, Environ. Sci. Technol., 33,2638-2644.
(Hoekstra, E. J.; Deweerd, H.; De Leer, e. W. B.; Brinkman, U. A T. 1999, Environ. Sci. Technol., 33,2543-2549.
Svitel, J. and Miertus, S. 1998, Environ. Sci. Technol., 32,828-832.
Ambient Water Quality Criteria for Phenol, U. S. EPA 440/5-80-066; U.S.EPA: Washington, DC, 1980.
Finep
UEL