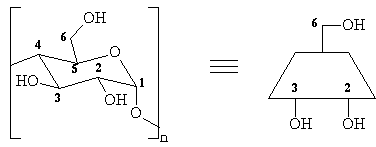
SÍNTESE DE NOVAS FASES QUIRAIS, PERALQUILADAS E PERACILADAS, UTILIZANDO g-CICLODEXTRINAS
Anderson Stoffels Mallmann (IC), Adriana Flach (PG), Marco Aurélio Dessoy (PG), Eduardo Miranda Ethur (PG) e Ademir Farias Morel (PQ)
Departamento de Química - Núcleo de Pesquisa de Produtos Naturais - Universidade Federal de Santa Maria - RS
palavras-chave: ciclodextrina, cromatografia gasosa, enantioseletividade
Introdução e Objetivos:
Apesar da quiralidade ser conhecida desde o século passado, quando Louis Pasteur separou mecanicamente cristais com formas isoméricas de ácido láctico com ajuda de um microscópio óptico, somente há poucos anos tem-se notado a sua imensa importância em termos de interação com materiais biológicos.
Na química atual este fato tem merecido uma crescente atenção. Como conseqüência, a análise configuracional de produtos naturais e a determinação da pureza enantiomérica de medicamentos, defensivos agrícolas e produtos de síntese assimétrica ou de processos de biotransformação são, hoje, o tema central de pesquisa em laboratórios de análise e de síntese, de inúmeras instituições espalhados ao redor do mundo.
Os derivados alquilados e/ou acilados de a- b- e g-ciclodextrinas (representação na Figura 1) tem sido, nos últimos anos, utilizados com muito sucesso como fases estacionárias quirais em cromatografia gasosa capilar, com o objetivo de se determinar a composição enantiomérica e a configuração absoluta de vários compostos voláteis ou possíveis de se tornarem voláteis.
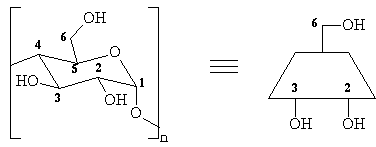
Métodos e Conclusão:
Neste projeto sintetizamos novas fases quirais seletivamente alquiladas e/ou aciladas a partir das b- e g-ciclodextrinas nativas (1 a,b). As fases 6-O-etil-2,3-di-O-pentil-b-ciclodextina (5a), 6-O-etil-2,3-di-O-pentil-g-ciclodextina (5b), 2,3-di-O-iso-valeril-6-O-TBDMS-b-ciclodextina (6a) e 2,3-di-O-iso-valeril-6-O-TBDMS-g-ciclodextina (6b) foram sintetizadas por métodos já descritos na literatura.
A confirmação estrutural das fases foi realizada com base em dados de RMN uni- (1H, 13C e dept 1350) e bi-dimensional (COSY e HMQC). Suas habilidades no reconhecimento de moléculas quirais foram avaliadas em um cromatógrafo a gás Varian 3800
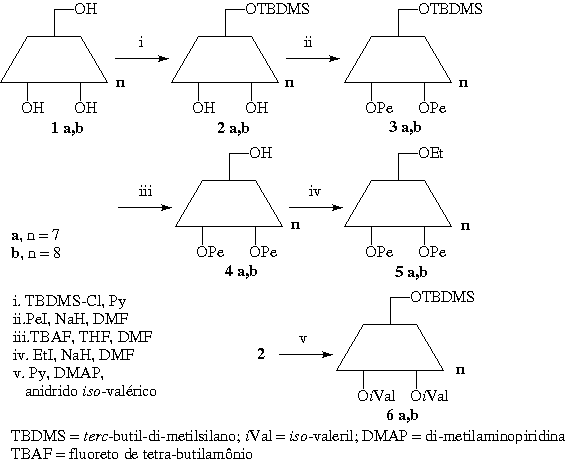
Figura 2 - Esquema de Síntese das novas fases
Bibliografia:
1-De Camp, W. H.; Chirality (1989), 1, 2.
2-W. König, “Gas Chromatographic Enantiomer Separation With Modified Cyclodextrins”, Ed. Hü thig Verlag, Hamburg, 1992
3-J. Boger, R. J. Corcoran and J. M. Lehn, Helvetica Chimica Acta Vol. 61, fasc. 6, (1978) - Nr. 203
CNPq, FAPERGS