ESTUDO TEÓRICO (AB INITIO) DOS EFEITOS DE SUBSTITUINTES NAS PROPRIEDADES ESTRUTURAIS E ELETRÔNICAS DE NÚCLEOS 1,3-BENZODIOXÓLICOS
Mauro Barbosa de Amorim (PQ) e Jorge Gonçalo Fernandez Lorenzo (PG)
Núcleo de Pesquisa de Produtos Naturais - Universidade Federal do Rio de Janeiro
Palavras-chave: efeito anomérico, cálculo ab initio, 1,3-benzodioxolas
INTRODUÇÃO:
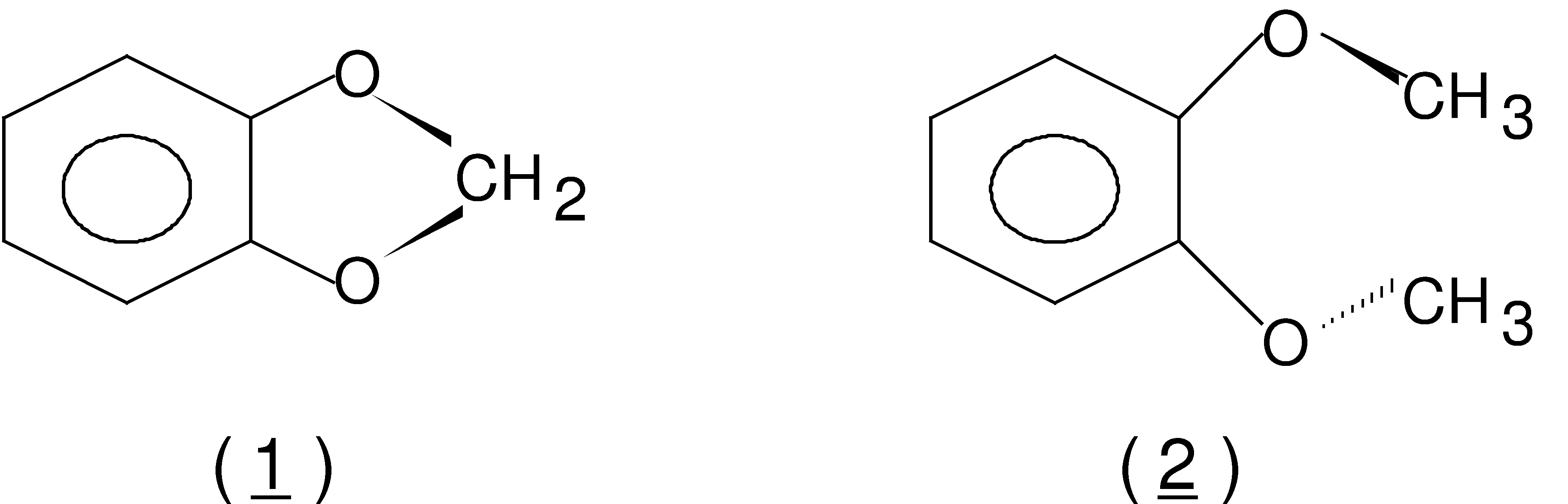
Substâncias com núcleo 1,3-benzodioxólico (1), quando comparadas a seus análogos 1,2-dimetoxilados (2), geralmente apresentam uma maior atividade biológica.1 Uma das possíveis razões para essa diferença de atividade pode estar associada à alterações de distribuição de densidade de carga no núcleo 1,3-benzodioxólico,2 em virtude da ocorrência de efeito anomérico na ponte metilenodioxílica,3 inexistente nos análogos dimetoxilados. Há que se considerar, contudo, que tais substâncias biologicamente ativas apresentam grupos substituintes no sistema benzodioxólico. Não há, entretanto, qualquer relato na literatura sobre o efeito de grupos substituintes nas propriedades estruturais e eletrônicas desse sistema.

OBJETIVOS:
Estudo teórico, através de cálculos ab initio de orbitais moleculares, do efeito de grupos substituintes (doadores e retiradores de elétrons) nas propriedades estruturais e eletrônicas de núcleos 1,3-benzodioxólicos.
METODOLOGIA:
Esses cálculos foram realizados, em nível RHF/6-31G*, em um computador pessoal Pentium MMX, 233 MHz, com 96 MB de memória RAM, utilizando o pacote PC Spartan Plus v 1.5.34 e em um supercomputador IBM RS/6000 SP2 com o pacote Gaussian 94.5 As estruturas inicialmente geradas foram otimizadas sem quaisquer restrições e as estruturas assim obtidas foram caracterizadas como pontos de mínimo na superfície de energia potencial através de análise vibracional (ausência de freqüências imaginárias).
RESULTADOS:
Os resultados obtidos estão sumarizados na tabela abaixo.
|
|
Ângulos diedros (o) a |
Comprimento de ligação C-H (Å) b |
Carga nos átomos c (elétrons) |
|
OH |
14,20 / 14,41 |
1,0836/1,0781 |
- 0,447 / - 0,466 / + 0,466 |
|
CH3 |
13,38 / 13,34 |
1,0836/1,0784 |
- 0,463 / - 0,462 / + 0,484 |
|
H |
13,11 / 13,11 |
1,0835/1,0784 |
- 0,495 / - 0,495 / + 0,594 |
|
E - CHO |
9,74 / 9,84 |
1,0822/1,0784 |
- 0,470 / - 0,480 / + 0,516 |
|
Z - CHO |
8,68 / 8,80 |
1,0819/1,0785 |
- 0,485 / - 0,490 / + 0,565 |
|
NO2 |
6,12 / 6,22 |
1,0809/1,0786 |
- 0,457 / - 0,457 / + 0,478 |
a- Diedros: C7a-O1-C2-O3 e C3a-O3-C2-O1; b- Ligações C2-H1/C2-H2
c- Átomos: O1, O3 e C2
CONCLUSÕES:
Nossos estudos anteriores2 indicaram cargas maiores nos átomos de oxigênio, carbono da ponte metilenodioxílica e carbonos do anel aromático do núcleo 1,3-benzodioxólico do que aquelas calculadas para os átomos correspondentes do 1,2-dimetoxibenzeno, o que pode ser atribuído ao efeito anomérico existente na ponte metilenodioxílica.3 A magnitude do efeito anomérico pode ser avaliada pelas alterações dos ângulos diédricos (C7a-O1-C2-O3 e C3a-O3-C2-O1) e dos comprimentos de ligação C2-H1’/H2’ (1,0835 Å/1,0784 Å) quando comparado aos valores da estrutura plana (estrutura de transição entre as duas configurações angulares) do núcleo 1,3-benzodioxólico. Nossos resultados mostram claramente que os grupos retirantes de elétrons diminuem o efeito anomérico, enquanto grupos doadores de elétrons o acentuam. Não se observa, contudo, uma correlação simples e direta entre essas alterações geométricas e as cargas atômicas calculadas. Cálculos com bases maiores e tratamento pós-Hartree-Fock de correlação eletrônica que, preliminarmente, confirmam essas tendências estão sendo realizados.
BIBLIOGRAFIA:
1. ver, por exemplo, Wang, Y. et al., J. Med. Chem., 1998, 41, 2621.
2. Amorim, M. B. de e Lorenzo, J. G. F., in 22ª Reunião Anual da SBQ, 1999, Poços de Caldas, Livro de Resumos v. 1, QT-017.
3. Sakurai, S., J. Am. Chem. Soc., 1999, 121, 5056.
4. Heher, W. J. et al., Wavefunction, Inc., 18401, Von Karman Ave., Suite
370, Irvine, 92612.
5. Frisch, M. J. et al., Gaussian 94, Revision C.3, Gaussian, Inc., Pittsburgh PA, 1995.
Agradecimentos: NCE–UFRJ