
Resultados e Discussão: A rota sintética empregada para a obtenção dos isômeros está demonstrada nos esquemas 1 e 2, abaixo.
SÍNTESE ENANTIOSSELETIVA DO (R)- E (S)- 2-METIL-4-OCTANOL: ATRIBUIÇÃO DA ESTEREOQUÍMICA ABSOLUTA DO FEROMÔNIO DE AGREGAÇÃO DO BICUDO DA CANA Sphenophorus levis
Paulo Henrique Gorgatti Zarbin* (PQ)1, Aurélia Reckziegel (PQ) 2, Alfredo Ricardo Marques Oliveira (PQ)1, Fábio Simonelli (PQ)1 e Francisco de Assis Marques (PQ)1
1 Departamento de Química - UFPR, Cx.P. 19081 - CEP 81531-990, Curitiba - PR, email:pzarbin@quimica.ufpr.br 2 Institut of Organic Chemistry, University of Hamburg - Alemanha
Palavras-chave: 2-metil-4-octanol, Sphenophorus levis, feromônio
Introdução: O besouro curculionídeo Shenophorus levis é uma espécie conhecida como praga da cana de açúcar no Brasil, com principal incidência na lavoura canavieira do estado de São Paulo. As perdas atribuídas a ação deste inseto giram em torno de 14 toneladas/ha/ano, sendo que a maior dificuldade de controle está no fato de haver ocorrência de ninfas e larvas em locais inacessíveis aos produtos químicos convencionais, abrindo desta forma uma perspectiva bastante interessante para a implantação de técnicas que utilizam semioquímicos como princípio ativo.
Objetivos: Continuando nossos estudos relacionados a ecologia química de S. levis, o objetivo principal desta etapa do trabalho foi o desenvolvimento de uma metodologia sintética para a obtenção enantiosseletiva dos dois isômeros do 2-metil-4-octanol (1), previamente identificado como sendo o feromônio de agregação da espécie1,2. Em adição, a estereoquímica absoluta do produto natural foi atribuída através de análises comparativas de cromatografia gasosa empregando-se coluna quiral, entre os enantiômeros sintéticos e o produto natural isolado do extrato.

Resultados
e Discussão: A rota sintética empregada para a
obtenção dos isômeros está demonstrada nos
esquemas 1 e 2, abaixo.
Esq.1: Síntese do (S)-2-metil-4-octanol (1)
O álcool 2 comercial utilizado como material de partida forneceu a estereoquímica desejada para o produto final, uma vez que não há nenhuma etapa envolvida que possa causar racemização. Cabe frisar apenas que o material de partida (R), levará à formação do produto (S), em função da inversão de prioridades. De maneira análoga, o composto (S)-2 forneceu o feromônio (R)-1.

Esq.2: Síntese do (R)-2-metil-4-octanol (1)
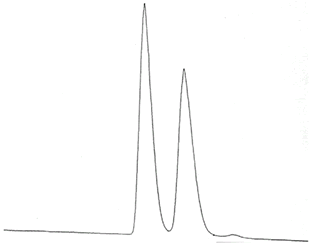
Feromônio Racêmico
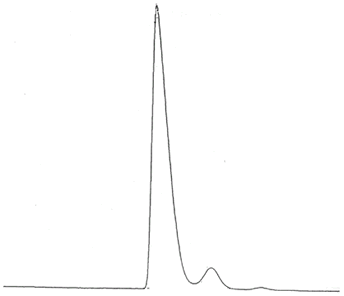
(R)-2-metil-4-octanol
[a]D = -9,21
96 % ee
(S)-2-metil-4-octanol
[a]D = +9,17
96,5 % ee
Feromônio Natural
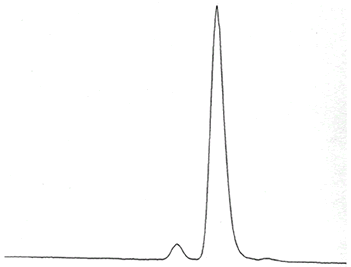
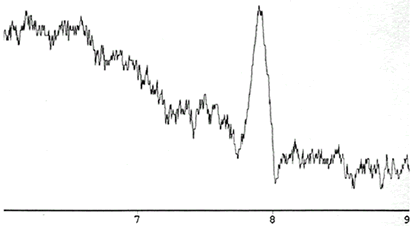
Fig.1: Atribuição da estereoquímica absoluta do feromônio por cromatografia gasosa empregando-se coluna quiral.
Conclusões: A metodologia sintética empregada mostrou-se altamente viável para a obtenção em grandes quantidades e alto excesso enantiomérico dos isômeros do 2-metil-4-octanol (1). Além de ter possibilitado a atribuição da estereoquímica absoluta do feromônio natural, tais compostos estarão sendo empregados em testes de campo para verificar a importância deste centro estereogênico na atividade biológica desta molécula.
Zarbin, P.H.G. et.all., manuscrito em preparação
Zarbin, P.H.G., Arrigoni, E.D.B., Baraldi, P.T., Alves, J.M., Vieira, P.C. Livro de Resumos, I Encontro Brasileiro de Ecologia Química - I EBEQ, Curitiba-PR, Dez/99
IFS ( grant to PHGZ), CNPq, Plantações E. Michelin, UFPR