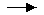 (15NH4)2SO4
+ 2NaOH 215NH3 + Na2SO4
+ H2O (1)
(15NH4)2SO4
+ 2NaOH 215NH3 + Na2SO4
+ H2O (1)OBTENÇÃO DE AQUAMÔNIA-15N PARA A PRODUÇÃO DE COMPOSTOS MARCADOS
Claudinéia Raquel de Oliveira (PG); André César Vitti (PG); Everaldo Máximo (PG); José Albertino Bendassoli (PQ); Paulo César O. Trivellin (PQ)
Laboratório de Isótopos Estáveis – Centro de Energia Nuclear na Agricultura Univeridade de São Paulo (CENA-USP) email: crolivei@cena.usp.br
palavras chaves: nitrogênio 15; amônia anidra; amônia aquosa
Os compostos nitrogenados marcados no isótopo 15N têm sido utilizados em estudos agronômicos e seu emprego, associado à técnica de diluição isotópica, o que caracteriza uma importante ferramenta na elucidação do ciclo do N.
A aquamônia ou amônia aquosa (NH3aq), produzida por hidratação da amônia anidra (Bendassoli et al., 1988), vem sendo usada no Brasil como fertilizante nitrogenado em culturas, como cana-de-acúcar. A partir da 15NH3aq é também possível sintetizar outros compostos enriquecidos entre eles os aminoácidos (alanina e glicina). Este trabalho descreve um método de obtenção da 15NH3aq que servirá de matéria prima para a síntese desses compostos.
O objetivo deste trabalho foi avaliar a eficiência no rendimento da produção da aquamônia utilizando-se de diferentes massas de (NH4)2SO4, a partir da reção (1) e possível diluição isótópica no processo de obtenção da 15NH3aq.
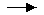 (15NH4)2SO4
+ 2NaOH 215NH3 + Na2SO4
+ H2O (1)
(15NH4)2SO4
+ 2NaOH 215NH3 + Na2SO4
+ H2O (1)
No processo de obtenção de NH3aq foi avaliado a eficiência do método a partir de diferentes massas de (NH4)2SO4 (40, 80 e 150g) com 3 repetições. Para uma das massas de 150g foi realizado testes (4 repetições), utilizando-se do composto ((15NH4)2SO4) préviamente enriquecido no isótopo 15N (3,5 at % em 15N).
A NH3 produzida, a partir da reação dada pela eq. (1), é arrastada por um fluxo de N2 e retida em reatores. Inicialmente o vapor de H2O formado no decorrer da reação passa por um condensador, e em seguida por uma coluna preenchida com pastilhas de NaOH para retenção do vapor remanescente. Na sequência, amônia anidra passa por dois estágios, com o objetivo de promover sua liquefação. O primeiro é constituído por uma serpentina disposta à temperatura de –33 oC onde a amônia passa ao estado de vapor saturado. O segundo estágio do sistema constitue-se de 2 reatores de áço inoxidável: R1 (NH3 anidra) e R2 (NH3aq). A 15NH3 anidra no estado de vapor saturado é liquefeita em R1, refrigerado à –73 oC. O gás de arraste N2, na saída do reator R1, carrega uma pequena massa de amônia que é retida em água desmineralizada contida no R2, mantido à temperatura de aproximadamente 1oC. Em seguida traços remanecentes de NH3 no gás de arraste são retidos e um becker contendo H2SO4 1 mol L-1.
A utilização do (NH4)2SO4 150 g L-1 permite a obtenção de maior massa de NH3aq, já que o rendimento se manteve constante em torno de 80% (Tabela 1), viabilizando sua utilização. Os valores obtidos são sujestivos para a realização de novos testes na avaliação de maiores massas de (NH4)2SO4, entretanto deve se considerar a capacidade do reator, o aumento da perda de 15N quando se trabalha com (15NH4)2SO4.
A retenção da NH3, contida no gás de arraste, em ácido sulfúrico na porção final do sistema, confere ao mesmo vantagens do ponto de vista de segurança, ambiental e econômico.
No processo de obtenção da NH3 aq não foi verificado a ocorrência de diluição isotópica para o teste empregando (15NH4)2SO4, verificado pela marcação do composto final (15NH3aq).
Verifica-se que as perdas no balanço global referente as massas 40 e 150* g estão na ordem de 10%. Com relação as massa de 80 e 150 g as perdas foram mais elevadas (17%). Essa diferença é atribuída ao pouco tempo de recuperação da massa de (NH4)2SO4 resídual do balão de reação contendo NaOH.
Tabela 1. Produção de NH3 anidra e aquosa, utilizando diferentes massas de (NH4)2SO4.
|
(NH4)2SO4
|
Maa |
Map |
Mar |
Produção de NH3aq |
Balanço de massa globa |
|
-------------------------------- Massa (g) ----------------------------- |
------------------% ---------------- |
||||
|
40 |
7,30±0,53 |
8,11±0,77 |
1,17±0,46 |
78,66±7,46 |
90,04±3,22 |
|
80 |
15,00±0,66 |
15,86±0,29 |
1,30±0,13 |
76,92±1,42 |
83,22±1,85 |
|
150 |
28,39±1,12 |
30,40±0,71 |
1,75±0,79 |
78,64±1,83 |
83,16±1,88 |
|
150* |
28,31±0,42 |
31,00±1,58 |
4,61±1,67 |
80,17±4,10 |
92,09±2,63 |
Maa: Massa de amônia anidra, em R1; Map: Massa de amônia anidra + massa de amônia aquuosa retida em reator 2; Mar: Massa de amônia arrastada e recuperada em solução H2SO4 1mol..L-1; *: massa de (15NH4)2SO4 marcado em 3,5% em at de 15N.
Não houve variação no rendimento da produção da aquamônia quando se empregou diferentes massa de (NH4)2SO4 e não ocorreu diluição isótópica durante o processo de produção de aquamônia.
Portanto, o método apresenta viabilidade para produção de aquamônia enriquecida no isótopo 15N, que poderá ser utilizada na síntese de aminoácidos enriquecidos, ou utilizado em estudos agrônomicos.
[FAPESP]
BENDASSOLI, J.A; et al. Síntese de fertilizantes nitrogenados em 15N – Parte 3. Produção de amônia anidra enriquecida em 15N. Energia Nuclear da Agricultura, Piracicaba, V-9, n.2 p.66-93, 1988.