 (1)
(1)IDENTIFICAÇÃO DE NOVAS SÉRIES DE ALTA MASSA MOLECULAR DERIVADAS DO FITOL E DO a-TOCOFEROL
Denilson Soares de Siqueira (PG)1, Alberto dos Santos Pereira (IC)1, Vladimir Oliveira Elias (PG)2, Bernd R. T. Simoneit (PQ)3, José A. Cabral (PQ)4, Carlos Alberto Cid Ferreira (PQ)4, Francisco Radler de Aquino Neto (PQ) 1
1LADETEC - Instituto de Química – Departamento de Química Orgânica – UFRJ,
palavras-chave: fitol, tocoferol, alta massa molecular, CGAR-AT-EM
A formação e a composição dos compostos graxos de alta massa molecular nas plantas superiores depende, de certa forma, das condições ambientais tais como solo, água e luminosidade1. Os compostos graxos são importantes para o controle de água e o balanço de gases entre as plantas e o meio ambiente. Outras possibilidades funcionais podem estar relacionadas a proteção da epiderme celular contra impactos, desenvolvimento de fungos e ataques de insetos2
Nas últimas três décadas, alguns compostos de alta massa molecular tem sido identificados; por exemplo, compostos de diferentes classes e em diferentes matrizes, tais como, alquil éter de colesterol em músculos cardíacos bovino3 e cetonas de cadeia longa em sedimentos de diatomáceas4. Mais recentemente, com o avanço da Cromatografia Gasosa de Alta Resolução e Alta Temperatura e seu acoplamento a Espectrometria de Massas (CGAR-AT e CGAR-AT-EM), esses compostos passaram a ser caracterizados e identificados em maior número e em novas matrizes, tais como ésteres graxos de cadeia longa ( palmitatos e oleatos) de extrato bruto de própolis e alcanoatos triterpênicos em fumaça de queima de biomassa5.
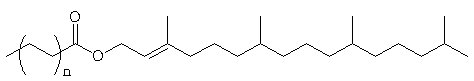
Neste trabalho, identificamos duas novas séries de compostos de alta massa molecular em extrato hexânico de folha de marupá (Simaruba amara); uma série de ésteres de fitol (1) com o número de carbono variando linearmente de C32 a C45 e uma série de ésteres do a-tocoferol (2) vaiando o número de carbono da série linearmente de C39 a C49.
 (1)
(1)
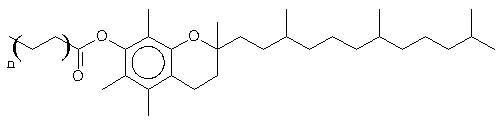 (2)
(2)
Inicialmente, estes compostos foram caracterizados por análise em CGAR-AT-EM do extrato hexânico do marupá. A identificação dos mesmos se fez através da síntese de um membro de cada série e sua respectiva análise por CGAR-AT-EM, RMN de 1H(200MHz) e 13C(50MHz) e IV-FT. Da série do fitol, foi sintetizado o palmitato de fitila e da série do tocoferol foi sintetizado o palmitato de tocoferila.
O palmitato de fitila foi obtido através da reação de esterificação do cloreto de palmitoíla com o fitol, na presença de trietilamina, usando hexano como solvente e refluxo a 80°C por 2 horas. O palmitato de fitila foi isolado do meio reacional através de cromatografia em camada delgada (CCD). O palmitato de tocoferila foi obtido através da esterificação do a-tocoferol com o cloreto de palmitoíla usando hexano como solvente e refluxo a 80°C por 2 horas. O éster obtido foi isolado por CCD.
As análises de CGAR-AT foram realizadas em uma coluna de borossilicato, de 20 metros de comprimento e 0,2 mm de diâmetro interno, recoberta com a fase PS-086 (15% fenil – 85% metilpolissiloxana) com 0,2 mm de espessura de filme de fase estacionária. Utilizou-se um cromatógrafo HP-5890-II, com detector por ionização em chama (FID) e injetor tipo na coluna a frio “cold on column” a 400 °C e temperatura ambiente, respectivamente. As seguintes condições de análise foram aplicadas: temperatura inicial 40 °C, taxa de aquecimento de 10°C/min, temperatura final 390 °C, velocidade linear do gás carreador (H2) 50 cm/s e volume de injeção 0,5 ml.
As análises de CGAR-AT acoplada a espectrometria de massas foram realizadas em HP-5972-MSD acoplado a um cromatógrafo HP-5890-II, com temperaturas de interface e da fonte 370 °C e 300 °C respectivamente utilizando-se uma faixa de varredura de 50 a 700 daltons e a 70 eV (modo impacto de elétrons). Foram utilizadas as mesmas condições cromatográficas embora com hélio como gás carreador.
1-Biachi, A.; Biachi, G.; Avato, P.; Salamini, F.; Maydica, 1985, 30, 179.
2-Tava, A.; Cunico, C.; Cremona, R.; Piccinini, E.; J. High Resoln. Chromatogr., 1996, 19, 43.
3-Boon, J.J.; Leeuw, J.W.; Marine Chem., 1979, 7, 117.
4-Elias, V.O.; Simoneit, B.R.T.; Pereira, A.S.; Cardoso, J.N.; J. Mass Spectr., 1997, 32, 1356.
5-Pereira, A.S.; Ramos, M.F.S.; Poças, E.S.C.; Dias, P.C.M.; Santos, E.P.; Silva, J.F.M.; Cardoso, J.N.; Aquino Neto, F.R.; Z. Naturforch., 1997, 54c, 395.
(CNPq, UFRJ/SR-2, FAPERJ, FUJB, FINEP)