ESTUDO DOS PROCESSOS DE REDUÇÃO DE ÓXIDOS DE FERRO. EFEITO DO VANÁDIO
Grupo de Estudos em Cinética e Catálise, Universidade Federal da Bahia
Palavras-chave: redução de óxidos de ferro, vanádio, reação de HTS
O interesse pelo estudo das propriedades dos óxidos de ferro está relacionado à sua importância nas mais diversas aplicações, tais como tratamento de água e efluentes, prevenção nos processos de corrosão, resinas de troca iônica e tratamento e conservação de solos1. Esses compostos também são importantes como catalisadores, sendo empregados comercialmente em uma grande variedade de reações, podendo-se citar a desidrogenação do etilbenzeno a estireno e amoxidação do propeno a acrilonitrila, a síntese de amônia, a conversão de monóxido a dióxido de carbono a altas temperaturas, a reação de Fischer-Tropsch e a desidrogenação oxidativa do etilbenzeno2. A maioria dessas aplicações relaciona-se à facilidade do ferro em variar o seu estado de oxidação e, dessa forma, a redução dos seus óxidos torna-se um importante campo de estudo.
Uma das técnicas mais convenientes para o estudo dos processos de redução de metais é a redução termoprogramada (TPR)3. Entretanto, devido à influência das propriedades texturais dos sólidos sobre o perfil das curvas, a atribuição dos picos torna-se muitas vezes complicada, exigindo um estudo mais detalhado. Neste trabalho, foram estudados os processos de redução de óxidos de ferro puro e contendo vanádio, usando TPR como técnica básica.
As amostras foram preparadas por precipitação dos sais precursores à temperatura ambiente, seguida de lavagem com solução 5% de acetato de amônio, e secagem, obtendo-se hidroxoacetatos de ferro III (HAF) contendo ou não vanádio. A calcinação a 400oC, sob fluxo de nitrogênio, produziu óxidos de ferro, na forma de magnetita pura (Amostra M) e contendo vanádio nas razões molares Fe/V= 10 e 30 Amostras V1 e V3)4. Os sólidos foram submetidos à redução termogramada, estabelecendo-se, a partir dos termogramas, as temperaturas das principais etapas de redução. Foram,então, conduzidos experimentos isotérmicos, nessas temperaturas, reproduzindo-se as condições usadas no TPR, ou seja, os materiais foram aquecidos sob fluxo de uma mistura 5% H2/N2 a uma velocidade de aquecimento de 10 graus/min. As amostras foram caracterizadas por análise química (Fe (III), Fe(II)), difração de raios-X e medidas de área superficial e de porosidade.

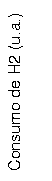
A partir desses resultados, pode-se concluir que o aquecimento de amostras de magnetita (obtida por decomposição térmica de HAF), sob fluxo de uma mistura redutora, produz ferro metálico a temperaturas superiores a 600oC , via a formação de wustita. A presença do vanádio dificulta o processo, mas não altera a natureza das fases formadas. (PADCT/CNPQ, FINEP)
1 Kavanagh, B. V, et al. Journal of Colloid Interface Science, 6, 54 (1977).
2Kung, H. H., Kung, M. C., Advances in Catalysis, 13, 159 (1985).
3 R.J.Farrauto;C.J.Bartolomew.Catalytic Processes. Blackie Academic& Professional. London. 1997.
4 I.L.Júnior, M. C. Rangel, Livro de Resumos da 22a Reunião da Sociedade Brasileira de Química.1999.
5 M.V.Twigg, ; L.Lloyd.; D.E. Ridler. Catalyst Hanbook. Manson Publishing Ltda. London. p. 283 (1996).