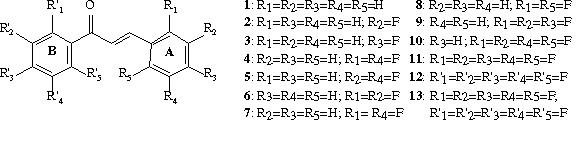
As fotorreações no estado cristalino têm sido estudadas há mais de 100 anos e os trabalhos pioneiros nessa área são devidos a Liebermann, que estudou a dimerização de olefinas.1 Durante a primeira parte do século XX vários pesquisadores iniciaram a sistematização dos resultados da dimerização no estado cristalino a partir dos estudos com derivados do ácido cinâmico. Somente após os anos 60, com o aparecimento de técnicas de difração de raios-X, foi possível a Schmidt e colaboradores avançar no entendimento dos processos de fotodimerização no estado cristalino, estabelecendo importantes regras para estes processos, chamadas de regras topológicas.2 Vários artigos de revisão podem ser encontrados na literatura, os quais apresentam detalhes sobre as várias formas de imperfeições estruturais e sua caracterização por técnicas físicas, bem como acerca da sua importância nas transformações fotoquímicas.3
Uma visão moderna no sentido de um melhor entendimento das fotorreações no estado cristalino está relacionada ao conceito de cavidade reacional proposto por Cohen.4 A cavidade reacional é um conceito qualitativo e representa o espaço ocupado pelo reagente e, neste conceito, os movimentos atômicos que se seguem durante uma reação exercem pressão sobre as paredes da cavidade, a qual torna-se distorcida, sendo assim limitados os movimentos correspondentes aos deslocamentos molecular e conformacional que são permitidos durante a reação.4
Objetivo
Esse trabalho tem como objetivo verificar a influência produzida pela substituição dos átomos de hidrogênio aromático de chalconas por átomos de flúor, em diferentes posições e quantidade, na sua fotoquímica no estado cristalino.
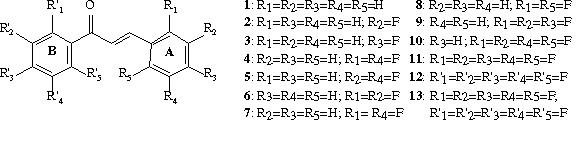
Experimental
Os derivados 1-13 foram obtidos a partir da condensação aldólica, em meio básico, entre acetofenona e os respectivos benzaldeídos e foram recristalizados sucessivas vezes em EtOH/H2O. Os cristais, submetidos a irradiação na faixa do ultra violeta (l=300nm), foram obtidos por evaporação a partir de uma solução em CH2Cl2 em atmosfera de argônio. Após irradiação os produtos foram dissolvidos em CDCl3 e analisados por RMN 1H e 13C.
Resultados
|
Dímeros |
hh-anti(dc) |
ht-sin(dc) |
hh-sin(dc) |
ht-anti(dc) |
|
||||
|
1 |
47,58 |
47,86 |
42,37 |
50,59 |
44,70 |
49,07 |
- |
- |
|
|
2 |
47,09 |
47,37 |
42,00 |
50,25 |
44,40 |
48,71 |
|
- |
|
3 |
47,40 |
47,64 |
41,45 |
51,00 |
44,00 |
49,00 |
- |
- |
|
|
4 |
- |
|
41,25 |
50,42 |
- |
- |
- |
|
|
|
5 |
- |
|
41,95 |
50,02- |
- |
- |
- |
|
|
|
6 |
|
|
|
|
|
|
34,60 |
48,60 |
|
7 |
|
|
|
|
39,26 |
47,37 |
- |
|
|
|
8 |
- |
- |
- |
- |
- |
|
35,1 |
47,69 |
|
9 |
- |
- |
- |
- |
- |
|
34,2 |
48,47 |
|
Dímeros |
hh-anti(dH) |
ht-sin(dH) |
hh-sin(dH) |
ht-anti(dH) |
|||||
|
1 |
3,92 |
4,6 |
4,8 |
4,8 |
4,46 |
4,72 |
- |
- |
|
|
2 |
3,88 |
4,50 |
4,74 |
4,83 |
4,42 |
4,68 |
- |
- |
|
3 |
3,84 |
4,53 |
4,78 |
4,88 |
4,37 |
4,70 |
- |
- |
|
|
4 |
- |
- |
4,74 |
4,82 |
- |
- |
- |
- |
|
|
5 |
- |
- |
4,77 |
4,81 |
- |
- |
- |
- |
|
|
6 |
- |
- |
- |
- |
- |
- |
4,87 |
5,22 |
|
7 |
|
|
|
|
4,70 |
4,85 |
- |
- |
|
|
8 |
- |
- |
- |
- |
- |
- |
4,85 |
5,33 |
|
9 |
- |
- |
- |
- |
- |
|
4,82 |
5,14 |
|
Conclusão
Verificou-se que a fotorreatividade de chalconas no estado cristalino é dependente tanto da posição quanto do número de átomos de flúor presentes no anel A. Como resultado da irradiação das chalconas 1-14, observou-se a formação dos dímeros hh-anti para os derivados 1-3 e 12, ht-anti para os derivados 4 e 5, e ht-sin para 6-9. Os demais compostos, isto é 10, 11 e 13, apresentaram-se fotoestáveis nas condições experimentais descritas acima.
Referências Bibliográficas
1 C. Libermann, Chem. Ber. 1889, 22, 124.
2 M. D. Cohen, G. M. J. Schmidt e F. I. Sonntag, J. Chem. Soc. 1964, 2014.
3 a) V. Ramamurthy, K. Venkatesan, Chem. Rev. 1987, 87, 433 b) V. Ramamurthy; K. Venkatesan, Photochemistry in Organized and Constrained Media , Ed. V. Ramamurthy, VCH Publishers,1991, NY.
4 M. D. Cohen, Angew Chem. Int. Ed . Engl. 1975, 14, 386.
(CNPq, CAPES, FAPERJ)