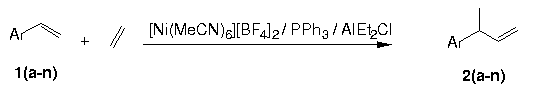
Síntese de 3-aril-1-butenos via hidrovinilação catalítica de olefinas
Viviane Fassina (PG), Carolina Ramminger (IC), Adriano Lisboa Monteiro(PQ)
Instituto de Química – Universidade Federal do Rio Grande do Sul
palavras-chave: hidrovinilação, catálise homogênea, níquel.
A codimerização de olefinas com etileno, também chamada de hidrovinilação de olefinas, pode ocorrer com elevadas quimio- e regiosseletividades e sob condições amenas, quando conduzida na presença metais de transição e ligantes apropriados. No caso da hidrovinilação de derivados do estireno, os produtos desejados são os 3-aril-1-butenos. Essas olefinas são facilmente oxidadas a ácidos 2-arilpropiônicos, que são largamente utilizados como antiinflamatórios não estereoidais, tais como Ibuprofeno, Naproxeno e Ketoprofeno. Além disso, o (R)-3-fenil-1-buteno pode ser usado como monômero para homopolimerização ou copolimerização de olefinas, fornecendo polímeros com alta regularidade e boas propriedades físicas e mecânicas. Em trabalhos anteriores, nós aplicamos o sistema catalítico [Ni(MeCN)6][BF4]2 / AlEt2Cl / PPh3 para a reação de hidrovinilação de ariletilenos1. Nas condições estudadas somente o estireno e alquilestirenos conduziram a um sistema ativo e seletivo. No presente trabalho procurou-se estudar a reação de hidrovinilação catalítica de diversos substratos ariletilenos, visando encontrar as condições reacionais mais adequadas para a obtenção quimio- e regiosseletiva de produtos 3-aril-1-buteno, independente dos grupos ligados ao anel aromático.
Os testes catalíticos foram realizados sob condições amenas. Todas as reações foram realizadas em atmosfera inerte, empregando-se a técnica do tubo Schlenk. Utilizou-se um reator de aço inox com volume interno de 100 mL, que permitiu alimentação contínua de etileno, agitação magnética e controle de temperatura. A determinação quantitativa dos produtos obtidos nos testes catalíticos foi feita por cromatografia em fase gasosa e para sua caracterização empregou-se espectroscopia no infravermelho, espectroscopia de ressonância magnética nuclear de próton e carbono-13 e espectrometria de massas.
Foram testados treze diferentes compostos como substratos para hidrovinilação catalítica seletiva (equação 1). A tabela 1 mostra os resultados obtidos a partir da otimização dos parâmetros reacionais para cada substrato estudado.
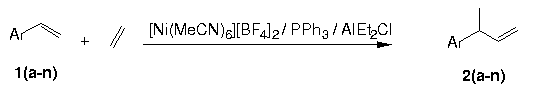
0,05 mmol [Ni], [P]/[Ni] = 4, 20 mL CH2Cl2, 10 bar etileno, T ambiente
Tabela 1 – Otimização de condições reacionais na hidrovinilação de substratos ariletilenos
|
Substrato |
T (min) |
[Al]/ [Ni] |
[subst.]/ [Ni] |
Conv. (%)a |
Seletiv.(%)b |
Rend (%)a |
|
|
1a |
Estireno |
50 |
5 |
400 |
100 |
98 |
98 |
|
1b |
4-metilestireno |
60 |
5 |
400 |
98 |
86 |
84 |
|
1c |
4-isobutilestireno |
30 |
10 |
200 |
100 |
95 |
94 |
|
1d |
2-vinilnaftaleno |
40 |
10 |
100 |
97 |
96 |
93 |
|
1i |
3-benzoilestireno |
60 |
38 |
100 |
100 |
>99 |
99 |
|
1f |
4-benzoilestireno |
60 |
38 |
100 |
100 |
88 |
88 |
|
1g |
3-cloroestireno |
60 |
7 |
400 |
95 |
98 |
93 |
|
1h |
2-cloroestireno |
60 |
6 |
300 |
93 |
95 |
88 |
|
1i |
4-metoxiestireno |
60 |
10 |
350 |
100 |
95 |
95 |
|
1j |
a-metilestireno |
60 |
15 |
200 |
100 |
68 |
68 |
|
1l |
Vinilferroceno |
45 |
5 |
100 |
100 |
>99 |
99 |
|
1m |
Indeno |
60 |
5 |
200 |
65 |
57 |
37 |
|
1n |
2-metoxi-6-vinilnaftaleno |
40 |
20 |
100 |
97 |
99 |
96 |
a – determinado por CG, b – em relação a 3-aril-1-buteno
Observa-se que pequenas variações nas condições reacionais empregadas possibilitaram que altas conversões e rendimentos fossem alcançados independente do caracter eletrônico do substituinte associado ao anel aromático. Quando o substrato apresentava características básicas, a ordem de adição dos reatantes é determinante na reatividade do sistema, uma vez que o cocatalisador alquilalumínio pode ser consumido pelo substrato, antes da formação de espécie cataliticamente ativa. Este sistema permite a hidrovinilação de olefinas com substituintes nos carbonos vinílicos (1j e 1m) com boa atividade e seletividade, contrariamente aos demais sistemas descritos na literatura que são inativos para este substratos2. Em suma, este sistema catalítico é extremamente versátil, ativo, seletivo e regiosseletivo. Os produtos 2c e 2i foram oxidados com KMnO4/ NaIO4/ K2CO3 conduzindo aos fármacos Ibuprofeno (71%), e Cetoprofeno (65%).
Referências:
1 - A. L. Monteiro, M. Seferin, R. F. de Souza e J. Dupont, Tetrahedron Lett.1996, 37, 1157.
2. T. V. RajanBaju in “Comprehensive Asymetric Catalysis”, Eric N. Jacobsen, Andreas Pfaltz , Hisashi Yamamoto, 1999, 417 – 427.
CAPES, CNPq, PADCT, FAPERGS