ESTUDO DE QSAR DE COMPOSTOS DERIVADOS DA ARTEMISININA COM ATIVIDADE ANTIMALÁRICA
Melissa Tatiana de Oliveira (IC),a Clodoaldo Machado (PQ)a e
Carlos Alberto Montanari (PQ)b
a Departamento de Química – FURB - Blumenau - SC - CEP 89010971
b Departamento de Química – UFMG – Belo Horizonte - MG - CEP 31270901
palavras-chave: QSAR, malária, artemisinina
A malária tem se apresentado como uma das doenças infecciosas mais comuns e severas dos países tropicais. Segundo dados da Organização Mundial de Saúde, ocorrem 280 milhões de casos de malária a cada ano, causando aproximadamente 2 milhões de mortes. A malária é causada por protozoários do gênero Plasmodium. O alto índice de mortalidade em pacientes contaminados com malária detectados atualmente (entre 20 e 50%), deve-se principalmente ao poder de adaptação do agente causador da enfermidade e a conseqüente perda da eficácia das drogas antimaláricas comumente utilizadas nas últimas décadas, como aquelas derivadas da quinolina [1].
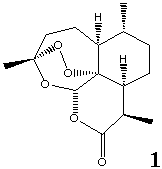
Uma nova classe de compostos antimaláricos, caracterizada pela presença da unidade farmacofórica 1,2,4-trioxano, tem sido investigada desde 1972, quando a artemisinina (1), principal constituinte do extrato da planta Artemisia annua (qinghao), foi isolada e identificada [2]. O modo de ação desta droga compreende a clivagem da ponte endoperóxida mediada pelo ferro, gerando assim radicais e espécies eletrofílicas que podem destruir o parasita por alquilação ou oxidação de biomoléculas, interrompendo o processo bioquímico vital.
Objetivos
A utilização da artemisinina e alguns de seus derivados no combate a malária em países asiáticos e africanos tem comprovado a eficiência desta nova droga [3,4]. Em particular, este trabalho investiga as correlações estrutura-atividade (QSAR) para uma série de compostos derivados da artemisinina (2Aa-2Jb) [5].

|
Molécula |
R |
IC50 (nM)a |
|
2A(b |
Ph |
110 |
|
2A( |
Ph |
38 |
|
2B( |
p-PhPh |
76 |
|
2B( |
p-PhPh |
68 |
|
2C( |
1- naphthyl |
170 |
|
2C( |
1- naphthyl |
44 |
|
2D( |
p-ClPh |
49 |
|
2D( |
p-ClPh |
55 |
|
|
p- MeOPh |
> 2500 |
|
2F( |
2-furyl |
600 |
|
2G( |
p-HOCH2Ph |
78 |
|
2G( |
p-HOCH2Ph |
15 |
|
2H( |
p-MeOCH2Ph |
39 |
|
2H( |
p-MeOCH2Ph |
51 |
|
2I( |
p-MeC(O)OCH2Ph |
44 |
|
2I( |
p-MeC(O)OCH2Ph |
20 |
|
2J( |
p-FPh |
65 |
|
2J( |
p-FPh |
30 |
a Ref. 5. bA simbologia ( corresponde ao grupo OMe a favor, e ( oposta, ao grupamento peróxido, respectivamente.
Resultados e Discussão
As duas primeiras componentes principais descreveram 84,5% da variância total. Houve uma separação dos compostos através, principalmente, da PC2. O composto mais potente de toda a série (2G() tem maiores valores negativos em PC1 e PC2 do que todos os demais. O composto (2E), o menos potente, entretanto, está presente no mesmo quadrante. Os principais descritores físico-químicos estão localizados em PC2. O composto mais potente (2G() tem, em seu índice de similaridade Carbo o principal requisito necessário para descrevê-lo como tal: sua similaridade combinada entre a forma e a carga. Isso significa que todos os demais compostos precisam ter similaridade próxima para que sejam ativos. O segundo parâmetro importante em PC2 é o lipofílico. O coeficiente de partição parecer ter um papel importante no que diz respeito ao transporte dessas drogas até o sítio ativo. Entretanto, os log Ps calculados para os compostos 2G( e 2E são, respectivamente, 3,8 e 4,1. Dessa forma, parece lícito observar que a presença dos dois compostos na mesma família estabelece que esse parâmetro é importante para que os compostos apresentem suas respectivas potências indistintamente. O índice de similaridade combinada para o composto 2E é 0,98 em relação ao 2G(. Da mesma forma, está implícito que a similaridade desses compostos não traduz suas diferenças em potências.
Conclusão
Preliminarmente, pode-se inferir a partir dos resultados obtidos neste trabalho que a classificação dos compostos de acordo com certas características físico-química imprime uma racionalização. A importância do parâmetro lipofilicidade aqui determinada, está de acordo com resultados recentes de QSAR empregando outros derivados da artemisinina [6]. A partir desses resultados, novos compostos serão planejados e sintetizados.
Bibliografia
[1] Ezedinachi, E. N. U.; Ejezie, G. C.; Meremikwu, M. Central African J. Med. 1996, 42, 109-111.
[2] Dhingra, V.; Rao, K. V.; Narasu, M. L. Biochemical Education 1999, 27, 105-109.
[3] Price, R. et al. Am. J. Med. Hyg., 1999, 60(4), 547-555.
[4] Meshnick, S. R.; Taylor, T. E.; Kamchonwonpaisan, S. Microbiol. Rev. 1996, 60, 301-315.
[5] Posner, G. H. et al. J. Med. Chem. 1998, 41, 940-951.
[6] Tang, Y; Jiang, H. L.; Chen, K. X.; Ji, R. Y. Indian J. Chem. 1996, 35B, 325-332.
(PIPe/FURB, UFMG)