INFLUÊNCIA DO SOLVENTE SOBRE OS ESPECTROS DE FLUORESCÊNCIA DE CORANTES SOLVATOCRÔMICOS
Viviane Cavalli (PG)a, Clodoaldo Machado (PQ)b e Valdir Soldi (PQ)c
a Mestrado Interinstitucional em Química - FURB/UFSC
b Departamento de Química – FURB - Blumenau - SC - CEP 89010971
c Departamento de Química – UFSC – Florianópolis – SC - CEP 88040900
palavras-chave: fluorescência, solvatocromismo, influência do solvente
As propriedades espectroscópicas dos compostos que possuem em sua estrutura um grupo doador de elétrons unido a um grupo receptor por meio de um sistema conjugado têm sido extensivamente estudadas nos últimos anos.1 Em particular, os espectros de absorção eletrônica (UV/Vis) da maioria destes compostos são extremamente sensíveis a mudança na polaridade do solvente, sendo então denominados de corantes solvatocrômicos.2 Apesar dos estudos com corantes solvatocrômicos serem bastante comuns na literatura, estes baseiam-se quase que exclusivamente na técnica de absorção eletrônica (UV/Vis), sendo os trabalhos de fluorescência ainda muito escassos.
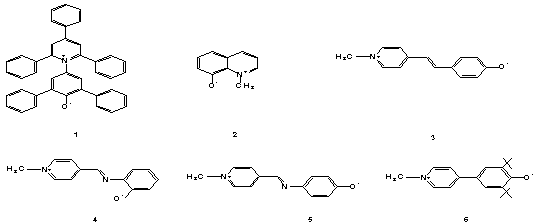
Neste trabalho estudou-se o efeito do solvente e de soluções salinas sobre o comportamento dos corantes 1 - 6 quanto a fluorescência. Os resultados foram correlacionados com dados de absorção eletrônica (UV/Vis) da literatura.







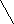
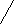
Métodos
As soluções foram preparadas pela dissolução dos corantes nos diferentes solventes a partir de uma solução estoque em etanol. As medidas espectrais de fluorescência foram realizadas a temperatura de 25,0 ± 0,1°C em um Espectro-fluorímetro HITACHI, modelo F-4500, com cubeta de quartzo de 1cm, [corante]final @ 1,7x10-5 mol.dm-3 e lexc = 485 nm.
Resultados
Todos
os compostos estudados apresentaram fluorescência. Para os
compostos 1, 2, 4 e 5, não foram
observadas variações significativas nos
comprimentos de onda máximos de emissão em função
da polaridade do solvente (lmáx
= 562 ± 3 nm). Já os
espectros dos corantes 3 e 6 mostraram-se mais
sensíveis a mudança de solvente. Entretanto, para o
corante 6, os valores observados não seguiram uma
tendência de polaridade do solvente, como observado para o
corante 3.
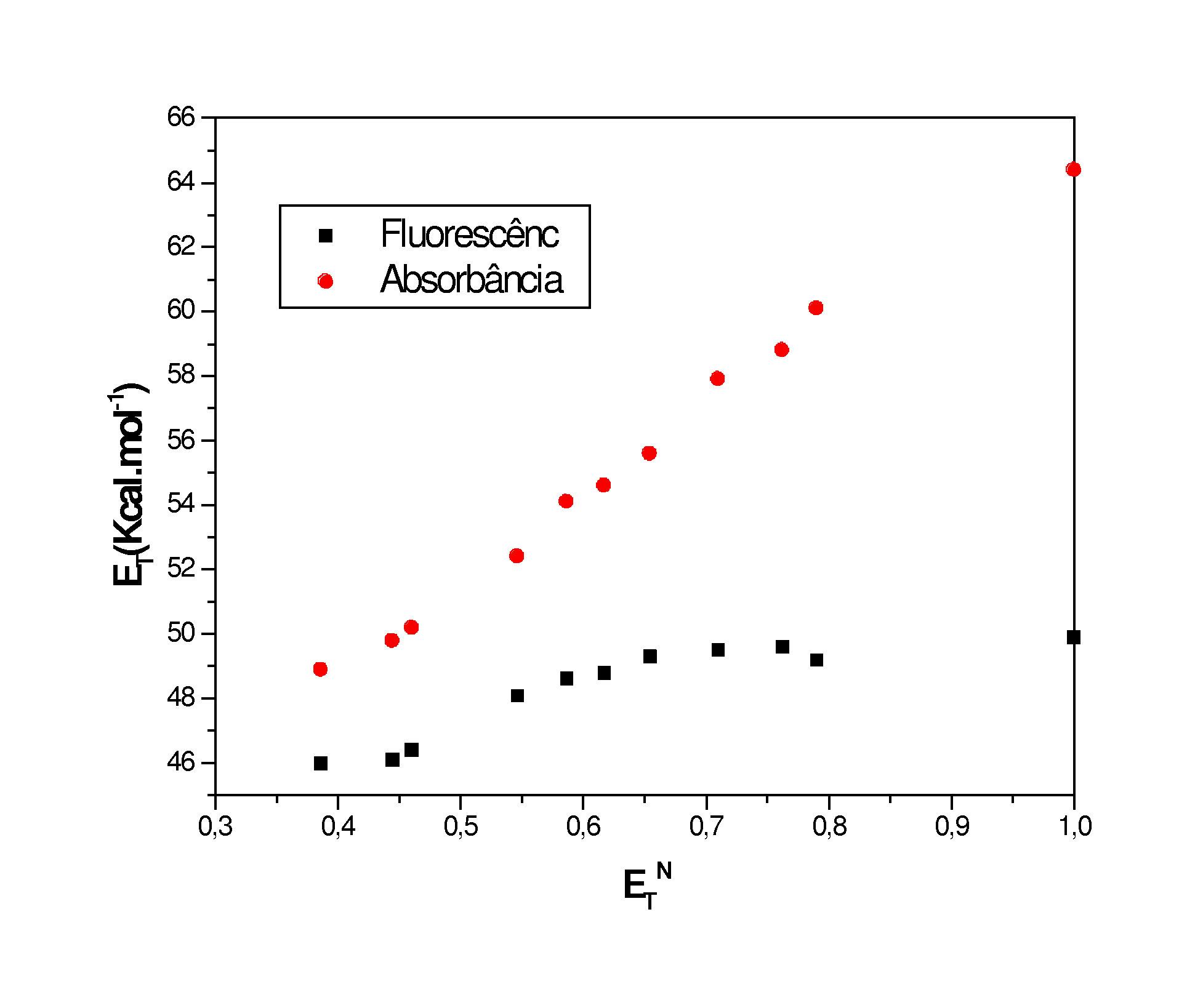
Figura 1 Figura 2
A Figura 1 apresenta os valores das energias de transição eletrônica (ET) calculadas a partir dos máximos de absorção e emissão (ET= 28590/lmáx.) para o corante 3 em função da polaridade (ETN) dos solventes empregados. Observa-se que o efeito do solvente é menor na fluorescência que na absorção eletrônica.
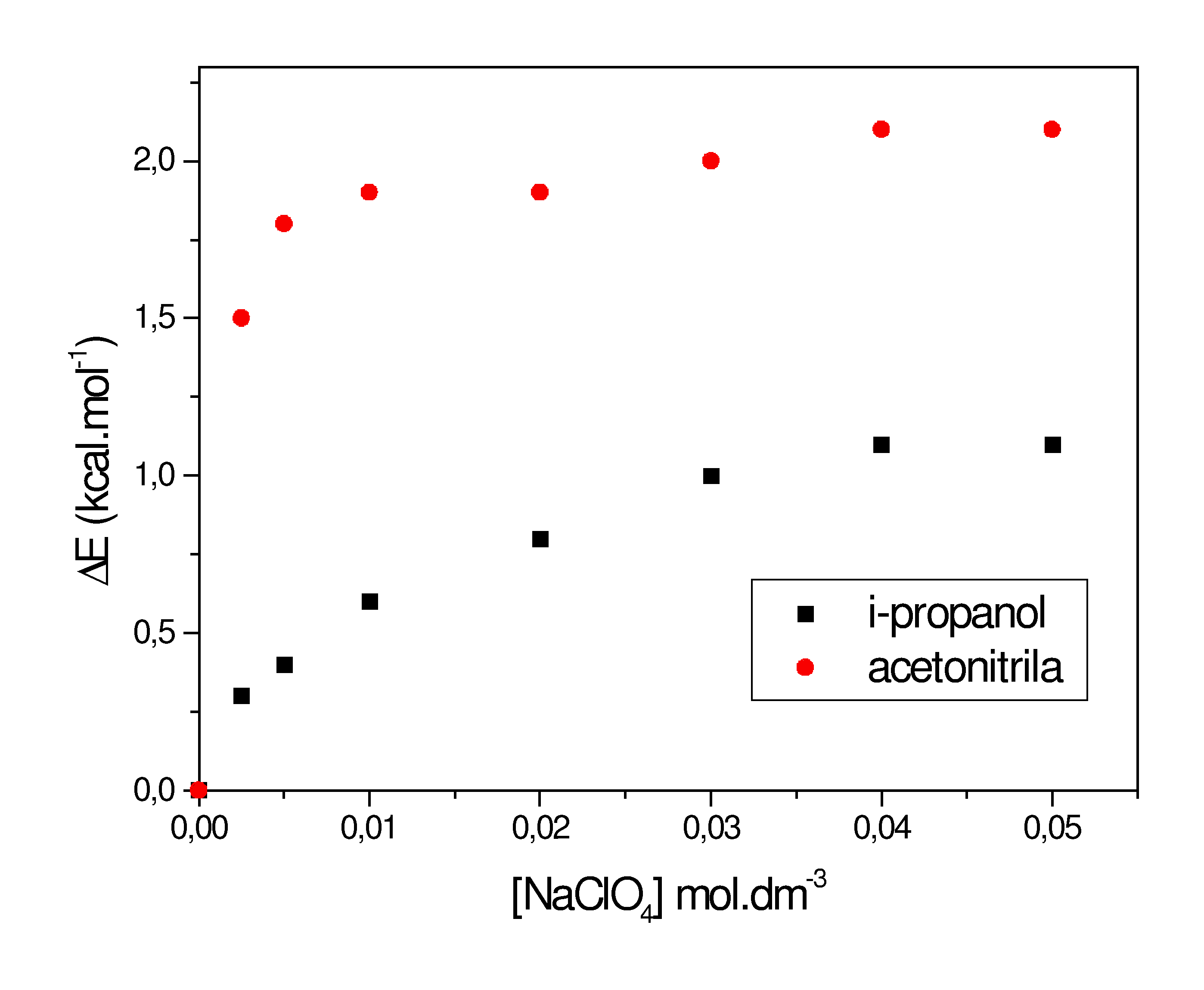
O espectro de emissão de fluorescência do corante 3 também foi registrado para soluções com concentrações crescentes de eletrólitos. A Figura 2 apresenta a variação de energia para a transição eletrônica na presença e ausência de sal (DE) em função da concentração de NaClO4. O comportamento observado em i-propanol e acetonitrila é similar aos valores obtidos com outros pares solvente/sal empregados. Quando o sal é adicionado ao meio, constituído do solvente e do corante, a associação entre o cátion solvatado e a unidade fenólica do composto 3 é quem determina as mudanças halocrômicas em solução e consequentemente as variações nos espectros de fluorescência.
Conclusões
Como todos os corantes investigados apresentaram fluorescência, pode-se concluir que as características estruturais que caracterizam os compostos solvatocrômicos, faz com que estes sejam também fluorescentes. O corante 3 mostrou-se bastante sensível a mudanças do meio, indicando o possível uso deste como uma sonda fluorescente para a detecção de mudanças na polaridade do meio.
Bibliografia
Machado, V. G.; Machado, C.; Nascimento, M. G.; Rezende, M. C. Química Nova
1996, 19, 523-528.
Machado, C.; Zanotto, S. P.; Scremin, M.; Rezende, M. C. J. Phys. Org. Chem.
1993, 6, 637-641.
FUNCITEC, CAPES, UFSC, FURB