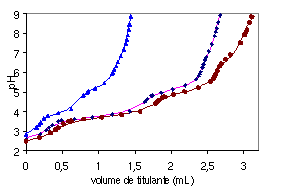
Fig. 1. Titulações potenciométricas.
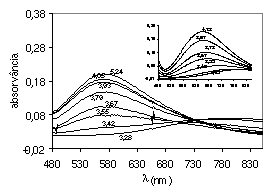
Fig. 2. Espectros no visível.
COMPLEXOS HETERONUCLEARES DE COBRE(II) E
CHUMBO(II) COM ÁCIDO GLICINOIDROXÂMICO
Augusto F. Oliveira (IC)1, Helena Duani (IC)1,
Hélio A. Duarte (PQ)1, Sandra Carvalho (PQ)1 e Eucler B. Paniago (PQ)2
1-Departamento de Química - Inst. Ciências Exatas - UFMG
2-Departamento de Química - Inst. Ciências Exatas e Biológicas - UFOP
palavras-chave: heteronuclear; aminoidroxâmico; cobre(II)
Em meio aquoso, sistemas contendo mais de um íon metálico, na presença de um ligante que possua mais de um sítio de coordenação, podem formar espécies heterobinucleares. Dependendo das condições, a formação dessas espécies bimetálicas pode ser favorecida em relação às espécies binárias também presentes no meio.
Um desses ligantes é o ácido glicinoidroxâmico (Gha=HL), o qual possui um grupo amínico –NH2 e um grupo hidroxâmico –CONHOH, podendo coordenar íons metálicos através dos dois átomos de nitrogênio ou dos dois oxigênios do grupo hidroxamato, isolada ou simultaneamente. A capacidade desse ligante de coordenar-se simultaneamente a dois íons metálicos está bem estabelecida [1]. Por exemplo, já que o íon Cu(II) prefere coordenar-se aos dois nitrogênios e Fe(III) e Al(III) preferem a coordenação O,O, o ânion glicinoidroxamato pode coordenar-se simultaneamente a Cu(II) e a Fe(III) ou Al(III), formando compostos bimetálicos [2]. Pela mesma razão, parece razoável supor que Gha, na presença dos íons Cu(II) e Pb(II), possa formar um composto análogo.
Neste trabalho (desenvolvido como um dos requisitos da disciplina Equilíbrio Químico em Bioinorgânica), temos como objetivo estudar a possível formação de espécies heterobinucleares no equilíbrio químico, em meio aquoso, envolvendo Cu(II), Pb(II) e Gha. Foram realizadas titulações potenciométricas de soluções com os três reagentes, em atmosfera inerte, em diferentes proporções metais/ligante, sempre com força iônica igual a 0,1 mol/L e temperatura de 25 OC. As curvas de titulação experimentais e calculadas (linha contínua) são mostradas na Fig. 1. Foram feitas também medidas de espectrofotometria de absorção molecular na região do visível, em diferentes valores de pH (Fig. 2).
|
|
|
|
Fig. 1. Titulações potenciométricas. |
Fig. 2. Espectros no visível. |
Os dados potenciométricos foram tratados com o programa SUPERQUAD, para ajustar os valores de logb das espécies heterobinucleares. Nesse tratamento, quatro modelos químicos diferentes foram testados, sempre incluindo todas as espécies binárias de Cu(II) e Pb(II) com Gha e também as constantes de hidrólise dos dois íons metálicos. A diferença entre os diferentes modelos se dá apenas com relação aos complexos binucleares. O melhor ajuste foi obtido supondo-se a forma-ção das espécies Cu2Pb(L)2(OH)2 (logb=20,20(8)) e CuPb(L)2(OH)2 (logb=14,04(8)).
A Figura 2 mostra espectros no visível de uma solução contendo uma mistura dos íons Cu(II) e Pb(II) na presença de Gha. Nessa figura, foi inserida uma série de espectros de soluções contendo apenas Cu(II) e Gha. Fica evidente que a adição de Pb(II) acarreta uma mudança no espectro do íon Cu(II) para menores comprimentos de onda, o que é uma característica de aumento do número de átomos de N na sua coordenação.
A Figura 3 mostra estruturas possíveis para cada uma das duas espécies bimetálicas, contendo dois átomos de cobre (lado esquerdo) ou apenas um (lado direito). Embora seja impossível, com base nos dados disponíveis, definir-se por uma dessas estruturas, todas têm uma razoável probabilidade de existirem.

Fig. 3. Estruturas propostas para os complexos heterobinucleares.
Kurzak, B.; Kozlowski, H.; Farkas, E., Coord. Chem. Rev , 114:169, 1992.
Fernandes, M. C. M. M. Tese de doutorado. UFMG. 1997.
CNPq/FAPEMIG/FINEP