 m impregnada
m impregnada
Vanessa Lima Gonçalves (PG), Mauro Cesar Marghetti Laranjeira (PQ)
Departamento de química
A quitosana é um biopolímero hidrofílico obtido industrialmente por desacetilação da quitina através de alcális. A hidrofilicidade do polímero é próprio do grupamento amino e é solúvel em soluções de ácido diluído. A quitosana apresenta propriedades favoráveis de biocompatibilidade (atóxica, biodegradável e de origem natural) e bioatividade.
Diclofenaco de sódio,ácido [2(2,6-diclorofenilamino]-benzenoacético monossódico é um antiinflamatório não esteroidal que possui também atividade analgésica e antipirética. É derivado do ácido fenilacético, com valor de pKa 4,0. Como resultado, o diclofenaco de sódio(DS) é praticamente insolúvel em soluções ácidas, porém dissolve em fluídos intestinais e água.
Acredita-se que seus efeitos farmacológicos decorrem da sua capacidade de inibir a cicloxigenase, impedindo a formação de prostaglandinas. Os efeitos gastrointestinais são comumente vistos. O tempo de meia vida curto do diclofenaco de sódio associado aos seus efeitos colaterais requer um sistema de liberação controlada como sistema alternativo de formulação para este fármaco. Este trabalho tem como objetivo estudar a liberação controlada in vitro do diclofenaco de sódio após sua impregnação em microesferas de quitosana reticuladas com glutaraldeído.
A preparação da quitosana foi realizada em meio anidro fortemente alcalino, conforme o método de Broussignac. As microesferas foram preparadas segundo o método de separação de fases via coacervação simples.
À solução de quitosana 4% em ácido acético 5% foi adicionado pó de alumínio com a finalidade de formação de poros. Esta solução foi gotejada em um banho de precipitação contendo solução de NaOH 2mol/ L, ocorrendo a formação das microesferas artificialmente porosas devido ao desprendimento de hidrogênio. As microesferas permaneceram 20 minutos em solução de EDTA o,o1mol/ L para a complexação do possível alumínio residual. A reticulação das microesferas foi realizada em solução de glutaraldeído 2,5% (v/v) onde permaneceram por 24 horas, com a finalidade de aumentar a resistência mecânica e química.
A impregnação das microesferas reticuladas com glutaraldeído (MRG) foi feita em solução de diclofenaco de sódio– em metanol-água, durante 24 horas de agitação constante. Para determinar a massa de DS impregnada foi destruído 1g de microesferas úmidas e mantido sob agitação em metanol. A solução foi filtrada e lida em lmax 280nm. A partir disso, foi calculada a massa de DS impregnada em MRG.
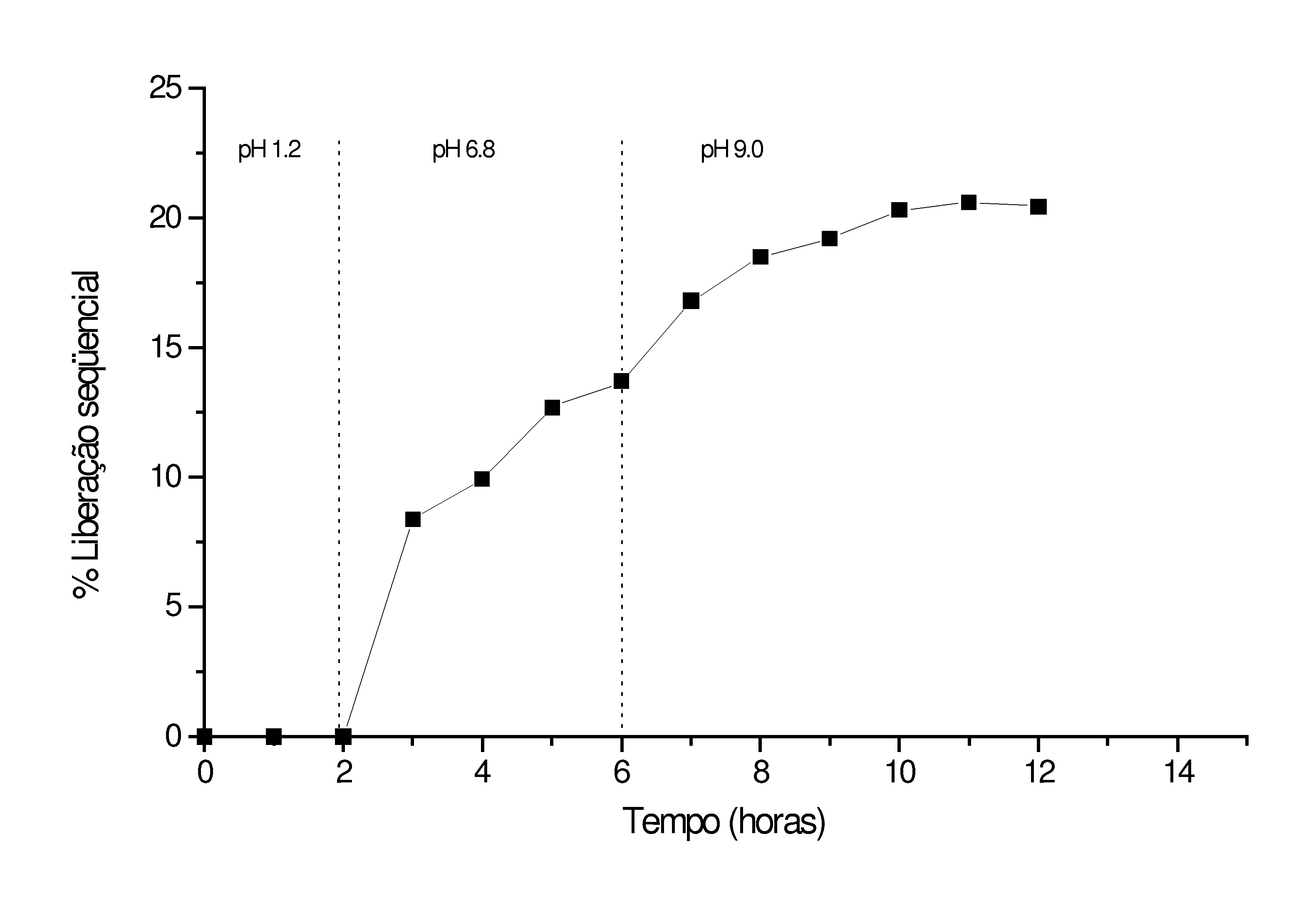
O controle da liberação seqüencial de DS das MRG foi realizado utilizando-se apenas uma batelada de MRG secas, as quais foram transferidas pelos diferentes valores de pH, simulando o trato gastrointestinal, totalizando 12 horas a 37°C com agitação horizontal em 100 rpm. Alíquotas de 1 mL foram retiradas em intervalos de 1 hora. Em seguida foi realizada leitura em curva de calibração para cada pH.
O cálculo da porcentagem liberada de DS em cada pH foi feito a partir da Equação % DS liberada = m liberada x 100 .
 m impregnada
m impregnada
Por ser um processo cumulativo os valores do pH 6,8 deverão ser somados ao último valor do pH 1,2, assim como os valores de pH 9,0 somados ao último valor do pH 6,8. O tamanho médio das microesferas foi analisado através de microscopia eletrônica de varredura.
As
microesferas de quitosana reticuladas com glutaraldeído (MRG)
apresentam pouca esfericidade e tamanho médio 1.295mm.O
resultado obtido da quantidade de massa impregnada de DS nas MRG foi
de 200mg/ g seca. O valor da liberação seqüencial
de DS das MRG obtido após 12 horas foi de 20.5%.
Gráfico 1: Liberação Seqüencial de DS das MRG
Assim, concluímos que a quitosana mostra ser excelente veículo para o processo de liberação do DS, tanto na produção das microesferas como na liberação do DS. O pó de alumínio, utilizado na preparação das microesferas é um artifício eficaz na formação de poros e no conseqüente aumento da impregnação. A menor liberação de DS em pH 1,2 é significativa tendo em vista que o estômago apresenta este pH e é onde ocorre a menor absorção do fármaco, assim como a maior liberação em pH intestinal simulado pois é neste pH que ocorre a maior absorção do DS.
Bibliografia
1.AÇIKGÖZ,M.,H.S.,HASÇELIK,Z.et al. Chitosan microspheres of diclofenac
sodium, II: IN vitro and in vivo evaluation. Pharmazie,v.50,H.4,p.275-277,1995.
2.LIU,C.,KAO,Y.,CHEN,S.et al. In vitro and in-vivo studies of the diclofenac
sodium controlled-release matriz tablets. Journal of Pharmacy and
Pharmacology, v.47, n. 5, p.360-364, may 1995.
3.TOZAKI,H. KOMOIKE,J.,TADA, C. et al. Chitosan Capsules for Colon-Specific Drug Delivery: Improvement of Insulin Absorption from the Rat Colon. Journal of Pharmaceuticals Science, v. 86, n.9, p. 1016-1021, 1997.