ALCOXOMETALATOS CONTENDO TITÂNIO E VANÁDIO: SÍNTESE, CARACTERIZAÇÃO E APLICAÇÕES NA FIXAÇÃO DE N2
Giovana G. Nunes (PG)1, Dayane M. Reis (IC)1, Peter B. Hitchcock (PQ)3, Manfredo Hörner (PQ)2, G. Jeffery Leigh (PQ)3, Fábio S. Nunes (PQ)1 e Jaísa F. Soares (PQ)1
1 Departamento de Química, Universidade Federal do Paraná, Curitiba, PR
2 Departamento de Química, Universidade Federal de Santa Maria, RS
3 School of Chemistry, Physics and Environmental Science, University of Sussex, UK
Palavras-chave: alcoxotitanatos, vanádio(III), fixação de nitrogênio.
A existência da fixação biológica de nitrogênio, ou a conversão enzimática de N2 a amônia por certas bactérias e algas, é conhecida desde o final do século XIX. A eficiência dos sistemas biológicos tem levado muitos pesquisadores à busca de sistemas químicos sintéticos capazes de mimetizar, estrutural ou funcionalmente, os catalizadores naturais da fixação de nitrogênio.
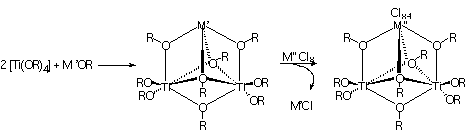
Com o objetivo de sintetizar modelos químicos funcionais da nitrogenase, temos interesse na preparação de agregados trinucleares do tipo [M'Ti2(OR)9] [1], onde M' = Na+ ou K+; R = OPri, que reajam com cloretos de ferro ou vanádio (M''Clx, x = 2 ou 3) produzindo alcóxidos heterobimetálicos do tipo [M''Cl(x-1)Ti2(OR)9], de acordo com a figura abaixo.
Figura 1: Esquema de síntese dos alcóxidos trinucleares.
As sínteses e a preparação das amostras para análises foram realizadas sob atmosfera de N2 (pureza 99,999%), através do uso de técnicas de Schlenk. Os materiais de partida, NaOPri e [Ti(OPri)4], foram preparados por alcoólise do hidreto de sódio e do tetracloreto de titânio, respectivamente.
O composto [Ti(OPri)4] foi colocado para reagir com NaOPri na proporção de 2:1, em tolueno a 70ºC por 5 horas, para obtenção do intermediário [Na{Ti2(OPri)9}]. A seguir adicionou-se uma suspensão de VCl3 em tolueno/isopropanol e deixou-se a mistura reacional em refluxo a 70ºC por 48 horas. Após a purificação foram obtidos cristais incolores com forma de diamantes (produto A), rendimento 49%.
A análise dos teores de Ti e V indicou que o titânio era o único metal de transição presente no produto A. Nesta preparação foram isolados outros produtos cristalinos (verde e azul), ainda não caracterizados completamente, que provavelmente contêm vanádio. A análise por cristalografia de raios X do produto A revelou que a estrutura molecular consiste de centros de TiIV ligados em ponte por dois grupos isopropóxido. A cada átomo metálico estão ligados também dois isopropóxidos terminais, um cloreto e uma molécula de isopropanol, levando à fórmula estrutural [{TiCl(OPri)2(PriOH)}2(m-OPri)2] para o produto A. Nesta reação, o VCl3 aparentemente atuou como doador de cloretos para o alcóxido de titânio.
|
Figura 2: Representação da estrutura molecular de A. Sistema monoclínico, grupo espacial P21/n (no 14), a = 10,8611(4)Å, b = 10,5932(5)Å, c = 15,3648(5)Å, b = 102,826(2)º, Z = 2. V = 1723,67(12)Å3. 10.969 reflexões coletadas, 2982 reflexões independentes, 2714 reflexões observadas (I>2si), 167 parâmetros refinados. R final [I>2si] = 0,041, wR2 = 0,101.
|
O produto A (sólido pulverizado a 77K) mostrou-se silencioso na análise por RPE, resultado coerente com a presença de TiIV (d0). O espectro de absorção na região do infravermelho (FTIR), em nujol, mostrou bandas a 1012 cm-1 {F, n(C-O)} e 933 cm-1{m, n(CO)} referentes aos grupos isopropóxido terminais e em ponte, respectivamente, coerentes com os dados da literatura [2]. O espectro de 1H-RMN do produto (CD3C6D5, 20ºC) apresentou sinais alargados (d = 1,26 e 4,62 ppm) atribuídos, respectivamente, aos hidrogênios metílicos e metínicos dos isopropóxidos. A falta de resolução poderia ser atribuída ao caráter fluxional do grupos -OPri (terminais e em ponte) em solução.
O fato do produto A ser molecular, cristalino e conter ligações longas Ti-Cl = 2,3846(6)Å e Ti-O(H)Pri = 2,1824(18)Å sugere que o composto possa ser utilizado como precursor de espécies de maior nuclearidade, analogamente ao que ocorre com o complexo binuclear de ferro(II) [{FeCl(tmeda)}2(m-Cl2] [3].
A reação utilizando NaOPri como um dos materiais de partida não produziu a espécie trinuclear esperada, provavelmente porque o raio iônico do sódio é muito pequeno para permitir a formação do intermediário [Na{Ti2(OPri)9}] (figura 1). Com o propósito de comprovar esta hipótese, repetimos a preparação com KOPri, o que gerou outro produto cristalino que está sendo caracterizado. Estamos também trabalhando em sínteses envolvendo [Ti(OPri)4] e haletos de FeII e FeIII, com o objetivo de obter produtos que, quando reduzidos na presença de N2, interajam com este substrato e o ativem para a conversão a amônia ou hidrazina.
[1] Mehrotra, R.C.; Singh, A. Polyhedron, 1998, 17, 689.
[2] Malti, B.; Singh, A.; Mehrotra, R.C.; Synth. React. Inorg. Met. Org. Chem., 1998, 28, 997.
[3] Davies, S.C; Hughes, D.L.; Leigh, G.J.; Sanders, J.R.; Soares, J.F., J. Chem. Soc., Dalton Trans., 1997, 1981.
UFPR, FUNPAR, CNPq, CAPES, PRONEX