COMPLEXOS DE VANÁDIO(III/IV) COM ALCÓXIDOS DERIVADOS DE AÇÚCARES
Miriam Christi Midori Oishi (IC), Cristiane Regina Budziak (IC),
Antonio Salvio Mangrich (PQ), Fernando Wypych (PQ),
Fábio Souza Nunes (PQ) e Jaísa Fernandes Soares (PQ)
Laboratório de Química Bioinorgânica, Departamento de Química, Universidade Federal do Paraná, Curitiba, PR
Palavras-chave: vanádio, alcóxido, dulcitol
O interesse na química de complexos de vanádio com ligantes O-doadores tem crescido desde a descoberta da redução catalítica ou estequiométrica de N2 por VII-catecolatos e -hidróxidos [1]. Adicionalmente, alcóxidos de vanádio têm sido vistos como precursores moleculares potenciais de óxidos poli(hetero)metálicos com aplicações em processos sol-gel [2].
Nosso trabalho investiga as reações entre materiais de partida de vanádio(III) e alcóxidos obtidos a partir de alditóis (açúcares reduzidos) e monossacarídeos. Nossos objetivos gerais são a preparação de compostos de coordenação de VIII e/ou VIV com ligantes O-doadores, seguida da redução dos produtos e da análise das condições experimentais que promovam a interação entre os complexos e N2. A escolha de derivados de açúcares como pró-ligantes baseia-se na sua grande variedade estrutural - além da ampla disponibilidade natural - bem como em relatos de que ligantes O-doadores volumosos estabilizam complexos mono- e polinucleares de VII®VIII de interesse para a fixação de N2 [1,3].
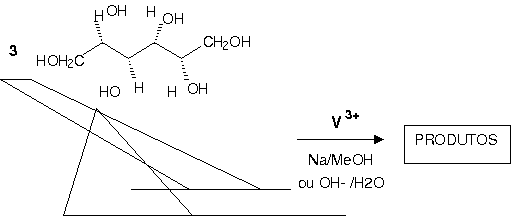
As sínteses foram realizadas sob atmosfera de N2(g) pelo uso de técnicas de Schlenk, em solução aquosa alcalina (temperatura ambiente) ou em metanol sob refluxo. Os reagentes de partida de vanádio(III), [V(acac)3] e [VCl3(thf)3] (acac = acetilacetonato e thf = tetraidrofurano) e o sal dissódico do dulcitol (galactitol, C6H14O6), gerado "in situ", foram combinados na proporção M:L de 1:3, conforme o esquema abaixo.

Esquema 1 - Preparação de alcóxidos de vanádio a partir do dulcitol em meio prótico
Os produtos sólidos verde-claros, sensíveis ao ar, foram isolados e caracterizados por análises dos teores de C, H e V, medidas de condutividade em solução aquosa, difratometria de raios-X (pó) e espectroscopias de Ressonância Magnética Nuclear de Hidrogênio (1H-RMN), Infravermeho com transformada de Fourrier (IV-TF) e Ressonância Paramagnética Eletrônica (RPE). Todas as técnicas de análise apontaram para a existência de uma mistura de sólidos (produto de reação + dulcitol não-coordenado) no material isolado a partir de metanol, mesmo após 4 dias de reação a 65oC. Este resultado é independente do material de partida de VIII empregado. Já o sólido obtido nas reações em meio aquoso alcalino (produto A, reação na proporção 1V : 3dulcitol : 6OH- por 22h à temperatura ambiente) não apresentou contaminação do pró-ligante, de acordo com o difratograma de raios-X (radiação lCo-Ka = 1,7902 Å). O produto A é praticamente amorfo, apresentando apenas bandas largas de difração nas condições de análise, enquanto o dulcitol livre é cristalino, com reflexões facilmente identificáveis nos difratogramas.
De acordo com os dados da análise elementar, o sólido obtido em meio aquoso contém três unidades dulc2- formando anéis quelatos com o metal. Os resultados são também compatíveis com a presença de um quarto ligante, possivelmente OH- ou O2-, embora o espectro de IV-FT de A não apresente absorções que possam ser inequivocamente atribuídas à presença de vanadila na região de 900 a 1000 cm-1. Teores obtidos (%m/m): C: 30,98; H: 5,56. Calculado para Na3[VIV(C6H12O6)3(OH)]×H2O: C: 31,08; H: 5,66. Calculado para Na4[VIV(O)(C6H12O6)3]: C: 30,91; H: 5,20. Apesar de sugerirem a presença de VIV no produto A, estes resultados não excluem a possibilidade de VIII (calculado para Na3[VIII(C6H12O6)3]×H2O: C: 31,86; H: 5,66). As medidas de condutividade em solução aquosa (concentração de 1,00 x 10-3 mol×L-1) feitas com o produto A e com uma série de padrões de eletrólitos MY, M2Y, M3Y e M4Y (M = Na+, K+ e Y = ânions complexos e ânions derivados de ácidos orgânicos e inorgâncos) sugerem que A seja um eletrólito do tipo M3Y (7m = 0,489 x 10-1 S×m2×mol-1). O espectro de IV-FT de A contém várias bandas de absorção característica do alditol coordenado, e não apresenta as vibrações do acetilacetonato e tetraidrofurano dos materiais de partida.
Os resultados das análises por RPE (banda X, 9,5 GHz) são independentes do material de partida de vanádio, do solvente e da temperatura de reação. Os parâmetros de RPE (extraídos por simulação dos espectros registrados em D2O à temperatura ambiente e a 77K) suportam os dados de microanálise e sugerem a oxidação de VIII a VIV durante a reação (giso = 1,977; Aiso = 73,5 x 10-4 cm-1; g* = 1,960; gz = 1,976; A* = 147,6 x 10-4 cm-1; Az = 44,2 x 10-4 cm-1). Estes dados são também compatíveis com relatos de literatura para complexos mononucleares de vanádio(IV) hexa- ou heptacoordenado contendo ligantes O-doadores [3]. Estudos de correlação giso x Aiso estão sendo desenvolvidos para relacionar os parâmetros isotrópicos com a simetria do complexo. Análises magnetoquímicas do produto A também deverão ser conduzidas, em solução e no estado sólido, para confirmar o estado de oxidação do metal.
[1] Bazhenova, T.A.; Shilov, A.E. Coord. Chem. Rev. 1995, 144, 69.
[2] Mehrotra, R.C.; Singh, A. Polyhedron 1998, 17, 689.
[3] Minhas, R.K.; Edema, J.J.H.; Gambarotta, S.; Meetsma, A. J. Am. Chem. Soc. 1993, 115, 6710.
[4] Bandwar, R. P.; Rao, C. P. J. Inorg. Biochem. 1997, 68, 1.
PIBIC/UFPR, FUNPAR, CNPq, CAPES, PRONEX