SÍNTESE DE PEPTÍDEOS EM FASE SÓLIDA: SÍNTESE DA d-MELANOTROPINA
Vinicius Caliari (IC), Milena Moraes (IC), Ademir F. Morel (PQ) e
Ionara I. Dalcol (PQ)
Departamento de Química (NPPN) - Universidade Federal de Santa Maria– Santa Maria – RS
palavras-chave: peptídeos, d-melanotropina, síntese em fase sólida
A síntese de peptídeos é de grande interesse devido a ampla aplicação farmacológica destes compostos biologicamente ativos como, por exemplo, hormônios e antibióticos. Na metodologia de síntese de peptídeos em fase sólida a sequência peptídica é sintetizada sobre um suporte polimérico mediante a incorporação sucessiva de cada aminoácido segundo as etapas de (i) acoplamento do aminoácido N-protegido e (ii) desproteção de seu grupo a-amino, até a obtenção da sequência completa. Uma vez sintetizada a sequência peptídica desejada, procede-se à sua separação do suporte polimérico, purificação e caracterização.
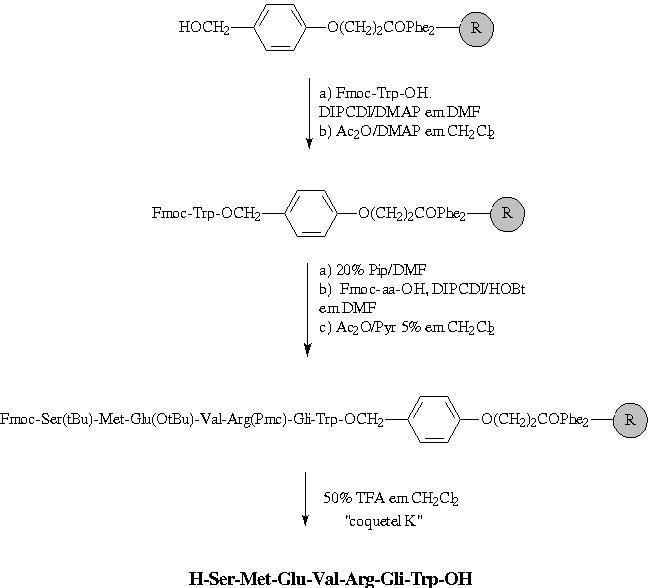
A d-melanotropina é um peptídeo de 880 Daltons composto pela sequência H-Ser-Met-Glu-Val-Arg-Gli-Trp-OH. As melanotropinas são derivadas dos hormônios corticotropina (ACTH) e b-lipotropina (b-LPH), estando presentes em várias regiões do sistema nervoso central, exercendo certos efeitos na função cerebral, tais como a aprendizagem e a retenção de novos conhecimentos. Neste trabalho, a síntese em fase sólida da d-melanotropina foi realizada mediante uma estratégia Fmoc/tBu (Esquema I), utilizando como suporte sólido a resina 4-metilbenzidrilamina (MBHA) e como separador bifuncional o ácido 3-(4-hidroximetilfenoxi)propiônico. O grupo 9-fluorenilmetiloxicarbonil (Fmoc) foi utilizado nesta estratégia sintética como grupo protetor temporário da função a-amino. As cadeias laterais dos aminoácidos serina e ácido glutâmico foram protegidas durante a síntese na forma de éter e éster terc-butírico respectivamente, enquanto a cadeia lateral do aminoácido arginina com o grupo 2,2,5,7,8-pentametilcroman (Pmc). O reagente de acoplamento diisopropilcarbodiimida (DIPCDI), em presença do supressor de racemização 1-hidroxibenzotriazol (HOBt), foi utilizado nas etapas de incorporação de cada aminoácido da sequência peptídica, sendo cada acoplamento monitorado pela realização de testes qualitativos de ninidrina. O peptídeo d-melanotropina foi obtido com um rendimento de síntese de 69%. Este peptídeo foi separado do suporte polimérico mediante acidólise com o coquetel K (87% ácido trifluoracético, 3% etanoditiol, 5% sulfeto de dimetila, 2% anisol e 3% água). O peptídeo sintetizado foi caracterizado por cromatografia líquida de alta eficácia (RPHPLC) e por espectrometria de massas MALDI-TOFF.

Esquema I - Síntese em fase sólida da d-MSH
Referências:
1. Nakanishi, S.; Inoue, A; Kita, T.; Nakamura, M.; Chang, A; Cohen, S.; Numa, S. (1979) Nature 278, 423.
2. Hadley, M. e col.; (1982) Proc. Natl. Acad. Sci. USA 79, 1751.
3. Carpino, L.A.; El-Faham, A.; Minor, C.A.; Albericio, F. (1994) J. Chem. Soc., Chem. Commun, 201-203.