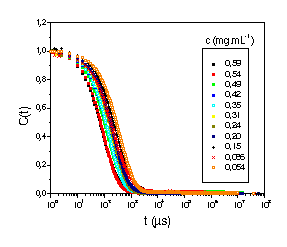
Figura 1. FCTs a 25°C e q=90° da solução mãe (0,59 mg.mL-1) e subsequentes diluições com DMF.
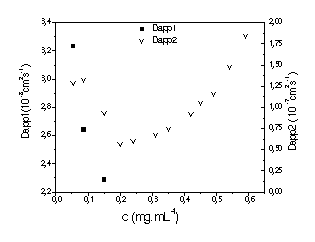
Figura 2. Coeficientes de difusão aparente (CONTIN) da solução mãe (0,59 mg.mL-1) e subsequentes diluições com DMF.
ESTUDO DA ESTABILIDADE DE AGREGADOS MICELARES (CREW-CUT) OBTIDOS A PARTIR DE COPOLÍMEROS ASSIMÉTRICOS ANFIFÍLICOS
Izabel Cristina Riegel (PG), Cesar Liberato Petzhold (PQ), Dimitrios Samios (PQ).
Instituto de Química - Universidade Federal do Rio Grande do Sul -UFRGS.
Av. Bento Gonçalves,9500 – 91501-970 – Porto Alegre - RS
e-mail:iriegel@if.ufrgs.br
Palavras-chave: micelas crew-cut, copolímeros assimétricos, espalhamento de luz.
1.INTRODUÇÃO
Micelas do tipo crew-cut 1 são formadas em solução aquosa a partir de copolímeros em bloco assimétricos que possuem uma longa cadeia hidrofóbica e uma pequena cadeia hidrofílica. Estas microesferas, cujo núcleo hidrofóbico é algumas dezenas de vezes maior que a coroa hidrofílica, possuem dimensões nanométricas e estabilidade termodinâmica. O núcleo pode servir como um microcontainer para várias substâncias2 viabilizando sua aplicabilidade nas áreas biológica e farmacêutica (drug delivery)3. Copolímeros em bloco assimétricos a base de aminoisoprenos apresentam-se como excelentes sistemas para obtenção de micelas crew-cut. A quaternização do grupo amino terciário presente no poli[5-(N,N-(dialquilamino)isopreno)-b- estireno], dá origem a um bloco catiônico que favorece a solubilidade destes polímeros em água.
2. OBJETIVO
Estudar a estabilidade e o comportamento em solução de agregados crew-cut obtidos a partir do copolímero tribloco poli [dietilamino(isopreno)-b-estireno-b-dietilamino(isopreno)], através de espalhamento de luz dinâmico (DLS).
3.METODOLOGIA
Procedeu-se à quaternização dos grupos amino terciário presentes nos blocos 5-N,N-(dialquilamino)isopreno 4 do copolímero a fim de torná-los catiônicos. Devido ao longo bloco poli(estireno) estes copolímeros iônicos não são solúveis diretamente em água, sendo necessária a prévia dissolução em DMF, que é um bom solvente para o poliestireno. Em seguida, água deionizada foi adicionada vagarosamente (20% em volume), sob agitação constante, para que ocorra a microseparação de fase devido a formação do agregado. A solução coloidal resultante foi dialisada por 3 dias contra água destilada para a remoção do DMF. A estabilidade da solução mãe foi estudada através de espalhamento de luz dinâmico procedendo-se a diluições da mesma com DMF e também com água. Foram avaliados para cada diluição: raio hidrodinâmico aparente(Rhapp), coeficiente de difusão aparente (Dapp) e a função de correlação temporal (FCT) a um ângulo de espalhamento q=90° e a 25°C.
4.RESULTADOS E CONCLUSÕES
A Figura 1 mostra uma série de FCTs, de soluções com diferentes concentrações, obtidas a partir da diluição da solução mãe (0,59 mg.mL-1) com DMF. Em todas as concentrações, pôde-se observar um único decaimento exponencial e um aumento do tempo de relaxação com a diluição, indicando um aumento no tamanho do agregado. Pelo tratamento de dados através do programa CONTIN (Figura 2), da C=0,59 mg.mL-1 (mãe) a C=0,2 mg.mL 1, observou-se a existência de agregados monodispersos, isto é, uma única estrutura foi detectada (um único Dapp). Porém, nas concentrações mais baixas, surgem dois processos de relaxação, um rápido e um lento, evidenciando a coexistência de duas estruturas. Este comportamento demonstra a afinidade do núcleo hidrofóbico com DMF, levando-o a um inchamento frente a contínuas diluições e ao colapso da micela crew-cut a C=0,2 mg.mL-1 (70% vol DMF). A partir desta concentração acredita-se ocorrer a inversão da micela, devido à menor afinidade do bloco aminoisopreno com DMF, que estaria em equilíbrio com a cadeia isolada.
Ao contrário, quando procedeu-se a diluições com água, os parâmetros dinâmicos das soluções não se alteraram quando comparados à solução mãe, demonstrando a estabilidade do agregado em água até concentrações em torno de 10-3 mg.mL-1.
|
|
|
|
|
Figura 1. FCTs a 25°C e q=90° da solução mãe (0,59 mg.mL-1) e subsequentes diluições com DMF. |
|
Figura 2. Coeficientes de difusão aparente (CONTIN) da solução mãe (0,59 mg.mL-1) e subsequentes diluições com DMF. |
5.BIBLIOGRAFIA
1 Zhang, L.; Eisenberg, A. J. Am. Chem. Soc. 1996, 118, 3168.
2 Lee, S. C.; Chang, Y.; Yoon, J.; Kim, C.; Kwon, I. C.; Kim, Y. H.; Jeong, S. Y.; Macromolecules 1999, 32, 1847.
3. Iyama, K.; Nose, T. Macromolecules 1998, 31, 7356.
4. Petzhold, C.; Kolshorn, H.; Stadler, R. Macromol.Chem.Phys., 1995, 196, 1405.
CAPES