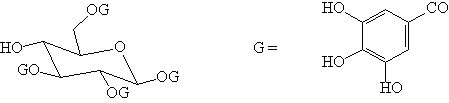
1,2,3,6-TETRAGALOILGLUCOSE DE CHAMAESYCE THYMIFOLIA MILLSP. (EUPHORBIACEAE)
Priscila Guimarães Salgado1 (IC), Wasley de Santana Bessa1 (IC), Ana Claudia Fernandes Amaral2 (PQ), Antonio Jorge Ribeiro da Silva1 (PQ) e Ricardo Machado Kuster1 (PQ)
Núcleo de Pesquisas de Produtos Naturais – Universidade Federal do Rio de Janeiro. 2. Fundação Oswaldo Cruz – Central Analítica, Farmanguinhos.
Palavras-chaves: tanino hidrolisável, Chamaesyce, RMN
Introdução: Chamaesyce thymifolia é uma planta da família Euphorbiaceae, cujo chá das folhas é popularmente utilizado no Brasil como diurético, para tratamento de infecções do tracto geniturinário e para remover verrugas. Pouquíssimos estudos fitoquímicos foram realizados com plantas deste gênero. Em estudo anterior, relatamos a atividade antiviral dos flavonóides de Chamaesyce thymifolia contra os vírus da herpes e diarréia bovina1. Neste trabalho, abordamos o isolamento e identificação estrutural de um tanino hidrolisável, o 1,2,3,6-tetragaloilglucose, o principal constituinte da fração polifenólica do extrato aquoso das partes aéreas da planta. Quantidades consideráveis de taninos hidrolizáveis têm sido isolados de várias plantas até o momento. A maioria contém um monossacarídeo, principalmente a D-glucose ou um poliol cíclico, os quais são esterificados com ácidos polifenólicos, como gálico, cinâmico e quínico2. O padrão de metabolismo do ácido gálico envolve três principais vias: 1. A formação de ésteres simples com açúcares, polióis e outros fenóis, 2. A formação de depsídeos e 3. A formação de ésteres (S)-hexahidróxidifenoíla com a D-glucopiranose em sua forma mais estável2. Entretanto, alguns grupos de plantas adotam uma variação metabólica adicional, na qual o acoplamento oxidativo entre dois ésteres galoilas adjacentes ocorrem para formar ambos os ésteres (S) e (R)-hexahidróxidifenoíla com uma D-glucopiranose em conformação menos estável2. Este grupo restringe-se a determinadas famílias vegetais, como Cercidiphyllaceae, Ericaceae, Onagraceae, Combretaceae, Nyssaceae, Aceraceae, Punicaceae, Simaroubaceae e Geraniaceae3.
Objetivo: Este trabalho objetiva o isolamento e identificação estrutural do tanino hidrolisável majoritário do extrato aquoso de Chamaesyce thymifolia.
Métodos: Cerca de 1 Kg das partes aéreas da planta fresca foram trituradas em liquidificador com cerca de 100 mL de água destilada. O material triturado foi derramado sobre 500 mL de água fervente e deixado em infusão por 5 minutos. Após 20 minutos em repouso, o chá foi filtrado e concentrado a 50 mL sob pressão reduzida. A solução resultante foi submetida a partições em clorofórmio e acetato de etila. A fração em acetato de etila foi redissolvida em água e cromatografada sobre uma coluna XAD-16 eluída inicialmente com água e crescendo o conteúdo em metanol até torná-lo o único solvente. As frações provenientes da XAD-16 foram concentradas sob pressão reduzida e cromatografadas em camafa fina de gel de sílica. Àquelas contendo substâncias reveláveis com nitrito de sódio/ácido acético foram reunidas por se tratar de taninos hidrolisáveis. Uma das frações que continha uma substância majoritária foi cromatografada sobre sephadex LH-20 (metanol como eluente) e depois sobre gel de sílica RP-18 (metanol:água, 3:7). Deste processo de separação foi obtido um pó branco amorfo, o qual se mostrou puro quando analisado por CLAE/UV.
Resultados: A amostra isolada foi analisada por 1H-RMN e 13C-RMN. O espectro de 1H-RMN mostra quatro sinais simples entre d 7,0 e 7,2 ppm, cada um integrado para dois hidrogênios, característicos de 4 resíduos galoilas, enquanto entre d 4 e 6 ppm surgem os hidrogênios da glucose, na qual se liga os 4 resíduos galoílas. O deslocamento das frequências de absorção dos hidrogênios do açúcar para campo magnético mais baixo comprova a esterificação das hidroxilas da glucose. As posições de galoilação nos carbonos 1,2,3 e 6 da glucose foram determinadas inequivocamente a partir da comparação com os dados de deslocamento químico de 13C-RMN da literatura3.
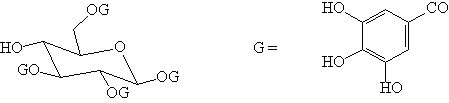
Conclusão: Taninos hidrolisáveis são comuns na família Euphorbiaceae. Do ponto de vista medicinal, a 1,2,3,6-tetragaloilglucose mostrou atividade inibitória da adesão de células LL2-Lu3 metastáticas em pulmão de camundongo4 e inibição da formação do complexo-II da cadeia respiratória mitocondrial em músculo de Ascaris5.
Referências bibliográficas:
Amaral, A.C.F., Kuster, R.M., Gonçalves, J.L.S., Wigg, M.D. Fitoterapia 70, 293-295 (1999).
Haddock, E.A., Gupta, R.K., Haslam, E. J.Chem.Soc.Perkin. Trans. I 2535-2545 (1982).
Yoshida, T., Hatano, T., Okuda, T., M, M.U., Shingu, T., Inoue, K. Chem. Pharm. Bull. 32, 1790-1799 (1984).
Saeki, K., Shoji, Y., Noro, T., Miyase, T., Nakamura, Y., Funayama, M., Isemura, M. Planta Medica 65, 227-229 (1999).
Konoshi, K., Adachi, H., Kita, K., Takamiya, S., Furushima, R., Oya, H., Horikoshi, I. Chem. Pharm. Bull. 37, 2533-2534 (1989).