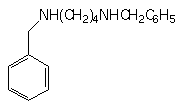ATIVIDADE
MOLUSCICIDA DE NITROAROMÁTICOS SINTÉTICOS. INFLUÊNCIA
DO POTENCIAL REDOX E DOS SUBSTITUINTES
1Fabiane
Caxico de Abreu 1,2(PG), Francine Santos de
Paula 1(IC),
Aldenir
Feitosa dos Santos1(PQ), Antônio Euzébio
Goulart Sant’Ana1 (PQ),
2Mauro
Vieira de Almeida3 (PQ), 1Marília O. F.
Goulart1 (PQ)*
1Departamento
de Química, Universidade Federal de Alagoas, 57.092-970,
Maceió, AL, 2Departamento de Química
Fundamental, UFPE, Recife, Pernambuco, 3Núcleo de
Pesquisas Químicas, ICE, Universidade Federal de Juiz de Fora,
Juiz de
Fora, MG. e-mail: mofg@qui.ufal.br
Palavras-chave:
nitroaromáticos, potenciais redox, moluscicida
INTRODUÇÃO
A
esquistossomose mansônica é doença parasitária
causada pela presença do helminto Schistosoma mansoni
no fígado das pessoas infectadas. É endêmica e
afeta regiões tropicais e sub-tropicais. O molusco
Biomphalaria glabrata age como hospedeiro intermediário.
A redução da esquistossomose é crucial. A
utilização de agentes moluscicidas promove a ruptura do
ciclo evolutivo do verme e é considerada um dos principais
pontos de ataque, em termos de erradicação da doença1.
Os
moluscicidas de uso atual são de origem sintética ou
natural. Vários deles são nitrocompostos aromáticos.
A presença do grupo nitro parece ser obrigatória. Este
requisito indica que parte da atividade deriva provavelmente da
produção nitro-catalisada de espécies oxigenadas
reativas ou ainda da ação de metabólitos
nitrogenados com menor estado de oxidação. Os objetivos
do presente trabalho consistiram em avaliar a ação
moluscicida (em adultos Biomphalaria glabrata) de compostos
nitroaromáticos, com a obtenção concomitante de
seus dados eletroquímicos, na perspectiva de correlacionar os
dados obtidos, o que poderia influenciar no planejamento de novas
moléculas. Os compostos investigados foram divididos em cinco
grupos principais.
|
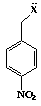
Grupo
A
|
1:
X = NH(CH2)6NH2
2:
X = NH(CH2)2SH
3:
X = OH
|
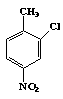
4
|
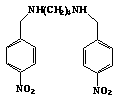
5
|
|
|
|
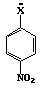
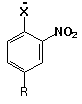
Grupo
B
|
6:
X = NH2
7:
X = OH
8:
X = NHCOCH3
9:
X= NHNH2
|
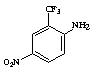
10
|
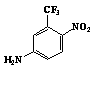
11
|
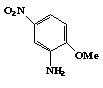
12
|
|
|
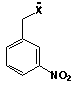
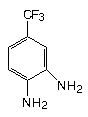
Grupo
C
13:
X = NH2; R = CF3
14:
X = NH2; R = OMe
|
|
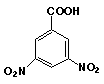
Grupo
D
15:
X = NH(CH2)2NH2
16:
X = NH(CH2)2SH
|
 17 17
|
|
|
20
Grupo E
|
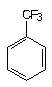
18
|
 19 19
|
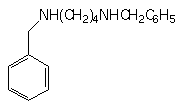
|
|
|
EXPERIMENTAL
Os
potenciais redox, em volts (V), foram obtidos em meio aquoso
tamponado (tampão fosfato, pH 7), são expressos vs.
eletrodo de Ag / AgCl,Cl-(0,1 M), por uso de voltametria
cíclica, em Hg. Os bioensaios seguiram os protocolos
estabelecidos pela OMS. As substâncias foram solubilizadas pelo
emprego de soluções contendo DMSO a 0,1 %. Seus valores
são expressos em ppm.
RESULTADOS
E DISCUSSÃO
A
tabela 1 indica os valores de DL50 e os de Epc1
obtidos para 1-20.
Tabela
1: Atividades moluscicidas e parâmetros eletroquímicos
dos nitroaromáticos
|
Comp
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
|
DL50
|
72,4
|
116,5
|
I
|
1,82
|
40,2
|
56,1
|
8,2
|
I
|
0,07
|
55,6
|
|
Epc1
|
-0,532
|
-0,533
|
-0,700
|
-0,606
|
-0,541
|
-0,840
|
-0,857
|
-0,773
|
-0,833
|
-0,840
|
|
Comp
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
19
|
20
|
|
DL50
|
52,9
|
I
|
48,8
|
86,8
|
I
|
I
|
I
|
I
|
I
|
I
|
|
Epc1
|
-0,816
|
-0,762
|
-0,810
|
-0,730
|
-0,636
|
-0,597
|
-0,558
|
EI
|
EI
|
EI
|
*
Instável; I = inativo; EI = eletroinativo
Alguns
dos compostos acima (4, 7, 9) apresentam
atividade significativa.
A
comparação entre os dados da tabela 1 (DL50
e Epc1) indica que a presença do grupo nitro é
fundamental para a atividade biológica. O mesmo efeito foi
anteriormente observado para agentes esquistossomicidas2.
A faixa de potencial de redução do grupo nitro é
muito larga e não se observa qualquer correlação,
o que parece indicar que enzimas (nitroredutases) presentes no
molusco são capazes de reduzir grupos nitro em diferentes
ambientes. O parâmetro mais importante está relacionado
à presença de grupos eletrodoadores em orto e
para aos grupos nitro aromáticos, diretamente ligados
ao anel ou em posição benzílica. Os resultados
sugerem a possível formação de espécies
eletrofílicas, após redução do grupo
nitro, em mecanismo similar ao descrito para drogas
anti-helmínticas2.
1
Lardans, V., Dissous, C. Parasitol.
Today 14 (1), 413-417, 1998.
2Cioli,
D.; Pica-Mattoccia, L.; Archer, S. Pharmac. Ther. 68 (1),
35-85, 1995.
FAPEAL,
CNPq, CAPES, FAPEMIG, OMS
![]()


![]()





 17
17
 19
19