ELETRORREDUÇÃO,
EM MEIO APRÓTICO, DE NAFTOQUINONAS 2-METIL- E
2,3-DIMETIL-SUBSTITUÍDAS. INFLUÊNCIA DO GRUPO
SUBSTITUINTE. CORRELAÇÃO
COM ATIVIDADES ANTI-CANCERÍGENAS.
Fabiane
C. de Abreu (PG)1,2, Adriana Carla de O. Lopes (IC)1,
Nivaldo A. Soares (PQ)1, Antônio V. Pinto (PQ)3,
Marília O. F. Goulart (PQ)1
1Departamento
de Química, CCEN, UFAL, Maceió-AL, 57072-970,
2Departamento de Química Fundamental, UFPE, Recife,
Pernambuco,
3Núcleo
de Pesquisas de Produtos Naturais, UFRJ, Rio de Janeiro-RJ
e-mail:
mofg@Qui.ufal.br; fca@Qui.ufal.br
palavras-chave:
quinonas, câncer, comportamento eletroquímico
INTRODUÇÃO
O
conceito de biorredução originando agentes alquilantes
de biomoléculas, principalmente macromoléculas, é
freqüentemente utilizado em química medicinal. Em relação
ao ADN, agentes alquilantes bifuncionais podem originar ligações
cruzadas intra- e inter-fitas e inter-hélices. Propriedades
estruturais bem definidas e potenciais redox em faixa adequada são
necessários, visando a obtenção de
intermediários eletrofílicos reativos.
No
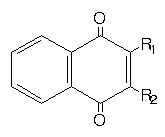
presente trabalho, quinze derivados da 2,3-dimetil-1,4-naftoquinona,
substituídos em uma ou ambas as cadeias laterais, com grupos
de diferente nucleofilia foram preparados e submetidos a estudos
eletroquímicos (voltametria cíclica e eletrólise),
de modo a investigar uma possível correlação
entre os parâmetros eletroquímicos (potencial de redução
da primeira onda catódica) obtidos em meio aprótico e
suas atividades anti-cancerígenas registradas na literatura.
Além disso, esses compostos são muito interessantes do
ponto de vista eletroquímico, por apresentarem dois sítios
eletroativos separados por um grupo metilênico (R1CH2R2).
Em condições redutivas, há possibilidade de
formação de quinonametídeo, após
eliminação do grupo abandonador adequadamente
localizado. Conseqüentemente, a natureza do grupo abandonador é
de alta relevância. Trabalhos anteriores1 indicaram
a complexidade do comportamento eletroquímico e permitiram
evidenciar a ocorrência da clivagem da ligação
C-X. Discute-se, portanto, a influência da natureza do grupo
substituinte no processo de eletrorredução. O meio
aprótico foi escolhido (DMF/TBAP 0,1 M), por mimetizar
ambientes celulares hidrofóbicos.
|
|
1:
R1 = Me; R2 = H; 2: R1 =
R2 = CH2Br;
3:
R1 = Me; R2 = CH2Br; 4: R1
= Me; R2 = CH2Cl;
5:
R1 = R2 = CH2Cl; 6: R1
= Me; R2 = CH2I;
7:
R1 = Me; R2 = CH2OAc; 8:
R1 = R2 = CH2OAc;
9:
R1 = Me; R2 = CH2OTs; 10:
R1 = R2 = CH2OTs;
11:
R1 = Me; R2 = CH2OH; 12:
R1 = R2 = CH2OH;
13:
R1 = Me; R2 = CH2ONO2;
14:
R1 = Me; R2 = CH2OCOH; 15:
R1 = R2 = Me
|
EXPERIMENTAL
A
síntese de alguns dos derivados quinônicos é
descrita pela primeira vez e os dados espectrais são
totalmente compatíveis com as estruturas propostas (6,
13, 14). Estudos voltamétricos foram realizados
em meio aprótico (DMF/TBAP 0,1 M), utilizando como eletrodo de
trabalho gota pendente de Hg (HMDE) ou Carbono Vítreo (Cv),
eletrodo auxiliar um fio de platina e referência, Ag/AgCl,Cl-
(0,1 M). Eletrólises em potencial controlado foram realizadas
em poço de Hg, espiral de platina e mesmo eletrodo de
referência da Voltametria Cíclica (VC). Os experimentos
foram realizados em um potenciostato/galvanostato da marca PAR 270.
RESULTADOS E DISCUSSÃO
A
facilidade de redução, em Hg, expressa através
da comparação dos dados de Epc1 é a
seguinte: 10 (-0,252 V) > 2 (-0,286 V) > 3
(-0,305 V) > 5 (-0,310 V) > 9 (-0,345 V) >
6 (-0,355 V) > 4 (-0,404 V) > 13 (-0,428
V) > 8 (-0,579 V) > 14 (-0,670 V) > 7
(-0,678 V) > 12 (-0,695 V) > 11 (-0,764 V) > 1
(-0,775 V) > 15 (-0,840 V).
|
De modo geral, os
compostos bis-substituídos são reduzidos mais
facilmente do que os correspondentes monossubstituídos, no
entanto, sua instabilidade, nas condições
experimentais atuais impede o estudo eletroquímico mais
aprofundado. Do ponto de vista eletroquímico, a facilidade
de clivagem da C-X, pode ser estabelecida da seguinte maneira:
Br>OTs>I>Cl>ONO2>OCHO>OAc>OH.
A comparação do comportamento
eletroquímico das quinonas monossubstituídas
estudadas em função do grupo substituinte, permitiu
classificá-las em três grupos diferentes:
|
|
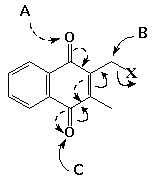
Grupo A: quinonas 1, 10, 15
apresentam redução típica de quinonas;
Grupo B: quinonas 3, 4 e 6,
mecanismo mais complexo dependente da velocidade de varredura, com
redução preliminar na C-X, levando à formação
de intermediários reativos;
Grupo C: quinonas 7, 9, 13,
14, com redução no grupo quinonoídico e
cisão de ligação após a entrada de um ou
dois elétrons (7).
Apesar
do número limitado de ensaios anti-cancerígenos
encontrados2,3 e da impossibilidade de realizá-los
localmente, é possível tecer considerações
importantes e diferentes daquelas obtidas em meio aquoso2.
Observa-se que uma maior atividade está ligada a quinonas com
potenciais de oxirredução mais positivos (> - 0.5
V). Os compostos completamente inativos apresentam potenciais bem
mais negativos e comportamentos em VC menos complexos. Não há
clivagem do ligação C-X. O meio aprótico permite
discriminar os grupos substituintes em abandonadores fortes e fracos.
REFERÊNCIAS
1Abreu,
F. C. et. al. Livro de Resumos da 22a. Reunião
Anual da SBQ, EQ-045, Poços de Caldas.
2Lin,
A. J., Sartorelli, A. C. Biochem. Pharmacol. 25, 206-207,
1976.
3Lin,
T, Antonini, I, Cosby, L. A, Sartorelli, A., C., J. Med. Chem.
27, 813, 1984
FAPEAL, CNPq,
CAPES, PADCT

