FLAVONÓIDES DAS FOLHAS DE CAESALPINIA PYRAMIDALIS
Marcus Vinícius Bahia (IC)1, Jorge Mauricio David (PQ)1, Juceni Pereira David (PQ)2
1Instituto de Química; 2Faculdade de Farmácia, Universidade Federal da Bahia, 40170-290, Salvador-BA.
(jmdavid@ufba.br)
Palavras-chave: Caesalpinia pyramidalis, Leguminosae, biflavonóides
A subfamília Caesalpinaceae-Leguminosae, compreende aproximadamente 2000 espécies distribuídas em 150 gêneros. Os representantes brasileiros do gênero Caesalpinia abrangem uma grande variedade de espécies sendo que a mais conhecida é C. echinata (pau-brasil)1. Na Bahia as folhas de C. pyramidalis Tul., uma árvore dispersa na caatinga e popularmente chamada de “catingueiro” ou “pau-de-rato”, é empregada para febre, doenças estomacais e como diurético2. No primeiro estudo fitoquímico realizado com C. pyramidalis, foram isolados além de lupeol, sitosterol, dois novos derivados dos ácidos 7-hidroxi e 8-hidroxi-cinâmicos, bem como uma biflavona (agastiflavona)3. Dando continuidade ao estudo fitoquímico de C. pyramidalis, no presente trabalho são descritos o isolamento de um novo biflavonóide (1) além do kaempferol e apigenina.
O extrato clorofórmico das folhas de uma espécimen de Caesalpinia pyramidalis foi submetido a CC sob sílica gel, eluída com misturas de CHCl3:MeOH em diferentes polaridades. Foram obtidas várias frações que foram reagrupadas por CCDC. Uma dessas frações reagrupadas (465 mg), eluídas com 15% de MeOH, foi submetida à permeação em Sephadex LH-20 obtendo-se 8 novas frações. As frações foram novamente submetidas a CC sob sílica gel obtendo-se 12 mg de 1 e uma mistura do kaempferol e apigenina (14 mg).
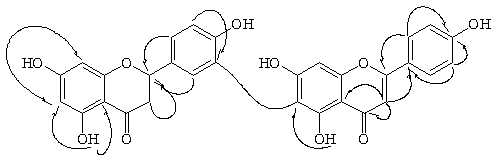
A determinação estrutural de 1 foi realizada através da análise dos dados dos espectros de RMN de 1H e de 13C (PND, DEPT), HMQC, HMBC e de massas, bem como através de comparação com dados descritos na literatura. Análise dos espectros de RMN claramente mostrou que 1 era constituída de unidades de flavona e flavanona. São sinais característicos no espectro de RMN de 13C de cada uma destas unidades, a carbonila em d 182,9 e o Csp2–H em d 103,28 referente ao C-3 da flavona. Enquanto que a carbonila em d 197,19, o carbono metilênico (d 42,87) e o oxibenzílico em d 79,51 são sinais característicos do anel C da flavanona. O espectro de RMN de 1H de 1 corrobora com o exposto anteriormente, uma vez que apresenta sinais dos hidrogênios a-carbonílicos em d 3,14 (dd, J=14,0 e 12,6 Hz), d 2,72 (dd, J=14,0 e 3,0 Hz) e um dd (d 5,38, J=12,6 e 3,0 Hz) correspondente ao hidrogênio oxibenzílico. A natureza biflavonoídica da substância pode ser evidenciada pela presença de sinais de dois carbonos não hidrogenados em d 96,42 e 130,69 sugerindo uma interligação entre o anel A de uma unidade e o anel B da outra unidade. Apesar do EMIE não ter registrado o íon molecular da substância, apresentou íon molecular de uma das unidades, bem como fragmentos de massas maiores, indicando não tratar-se de uma mistura. O espectro HMBC mostrou várias correlações que permitiram localizar a interligação entre as duas unidades flavonoídicas (Figura). Comparação com os dados de RMN de 13C da robustaflavona (2) e 3",8"-binarigenina (3)4, comprovaram a estrutura proposta para 1, bem como auxiliaram na atribuição dos dados de RMN.

1
Figura - Correlações observadas no espectro de HMBC de 1.
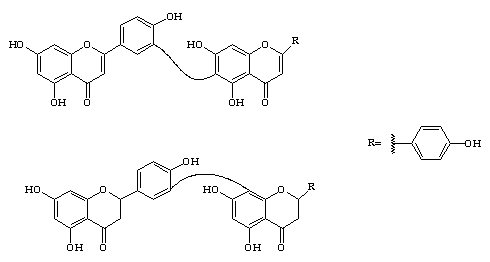
2
3
Referências:
Joly, A. B. Botânica – Introdução a Taxonomia Vegetal. Cia Ed. Nacional, 4a ed., São Paulo, 1977, p. 371.
Inventário de Plantas Medicinais do Estado da Bahia. Ed. pelo Gov. Estado da Bahia, SEPLANTEC/CADCT, 1979.
Mendes, C. C., Bahia, M. V., David, J. M., David, J. P. (2000) Fitoterapia 71, (no prelo).
Agrawal, P. K., Bansal, M. in Carbon-13 NMR of Flavonoids. Ed. by P.K. Agrawal, Elsevier – Amsterdam, 1989, p. 247.
PIBIC/CNPq/UFBA, CNPq