SÍNTESE
DO SEGMENTO C1-C12
DOS AGENTES
IMUNOSSUPRESSORES
PIRONETIN E NK-10958P
Luiz
C. Dias (PQ) e Luciana G. de Oliveira (PG)
Instituto
de Química - UNICAMP - C.P. 6154 - CEP: 13081-970
Campinas
- SP - Brasil - e-mail: ldias@iqm.unicamp.br
Palavras-chave:
pironetin, condensação aldólica, agente
imunossupressor
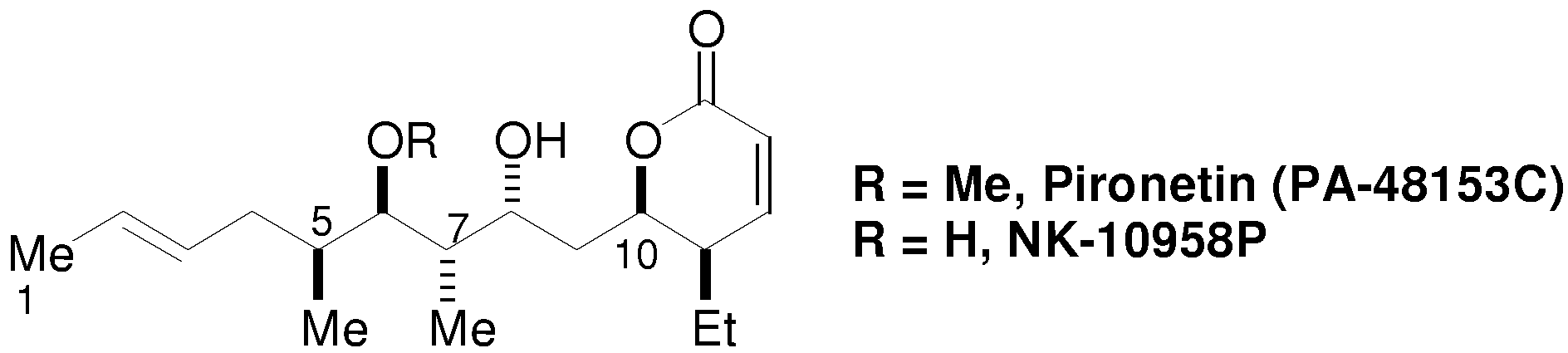
Introdução:
Agentes imunossupressores são importantíssimos na
prevenção à rejeição de órgãos
após transplantes cirúrgicos. Em 1993, foi relatado o
isolamento de um novo derivado de 2-piranona, Pironetin (PA-48153C)
a partir do produto da fermentação de Streptomyces
prunicolor PA-48153C e Streptomyces sp. NK-10958.1
Pironetin
mostrou atividade como regulador de crescimento de plantas e potentes
efeitos supressores nas respostas de linfócitos T e B para
mitogens. A maior limitação com relação
ao uso do Pironetin é a alta citotoxicidade observada em
várias células tumorais, mostrando que PA-48153C é
ainda muito tóxico para uso terapêutico. Recentemente,
resultados muito promissores foram alcançados em esforços
para reduzir a toxicidade por modificações químicas
do Pironetin a partir da preparação de derivados.2
Objetivos:
Nossa intenção é desenvolver uma rota
curta e eficiente para a síntese do Pironetin e do NK-10958P,
que possibilite também a preparação de novos
derivados com atividade imunossupressora. A rota proposta a seguir
possibilita que modificações estruturais sejam feitas
com este objetivo.3
Resultados:
Dando continuidade em nosso trabalho visando a síntese total
do Pironetin e do NK-10958P,3
a imida 1 foi metilada para fornecer o produto 2 em 60%
de rendimento. Devido ao rendimento moderado e dificuldade para
reproduzir esta reação, dificuldade de purificação
do produto por coluna cromatográfica, principalmente porque
observamos epimerização parcial do centro em C2,
decidimos promover algumas alterações. Redução
da imida 1 para o diol 3, tosilação
seletiva do álcool primário e metilação
forneceram o tosilato 5 em excelentes rendimentos. Extensão
da cadeia por reação com o cuprato derivado do
(E)-1-bromo-1-propeno, remoção do protetor PMB
em 6 com DDQ, seguido de oxidação de Swern,
conduziram ao aldeído 8 em ótimos rendimentos.
Condensação aldólica de 8 com o enolato
de boro da oxazolidinona 9 levou ao aduto aldol 10 em
94% de rendimento e >95:5 de diastereosseletividade.

Bibliografia:
1.Kobayashi, S.; Tsuchiya, K.; Harada, T.;
Nishida, M.; Kurokawa, T.; Nakagawa, T.; Shimada, N.; Kobayashi, K.;
J. Antibiot. 1994, 47, 697; 2.Yasui, K.;
Tamura, Y.; Nakatani, T.; Horibe, I.; Kawada, K.; Koizumi, K.;
Suzuki, K.; Ohtani, M. J. Antibiot. 1996, 49,
173; 3.Dias, L.C.; Oliveira, L.G. “Estudos Visando a
Síntese Total do Agente Imunossupressor Pironetin”, 22a
Reunião Anual da Sociedade Brasileira de Química –
SBQ – Poços de Caldas – MG – 25 a 28/05/99.
Livro de Resumos: QO-086.
FAPESP/CNPq

