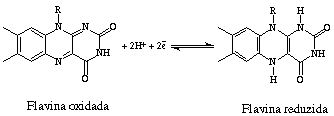
Riboflavina
PROPRIEDADES ELETROQUÍMICAS DA FLAVINA IMOBILIZADA SOBRE A SUPERFÍCIE DA SÍLICA GEL MODIFICADA COM ÓXIDO DE ZIRCÔNIO
Miyuki Yamashita (PG) e Lauro T. Kubota (PQ)
Instituto de Química - Universidade Estadual de Campinas
palavras-chave: flavinas, eletrodos de pasta de carbono, óxido de zircônio.
O comportamento eletroquímico das flavinas tanto em solução como imobilizadas sobre a superfície do eletrodo vem sendo frequentemente descrito na literatura [1,2].. Existe um grande interesse em investigar o mecanismo do processo catalítico envolvendo flavinas, visto que as mesmas apresentam um papel importante nos processos biológicos, atuando como transportador de elétrons nos metabolismos dos seres vivos na produção de energia. A função biológica das flavinas é bastante diversificada. A riboflavina participa no metabolismo das proteínas carbohidratados e lipídios; enquanto os derivados da riboflavina (RF), flavina mononucleotídeo (FMN) e flavina adenina dinucleotídeo (FAD) são grupos prostéticos das flavoproteínas os quais funcionam como membro do sistema redox celular. A RF apresenta um comportamento eletroquímico semelhante às FMN e FAD no qual são envolvidos dois elétrons e um próton, sendo que a parte reativa das flavinas está localizada no anel aloxazina (Figura 1).
|
|
Riboflavina |
Figura 1 – Representação esquemática da reação de oxi-redução da flavina.
O presente trabalho tem como objetivo estudar o comportamento eletroquímico da riboflavina (RF) imobilizada sobre sílica gel modificada com óxido de zircônio, utilizando-se eletrodo de pasta de carbono em meio aquoso.
A modificação da sílica gel com óxido de zircônio (Si:Zr) foi realizada, procedimento adaptado [3], a partir da reação da sílica gel 60, granulometria de 230-400 mesh (25 g), com oxicloreto de zircônio (8,14 g) dissolvido em 150 mL de água deionizada (Milli-Q). Esse material foi caracterizado por fluorescência de raios X e análise superficial (BET). A quantidade de zircônio adsorvido sobre a superfície da sílica gel foi de 1,15 mmol g-1 com área superficial de 426 m2 g-1.
A flavina foi adsorvida sobre a superfície da matriz Si:Zr pela adição de 10 mL da solução de 0,02 % de riboflavina (m/v) em 200 mg de Si:Zr. Esse material foi agitado durante três horas em um agitador mecânico a 25o C, filtrado, seco sob vácuo e armazenado em dessecador (24 horas). A quantidade de riboflavina adsorvida sobre a matriz (Si:Zr:RF) foi determinada por análise elementar, obtendo-se 82 mmol g-1 de riboflavina.
A pasta de carbono foi preparada a partir da mistura de Si:Zr:RF (56%), grafite (44%) e óleo mineral, sendo posteriormente colocada na cavidade do eletrodo de trabalho (0,1 cm de profundidade x 0,3 cm de diâmetro). O eletrodo de calomelano saturado (ECS) foi usado como eletrodo de referência e um fio de platina em espiral foi usado como eletrodo auxiliar. Esses eletrodos foram colocados em uma célula de vidro com entrada e saída para gás, contendo solução de KNO3 0,1 mol L-1. As medidas eletroquímicas foram realizadas utilizando-se um potenciostato modelo PGSTAT20 da AUTOLAB.
Na Figura 2 é apresentado o voltamograma do eletrodo de pasta de carbono com e sem a riboflavina imobilizada sobre a superfície da matriz Si:Zr. Ao imobilizar a riboflavina pode-se verificar o aparecimento de picos redox reversíveis na região entre -460 mV e -340 mV, os quais foram atribuídos à riboflavina imobilizada. O coeficiente de transferência de elétrons (a) foi determinado a partir da relação potencial de pico anódico vs. log v, de acordo com Laviron [4]. O aanódico obtido foi 0,41, evidenciando que o processo redox do sistema é quasi-reversível. Não houve diferença significativa na resposta do eletrodo de Si:Zr:RF para os diferentes ânions (Cl-, NO3-, SO42- e ClO4-) e cátions (Li+, Na+, K+, NH4+ e Ca2+) estudados.
Na Figura 3 é ilustrado o estudo da influência do pH na resposta da riboflavina em solução e imobilizada (Si:Zr:RF). Para o eletrodo de Si:Zr:RF o potencial formal (Eo´ = (Epa + Epc)/2) mantém-se constante no intervalo de pH entre 3 e 8. Para valores de pH menores que 3, o Eo´ se desloca para regiões mais positivos (Figura 3a). No caso da riboflavina em solução (Figura 3b), verifica-se uma diminuição linear de 52 mV/pH, o qual é próximo do verificado por SUN e col. (1996) [5]. Em pH 7,0 existe uma pequena diferença no valor do Eo´ da riboflavina em solução e imobilizada de 86 mV. Este deslocamento no Eo´ da riboflavina imobilizada para valores mais positivos pode ser atribuído à acidez do óxido de zircônio e/ou efeito protetor da matriz.
|
Figura 2 – Voltamograma cíclico obtido para eletrodo de pasta de carbono modificado contendo Si:Zr:RF (a) e sem a riboflavina (b). |
Figura 3 – Dependência do Eo´ da riboflavina imobilizada (a) e em solução (b) em função do pH da solução. |
[1] WANG, Y.; XU, Bo; ZHU, G.; WANG E. Electroanalysis. 9 (1997) 1422.
[2] SUN, W.; KONG, J.; DENG, J. Electroanalysis. 9 (1997) 115.
[ 3] PEIXOTO, C.R.M.; KUBOTA, L.T.; GUSHIKEM, Y. Anal. Comm. 32 (1995) 503.
[4] LAVIRON, E. J. Electroanal. Chem., 101 (1979) 19.
[5] SUN, W.; KONG, J.; DENG, J. Anal. Lett., 29 (1996)2425.
FAPESP