Elias Alves Severino (PG) e Carlos Roque Duarte Correia (PQ)
palavras–chaves: enecarbamato, reação de Heck, estereosseletividade

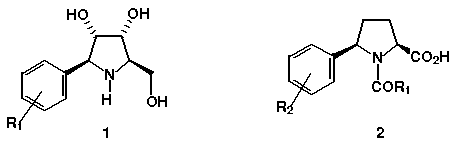
Visando a síntese de 1 e 2, um estudo envolvendo arilação de enecarbamatos endocíclicos enantiomericamente puros (EEEP) derivados de sistemas pirrolidínicos foi executado visando avaliar a seletividade facial quando um centro estereogênico está presente na posição 5.
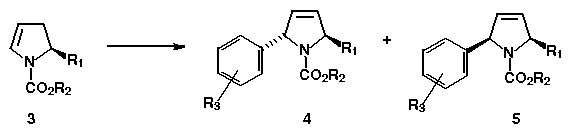
Pelo método A – Esquema 1 – foram obtidos bons rendimentos (79-95%) quando a relação enecarbamato e sal de diazônio foi de 2:1. A seletividade facial – Tabela 1 – é influenciada pelo substituinte em C-5 sendo o isômero trans formado preferencialmente em diferentes proporções. Entretanto, quando o substituinte é hidroximetila (3c) a seletividade se inverte, formando preferencialmente o isômero cis.
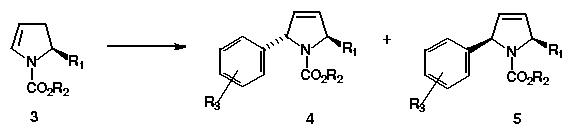
Tabela – Estereosseletividade na Reação de Heck com Pd(OAc)2
EEEP |
R1 |
R2 |
Trans:Cis3aCO2MeMe63:373bCO2t-But-Bu>95:053cCH2OHt-Bu25:753dCH2OTBDPSt-Bu76:243eCH2OTBDPSMe82:183fCH2OtrMe88:12 Pelo método B – Esquema 2 – foi possível obter a mesma seletividade com a vantagem de se utilizar temperatura mais baixa (t.a.), menor quantidade de catalisador e menor relação enecarbamato e sal de diazônio – Tabela 2.
|
|||
|
|
|
|
|
|||
|
|
|
|
|
|||
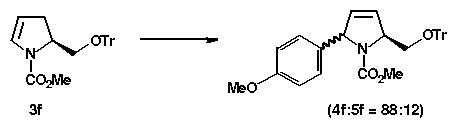
Tabela 2 – Reação de Heck com Pd2(dba)3
|
Enec.:Diaz. |
% mol Pd2(dba)3 |
Tempo |
Rend. (%)1:10,55 h211:11,01 h731:12,025 min831:1,51,040 min852:11,030 min95Conclusão: A reação de Heck de EEEPs 3a-f e sais de diazônio foi obtida com bons rendimentos em condições suaves, baixa quantidade de catalisador de Pd e menor relação enecarbamato e sal de diazônio. O substituinte em C-5 permite o controle estereoquímico em C-2 fornececendo o isômero cis ou trans com alta seletividade.
|
||
|
|
|
|
|
||
|
|
|
|
|
||
Oliveira, D.F.; Severino, E.A.; Correia, C.R.D.; Tetrahedron Lett. 1999, 40, 2083.
Makino, K.; Ichikawa, Y.; Tetrahedron Lett. 1998, 39, 8245 e ref. citadas.
Zaluski, M.C.F.; Coric, P.; Thery, V.; Gonzalez, V.; Meudal, H.; Turcaud, S.; Michel, J.P.; Roques, B.P.; J. Med. Chem. 1996, 39, 2594.
CNPq, FAPESP