USO DO FORNO DE MICROONDAS EM SÍNTESE
ORGÂNICA: PREPARAÇÃO DE AMIDAS
Giselle
Cerchiaro (PG), Juliana Baracat (IC), Lúcia Helena Brito
Baptistella* (PQ)
Departamento
de Química Orgânica, Instituto de Química,
Universidade Estadual de Campinas, Campinas - SP
Palavras chave: reações em microondas, preparação
de amidas, ácido quínico
Os
açúcares superiores, ou seja, aqueles com mais de 6
átomos de C na cadeia, tornaram-se alvo de grande interesse
devido principalmente aos seus papeis proeminentes em sistemas
biológicos. Além disso, são moléculas que
apresentam vários centros assimétricos contíguos,
o que representa um grande desafio aos químicos orgânicos
sintéticos.

Como
a biodisponibilidade dos açúcares superiores é
bastante limitada, busca-se uma rota sintética versátil
e barata para a síntese de um intermediário que possa
ser útil tanto para a obtenção desses
carboidratos quanto para de análogos com interesse biológico.
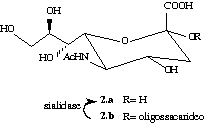
Um intermediário desse tipo pode ser a heptose 1,
adequada à síntese do ácido N-acetilneuramínico
2a, normalmente utilizado para a preparação de
potenciais inibidores da sialidase do vírus da gripe 1 ,
2 .
Usa-se
como material de partida nestas sequencias sintéticas o ácido
(3R,5R)-(-)-quínico 3, 3 um carbociclo
polioxigenado oticamente ativo, disponível comercialmente.
Fez-se
um estudo das primeiras etapas desta sequência, que consta da
proteção das hidroxilas em C3 e C4 de 3, e em
seguida a abertura do anel lactona formado entre oo grupos presentes
em C1 e o C5. Esta reação em 4 é
tradicionalmente feita com um alcoolato, numa etapa de
transesterificação, mas é geralmente
problemática. Preparações de amidas então
foram testadas, pois levariam a derivados mais estáveis destes
ácidos. Estudou-se também a reação de
formação de amida diretamente a partir de 3, sem
este passar pela lactona.

Legenda:
(a) acetona, H2SO4(cat.), Na2SO4,
refl., 2h, rdto quantitativo; (b) 4, 5 N,N-dimetilamina em
THF, THF ou clorobenzeno, refluxo, MP recuperado; (c)
diisobutilamina, THF, refl., MP recuperado; (d)6
benzilamina, AlMe3/tolueno 2M, CH2Cl2,
refl., MP recuperado; (e) benzilamina, clorobenzeno, refl., 48h, 20%
de 5b; (f) benzilamina, microondas P=700W, 1min/100mg, 90% de
5b; (g) dimetilamina sol. aq., microondas P=700W, 3min./100mg,
30% de 5a; (h) ciclohexilamina, microondas P=700W, 15min./1g,
rdto quantitativo de 5c; (i) ciclohexilamina, microondas
P=700W, água, 8min./100mg, 70% de 6.
Nestas
reações para formação de amidas, os
esforços foram dirigidos à utilização de
energia de microondas, já que os compostos utilizados possuíam
dipolos elétricos necessários à sua absorção.
Comparativamente às reações tradicionais (etapas
b, c, d, e), as realizadas em microondas foram extremamente mais
rápidas e os produtos foram isolados em altos rendimentos
(etapas f, g, h). No caso de reações feitas diretamente
sobre os ácidos carboxílicos (exemplificado pela etapa
i), a desidratação dos sais intermediários
formados exigiu mais tempo, no entanto as amidas puderam ser isoladas
em bons rendimentos.
Em
todos os casos as amidas podem ser utilizadas em quantidades
equimolares e não existe a necessidade de solvente, tornando a
metodologia bastante atrativa e com um grande interesse como reação
menos poluente ao meio ambiente. (CNPq)
Bibliografia:
DeNinno,
M., Synthesis, 5583 (1991)
Rohloff,
J.C.; Kent, M.K.; Postich, M.J. et al; J. Org. Chem., 63,
4545 (1998)
Barco,
A.; Benetti, S.; DeRisi, C. et al; Tetrahedron-Asymmetry, 8,
3515 (1997)
Zaugg,
H.E.; Horrow, B.W.; J. Am. Chem. Soc., 72, 3004 (1950)
Trost,
B.M.; Romero, A; J. Org. Chem., 51, 2332 (1986)
Basha,
A; Lipton, M.; Weinreb, S.M.; Tetrahedron Lett., 48,
4171 (1977)


