RESULTADOS PRELIMINARES NA SÍNTESE DE UM INTERMEDIÁRIO PARA O ESTUDO DA REGIOSSELETIVIDADE NA PREPARAÇÃO DE UM ANEL FENANTRIDÔNICO
Nader de Sousa Amadeu (IC) e Fernando Coelho (PQ)‡
‡ Depto de Química Orgânica – IQ – UNICAMP – 13083-970 – Campinas, SP
palavras-chave: Regiosseletividade, ciclização, fenantridona
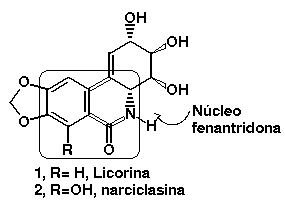
Introdução e Objetivos: O núcleo fenantridona está presente na estrutura de várias substâncias de origem natural, notadamente em alcalóides encontrados em plantas da família das Amarillydaceae (Figura 1). Esses alcalóides apresentam elevada atividade antitumoral

 O
anel fenantridona pode ser facilmente preparado a partir de uma
reação de ciclização intramolecular de um
carbamato, entretanto existem problemas relacionados a
regiosseletividade da ciclização, de acordo com o
mostrado no esquema 1.
O
anel fenantridona pode ser facilmente preparado a partir de uma
reação de ciclização intramolecular de um
carbamato, entretanto existem problemas relacionados a
regiosseletividade da ciclização, de acordo com o
mostrado no esquema 1.
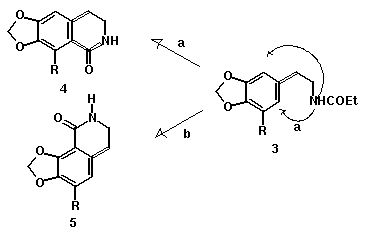
Em um trabalho que visa utilizar adutos de Baylis-Hillman como material de partida para a síntese de alcalóides de Amarillydaceae, era necessário estudar a etapa de ciclização visando a preparação do núcleo fenantridona presente nesses alcalóides (figura 1). Nesse trabalho apresentamos os resultados preliminares de uma estratégia sintética, que visa preparar um modelo que nos permita avaliar preliminarmente o nível de regiosseletividade alcançado (4 versus 5).
Resultados e Discussão: O aldeído 6 foi preparado em três etapas, a partir da vanilina comercial, de acordo com a metodologia mostrada abaixo1.
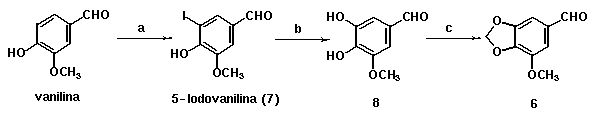
Reagentes e condições: a. ICl, HCl, H2O, t.a., 4 dias, 64%; b. NaOH 40%, CuSO4, 12h, refluxo, DMF, 88%; c. CH2Cl2, KF, DMF, 50%.
O aldeído 6 foi então submetido a uma sequência de etapas, de maneira a homologar uma unidade de carbono. Assim redução e mesilação, seguida de substituição por cianeto forneceu a nitrila 11, que em seguida foi reduzida para fornecer a amina 12. A partir da amina 12 uma reação com cloroformiato de etila deve fornecer o intermediário necessário à etapa de ciclização (3).
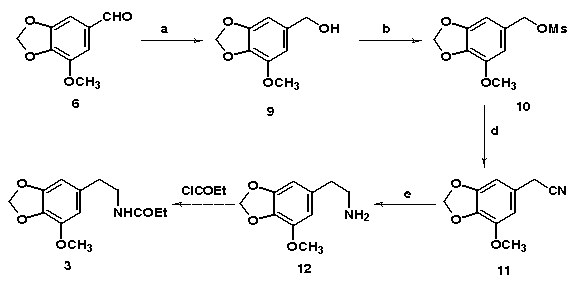
Reagentes e condições: a. NaBH4, EtOH, t.a., 3h, 85%; b. MsCl, Py, t.a., 12h, 50%; c. NaCN, DMF, t.a., 93%; d. LiAlH4, THF, 80%.
Os resultados dessa ciclização serão utilizados em nosso laboratório em outros trabalhos que visam a preparação de intermediários-chave para a síntese total de alcalóides com atividade antitumoral, a partir de adutos de Baylis-Hillman.
Referência: 1. Nishinaga, A. ; Matsuura, T., J. Organic Chem., 1964, 29, 1812.
[CNPQ, FAPESP]