


1902
1936
2040
2090
2141
2115




421
521
624
338
PAPEL DA CISTEÍNA E DO ASCORBATO NA LIBERAÇÃO DE ÓXIDO NÍTRICO A PARTIR DO NITROPRUSSIATO DE SÓDIO
Amarildo Grando (IC), Sílvia Mika Shishido (PG), Marcelo G. de Oliveira (PQ)
Palavras-chave: nitroprussiato de sódio, óxido nítrico, cisteína
O pentacianonitrosilferrato de sódio ou nitroprussiato de sódio (NPS), Na2[Fe(CN)5(NO)]), vem sendo utilizado a mais de 40 anos como vasodilatador, para o controle da pressão sanguínea em tratamentos pós-operatórios e no tratamento de hipertenção crônica.
Atualmente, sabe-se que a ação do NPS é baseada na produção e liberação de Óxido Nítrico (NO), de forma semelhante à ação dos nitratos orgânicos. Alguns autores acreditam que o mecanismo de liberação de NO do NPS envolve uma transferência de elétron ao ligante NO+, a partir de uma outra molécula, levando à redução do ânion nitroprussiato. Estas observações têm aumentado o interesse nas reações do NPS com certos agentes redutores como os tióis ou hemoproteínas, pois acredita-se que estes agentes redutores podem ser os responsáveis pelo transporte e liberação do NO in vivo.
Neste trabalho foi verificada a reatividade do NPS em relação ao grupo sulfidrila (SH) da L-Cis, e em relação ao ácido ascórico (H2A).
As reações de redução do NPS pela L–Cis e pelo H2A foram acompanhadas através da análise das variações espectrais nas regiões do UV/vis e do IV. Procurou-se associar os produtos formados às bandas presentes nestas duas regiões, bem como estabelecer uma via de reação que levasse aos produtos. As soluções de NPS e Cis foram preparadas em água e em solução tampão de fosfato (pH 7,4), sendo as concentrações calculadas em % em massa. Soluções não tamponadas foram preparadas em água deionizada. As caracterizações espectroscópicas das reações do NPS com a Cis e com o H2A na região do UV/Vis foram feitas utilizando-se um espectrofotômetro com arranjo de diodos (HP modelo 8453). Foram utilizadas cubetas de quartzo (L = 1 cm) e soluções de Cis 0,3 %. Os espectros no IV foram obtidos utilizando-se um espectrofotômetro FTIR (Nicolet – modelo 502) com filmes capilares das soluções em janelas de CaF2, sendo os espectros coletados em intervalos de 30 s. As reações do NPS com o H2A foram acompanhadas através de misturas equimolares dos reagentes cujas concentrações variaram na faixa de 1 - 6 % para as análises no UV/vis e IV.
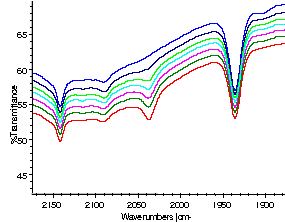
As figuras 1 e 2 mostram as variações espectrais no IV e UV/vis para a reação do NPS com a Cis em solução tamponadas.
1902 1936 2040 2090 2141 2115 421 521 624 338

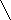







Figura 1: NPS-CySH em solução tampão Figura 2: UV-vis NPS-CySH em solução tampão
As bandas fracas que aparecem em 1902 cm-1 e 521 nm foram atribuídas à formação de um intermediário de coloração vermelha, de acordo com a reação:
 [Fe(CN)5(NO)]2-
+ RS- [Fe(CN)5N(O)SR]3-
[Fe(CN)5(NO)]2-
+ RS- [Fe(CN)5N(O)SR]3-
O aparecimento das bandas em 338 nm e 2040 cm-1 foi associado à formação de produtos contendo íons Fe(II), ([FeII(CN)5-x(H2O)x](3-x)-). As bandas em 421 nm e 2115 cm-1 foram associadas à formação de espécies contendo o íon Fe(III) ([FeIII(CN)5-x(H2O)x](2-x)-). Por fim as bandas em 624 nm e 2090 cm-1 foram associadas à formação de azul da prússia (Fe4III[FeII(CN)6]3). Observou-se também a formação do dímero da cisteína (cistina) através da detecção da bandas em 452 cm-1 e 540 cm-1, características da vibração de estiramento S – S.
Na reação de redução do NPS pelo H2A observou-se o desenvolvimento de uma coloração azul que foi atribuída à formação de um aduto intermediário que apresenta uma banda em 610 nm no espectro UV/vis. A formação deste aduto foi observada apenas em pH maior que 4. Os produtos desta reação apresentam bandas em 2115, 2088 e 2040 cm-1 indicando a formação de espécies contendo íons Fe (II) e Fe (III).
A identificação de espécies instáveis associadas às bandas em 521 nm e 608 nm para as reações do NPS com a Cis e o H2A, respectivamente, comprova os estudos que afirmam que a primeira etapa das reações do NPS com agentes redutores envolve a formação de um aduto intermediário. Consequentemente estes resultados indicam que tanto grupos SH de aminoácidos como o ascorbato, presentes no plasma, podem desempenhar um papel fundamental liberação de ·NO de NPS através da formação de adutos que levam à redução do NO+.
Bates, J.N.; Baker, M.T.; Guerra Jr, R.; Harrison, D.G., Nitric oxide generation from nitroprusside by vascular tissue – Evidence that reduction of the nitroprusside anion and cyanide loss are required. Biochem. Pharmachol., (1991) 42, S157-S-165.
![]()
