EPOXIDAÇÃO
DE CICLOOCTENO CATALISADA POR ÓXIDOS MISTOS DE Ti, Zr, Al e
Si.
Leandro
Martínez1 (IC), Robson F. de Farias2 (PQ),
Ulrich Arnold1 (PG), Ulf Schuchardt1 (PQ),
Claudio Airoldi1 (PQ)
1Instituto
de Química, Unicamp.
2Departamento
de Química, Universidade Federal de Roraima.
Palavras-chave:
epoxidação, oxidos mistos, catálise.
A
atividade catalítica de óxidos mistos de silício,
titânio e alumínio em reações de oxidação
de alcenos vem sendo extensivamente estudada [1-3]. Sua importância
provém da alta seletividade da catálise e da facilidade
com que os catalisadores podem ser recuperados. Algumas pesquisas
comparam a eficiência da conversão dos alcenos de acordo
com o oxidante [2], com o teor de titânio no óxido [1] e
com a estrutura dos materiais [1]. Nesta comunicação
comparam-se seis diferentes óxidos mistos de titânio,
zircônio, alumínio e silício em composições
1:1.

Figura
1: Reação de epoxidação de ciclocteno
Os
óxidos foram preparados via processo sol-gel a partir dos
alcóxidos dos respectivos metais [5,6]. Dissolveu-se
1,12-diaminododecano em etanol, adicionando-se em seguida os
alcóxidos e água na proporção desejada.
Os óxidos obtidos foram secos e calcinados a 700oC
para eliminação da diamina. Para os testes catalíticos
foram utilizados 10,0 mmoles de cicloocteno misturados a 15,0 mmoles
de tert-butil hidroperóxido (TBHP) de uma solução
88,0% em ciclohexano. Foram utilizados 50 mg de catalisador e a
reação foi feita a 80oC. Os materiais
preparados foram alumina (Al), óxido misto de alumínio
e silício 1:1 (Al/Si), zircônio e alumínio 1:1
(Zr/Al), zircônio e titânio 1:1 (Zr/Ti), titânio e
alumínio 1:1 (Ti/Al) e titânio e silício 1:1
(Ti/Si). Os materiais foram caracterizados por epectroscopia no IV e
por difração de raios X, sendo todos amorfos.
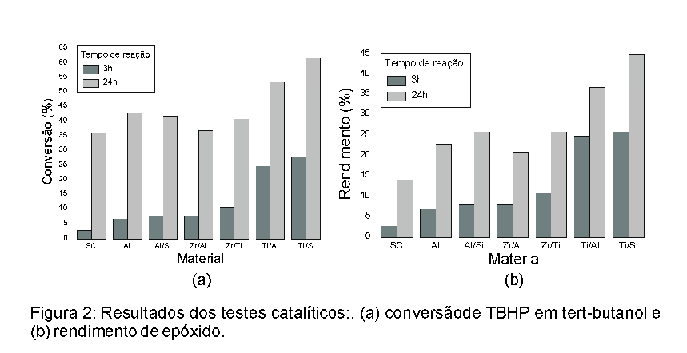
A
reação de epoxidação está
representada na figura 1, e os resultados estão apresentados
na figura 2. A conversão indica a porcentagem de consumo de
TBHP e o rendimento o porcentual de epóxido formado em relação
ao total de cicloocteno no meio reacional. A barra SC corresponde à
reação sem catalisador.
Os
resultados mostram que todos os materiais são ativos
cataliticamente, uma vez que a conversão de TBHP em
tert-butanol, para a alumina, o menos ativo, foi de 7,0% em 3 h de
reação, enquanto sem o catalisador a conversão é
de apenas 3%. Os materiais mais ativos são aqueles que contém
titânio, sendo que o para o material Ti/Si a conversão
foi de 28,0%, valor superior ao 23,5% descrito para a epoxidação
de 1-hexeno sob condições semelhantes [1]. A alumina
apresenta uma atividade catalítica comparativamente grande,
enquanto o óxido de zircônio é o menos ativo dos
óxidos estudados, apesar do zircônio formar complexos
ativos na polimerização de alcenos.
Hutter
et al. propuseram que nos óxidos mistos de Ti-Si há
microestruturas de titânia e átomos de titânio
isolados. Os átomos de titânio isolados são os
sítios cataliticamente mais ativos [4]. Isto pode explicar, de
certa forma, a menor atividade do óxido Ti/Al em relação
ao Ti/Si, sendo que o alumínio é mais ativo que o
silício. Sendo o alumínio trivalente, provoca uma maior
concentração de microestruturas de titânia no
óxido Ti/Al do que no Ti/Si, já que tanto o silício
como o titânio são tetravalentes e seus óxidos
estruturalmente semelhantes.
 A
figura 3 mostra a relação entre rendimento de epóxido
e conversão de TBHP. Ela indica a seletividade da reação,
sendo a seletividade máxima indicada pela reta R = C.
Nota-se que a seletividade de todos os materiais é bastante
alta nas 3 primeiras horas de reação, caindo muito após
24h. Neste tempo, material que apresenta maior seletividade é
o Ti/Si, com STi/Si = 73% e a reação
sem catalisador é a menos seletiva sendo Ssc
= 39%. Todos os óxidos aumentaram a seletividade da reação.
A
figura 3 mostra a relação entre rendimento de epóxido
e conversão de TBHP. Ela indica a seletividade da reação,
sendo a seletividade máxima indicada pela reta R = C.
Nota-se que a seletividade de todos os materiais é bastante
alta nas 3 primeiras horas de reação, caindo muito após
24h. Neste tempo, material que apresenta maior seletividade é
o Ti/Si, com STi/Si = 73% e a reação
sem catalisador é a menos seletiva sendo Ssc
= 39%. Todos os óxidos aumentaram a seletividade da reação.
[1]
Z. Liu, G. M. Crumbaugh, R. J. Davis, J. Catal. 159(1996)83 [2] K.U.
Ingold, D. W. Snelgrove, P.A. MacFaoul, R.D. Oldroyd, J.M. Thomas,
Catal. Lett. 48(1997)21. [3] R. Neumann, M. Levin-Elad, J. Catal.
166(1997)206. [4] R. Hutter, T. Mallat, A. Baiker, J. Catal.
153(1995)177. [4] R. F. de Farias, C. Airoldi, J. Colloid Interf.
Sci, no prelo. [5] R. F. de Farias, C. Airoldi, J. Solid State Chem.,
no prelo.
CAPES-PICDT,
CNPq, FAPESP


 A
figura 3 mostra a relação entre rendimento de epóxido
e conversão de TBHP. Ela indica a seletividade da reação,
sendo a seletividade máxima indicada pela reta R = C.
Nota-se que a seletividade de todos os materiais é bastante
alta nas 3 primeiras horas de reação, caindo muito após
24h. Neste tempo, material que apresenta maior seletividade é
o Ti/Si, com STi/Si = 73% e a reação
sem catalisador é a menos seletiva sendo Ssc
= 39%. Todos os óxidos aumentaram a seletividade da reação.
A
figura 3 mostra a relação entre rendimento de epóxido
e conversão de TBHP. Ela indica a seletividade da reação,
sendo a seletividade máxima indicada pela reta R = C.
Nota-se que a seletividade de todos os materiais é bastante
alta nas 3 primeiras horas de reação, caindo muito após
24h. Neste tempo, material que apresenta maior seletividade é
o Ti/Si, com STi/Si = 73% e a reação
sem catalisador é a menos seletiva sendo Ssc
= 39%. Todos os óxidos aumentaram a seletividade da reação.