CALIXARENOS-AMINOÁCIDOS: EXTRAÇÃO DE CÁTIONS ALCALINOS
Márcio Lazzarottoa (PQ), Patrícia Los Weinerta (IC), Francine Furtado Nachtigalla (PQ) e Faruk Nomeb (PQ).
a)Departamento de Química, Universidade Estadual de Ponta Grossa, Praça Santos Andrade, s/n, CEP 84010-000, Ponta Grossa- PR.
b)Departamento de Química- Universidade Federal de Santa Catarina, Campus Universitário, Trindade, 88040-900, Florianópolis-SC.
palavras-chave: calixarenos, química supramolecular, extração de metais.
Os calixarenos1 são moléculas utilizadas como plataformas para a síntese de receptores, visando estudos de reconhecimento molecular e Química Supramolecular. As propriedades dos alcoxi-carboxi-metoxi-para-terc-butilcalix[4] arenos (1) como agentes extratores de cátions alcalinos são conhecidas,2 com seletividade para o íon sódio.
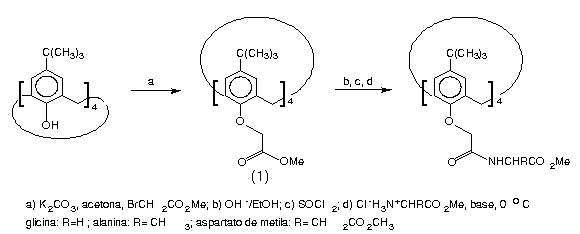
Neste trabalho, foram sintetizadas amidas de aminoácidos análogas a (1), seguindo a rota descrita abaixo:

Inicialmente, o para-terc-butilcalix[4]areno reage com o bromoacetato de metila em K2CO3/acetona, fornecendo apenas o produto tetrassubstituído na conformação cone. Após a hidrólise alcalina dos grupos éster, procedeu-se a formação do tetracloreto de ácido em SOCl2. Finalmente, foram realizadas as reações com os cloridratos dos ésteres metílicos dos aminoácidos (glicina, L-alanina e L-aspartato de metila), com a liberação da amina “in situ”, usando Et3N. Os produtos foram obtidos em rendimentos razoáveis (40-60 %) e isolados após recristalização em MeOH/H2O. A caracterização foi feita por espectroscopia de IV e RMN.
Os experimentos de extração foram realizados de água para clorofórmio, mediante a complexação dos metais pelos derivados de calixareno com glicina e aspartato de metila dissolvidos no clorofórmio; medindo-se a absorbância do picrato do metal alcalino (M+Pic-; M= Na, K, Rb, Cs; Pic-= 2,4,6 trinitrofenol) na fase orgânica. Considerando o equilíbrio abaixo, tem-se a seguinte equação para a constante de extração, Kext:
![]() ;
;
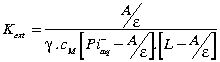
Onde
A corresponde ao valor da absorbância do picrato na fase
orgânica ,e=15000;
g
é o valor do coeficiente de atividade do íon metálico
na fase aquosa, calculado pela equação de Debye-Hückel;
cM= 10-2 mol.L-1,
![]() é a concentração de picrato, e L é
a concentração do calixareno usado como ligante
adicionada. Com os valores de Kext
obtidos foram construídos os gráficos abaixo:
é a concentração de picrato, e L é
a concentração do calixareno usado como ligante
adicionada. Com os valores de Kext
obtidos foram construídos os gráficos abaixo:
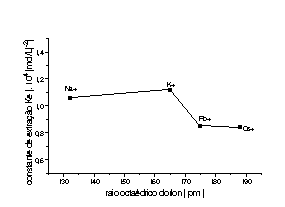
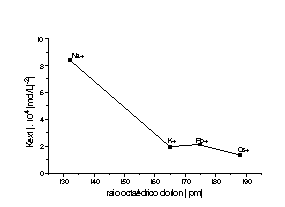
Gráficos de valores de constante de extração (Kext ) vs. raio iônico (N. C.= 8) para a extração de metais alcalinos com o para-terc-butilcalix[4]-glicinato de metila (esquerda) e para-terc-butilcalix[4]-L-aspartato de metila (direita).
A análise dos dados de extração leva às seguintes conclusões: a) o grau de extração usando estas amidas é bastante inferior àqueles obtidos para os ésteres, provavelmente devido à formação de ligações de hidrogênio intramoleculares N-H - - O=C, que diminuem a disponibilidade dos elétrons dos oxigênios na complexação do metal, b) o derivado com aspartato de metila apresenta seletividade para sódio, em relação aos outros metais. Este efeito pode ser atribuído a dois fatores: o sódio é complexado pelos oxigênios dos resíduos de aspartato, ou os oxigênios dos grupos éster g dos aspartatos fazem ligações de hidrogênio com os N-H, liberando os oxigênios do grupo OCH2C=O para complexar o íon sódio.
Concluindo, os receptores sintetizados são menos eficientes na extração de íons de metais alcalinos, e o derivado com aspartato apresenta seletividade para íon sódio.
Agradecimentos : CAPES, CNPq, PRONEX.
Revisão: Ikeda, A.; Shinkai, S. Chem. Rev. 1997; 97, 1713.
Chang, S.; Cho, I.; Chem. Lett. 1988, 477.