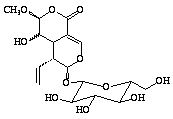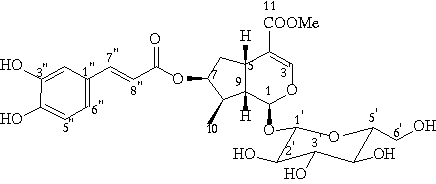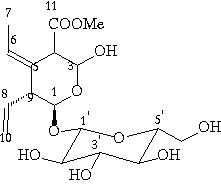
Chioccoca alba Hitch. (Rubiaceae) é uma planta arbustiva endêmica a várias regiões do continente americano e utilizada na medicina popular como tônico, diurético e nos processos inflamatórios em geral. As raízes desta espécie também são utilizadas como antiviral, antiedema e no tratamento de picadas de cobras1, 2. As ações farmacológicas das raízes de C. alba estão descritas nas Farmacopéias de várias nações européias desde o século passado3. Trabalhos anteriores sobre C. alba descrevem a ocorrência de lignanas e cumarinas4, triterpenos3, ceto-álcoois5, iridóides e seco-iridóides6. A fração n-butanólica obtida da partição do extrato CH2Cl2/MeOH das raízes de C. alba foi submetida a uma coluna filtrante a vácuo utilizando soluções de CHCl3 e MeOH em gradiente de polaridade crescente. Este processo forneceu um total de 10 frações. A fração 2 foi submetida a filtração em gel utilizando-se Sephadex LH-20 e metanol como eluente, originando 21 frações, as quais foram denominadas F-1 a F-21. As frações F-17 e F-18 foram reunidas e fracionadas em coluna de sílica "flash" utilizando-se uma solução de CHCl3/MeOH/H2O/HOAc (80:18:2:0,5) como sistema de eluição. A fração 25 resultante deste procedimento foi purificada via CLAE fornecendo o iridóide 1. A fração F-15 foi submetida a um procedimento análogo ao descrito para as frações F-17 – F-18, originando 29 frações. As frações 5 e 21 foram purificadas via CLAE fornecendo os seco-iridóides 2 e 3, respectivamente. Os dados espectrométricos de RMN de 1H de 1 e 3 sugeriram a presença de substâncias da classe dos iridóides devido aos singletos em 7,14 d e 7,46 d, respectivamente, característicos do H-3 do núcleo carbocíclico, confirmado pelos sinais do espectro de RMN de 13C em 154,20 e 150,5 d, respectivamente. Esses sinais correspondem aos carbonos metínicos C-3 e que analisados juntamente com os sinais em 109.3 e 111.2 d, correspondentes ao C-4 quaternário, respectivamente, caracterizam a estrutura da maioria dos iridóides. Através dos dados dos espectros de RMN de 1H e de 13C foi possível observar também que as substâncias 1 e 3 apresentaram características distintas; a principal delas devido aos sinais correspondentes a uma ligação dupla terminal 132.6 d e 119.2 d no iridóide 3, ausente no iridóide 1, atribuído aos C-8 e C-10 respectivamente. A ligação dupla terminal resultante da quebra oxidativa entre C-7 e C-8 de um esqueleto iridoidal é uma feição típica dos seco-iridóides. A constatação de sinais correspondentes a hidrogênios anoméricos em 4,6 d (d, J = 8,0 Hz) e hidrogênios hidroximetínicos na região de 3,0 - 4,0 d indicaram a presença das unidades glicosídicas em 1 e 3. A análise dos dados de RMN de 1H e de 13C de 1 permitiu inferir também a presença de uma unidade cafeoíla, a qual foi confirmada pelo padrão de multiplicidade desse sistema. Análise cuidadosa dos dados de 1, aliados aos registrados para substâncias análogas isoladas de C. alba6, permitiu estabelecer a estrutura desse iridóide como sendo 7-cafeoil-loganina. O esqueleto seco-iridóidal para a substância 3 foi corroborado pela análise dos demais sinais, principalmente devido ao aparecimento de um terceiro sinal na região de carbono hemicetálico, em 101,5 d atribuído ao C-7. A configuração do carbono hidroximetínico C-6 não pode ser determinada ainda, devido a complexidade e sobreposição de sinais na região compreendida entre 4,50 e 3,70 d, necessitando de experimentos adicionais de RMN de 1H. Os dados espectrais aliados às informações bibliográficas para seco-iridóides relacionados permitiram propor a estrutura 3 para o iridóide em discussão. A substância 2 também apresentou feições espectrais típicas de um seco-iridóide. As principais diferenças observadas nesta substância devem-se à ausência do sinal em torno de 7,34 d, típico do H-3 dos iridóides carbocíclicos e ao aparecimento de uma ligação dupla adicional (C = 135.2 e CH = 122.1 d) àquela registrada para o C8-C10 (132.6 e 119.8 d). Pelo HETCOR o dubleto em 5,7 d ( H-3, J = 8.9 Hz) corresponde ao hidrogênio ligado ao carbono responsável pelo sinal em 90.7 d no espectro de RMN de 13C e que foram fundamentais para estabelecer esta proposição estrutural. O iridóide 7-cafeoil-loganina é novo no gênero, entretanto, para confirmar se a estrutura 1 é de fato inédita, um levantamento bibliográfico está sendo realizado. Os seco-iridóides são inéditos.