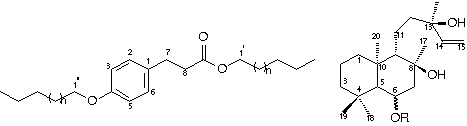
O extrato etanólico foi dissolvido em MeOH/H2O (80:20) e em seguida extraído com hexano, CH2Cl2, AcOEt e n-BuOH resultando nas respectivas frações hexânica, diclorometânica, acetato de etila, n-butanólica e aquosa. Todos as frações foram submetidas ao teste de atividade antimicrobiana utilizando os microorganismos descritos. Com halos de inibição variando na faixa de 10 a 25 mm, as frações de baixa polaridade mostraram inibição moderada e não seletiva dos microorganismos teste, enquanto que as frações mais polares inibiram as bactérias Gram-positivas. 1,0 g da fração hexânica foi submetida a uma coluna de sílica "Flash" eluída com hexano/AcOEt em gradiente, obtendo-se 25 subfrações, estando a atividade antimicrobiana concentrada nas subfrações eluídas com hexano/AcOEt 9:1 e 8,5:1.5. Purificação dessas subfrações conduziram ao isolamento da substância aromática 1, sitosterol e stigmasterol. A fração aquosa, fortemente bactericida, foi submetida a cromatografia em coluna utilizando-se XAD-16 como suporte e H2O, H2O:MeOH (80:20, 60:40, 40:60 e 20:80), MeOH, MeOH:CH2Cl2 (50:50) e CH2Cl2. A ultima fração dessa coluna foi posteriormente purificada fornecendo os diterpenos labdânicos 2-4, dentre eles o diterpeno 2 mostrou forte ação inibitória frente as bactérias Gram-positivas e álcool ácido resistente (Tabela 1). Os espectros de RMN de 1H e COSY 1H-1H obtidos para 1 indicaram a presença de um anel aromático 1,4 dissubstituído, identificados pelos dubletos em 7,07 d ( d, J = 8,0 Hz) e 6,76 d (d, J = 8,0 Hz). Foi possível observar também o acoplamento dos sinais em 4.20 d (t, J = 7,1 Hz) com os sinais em 2,85 d (t, J = 7,1 Hz); dois sinais correspondentes a dois grupos metílicos terminais acoplando com dois multipletos em torno de 1,55 d. O espectro de RMN de 13C confirmou o sistema aromático e indicou a presença de um grupo carbonílico (173,9), dois carbonos hidroximetilênicos (64,94 e 63,15), vários sinais em torno de 29,37 e dois sinais em 14.12 e 13.9 indicativos de metila terminal. Análise dos dados espectrais sugerem a estrutura 1 para a substância em questão. Hidrólise e massa de alta resolução estão sendo providenciados para a confirmação da substância 1 que apresentou bioatividade moderada. Os diterpenos 2-4 apresentaram feições espectrais muito similares: Os sinais em 5,84 d (1H, dd, J = 17, 0; 3,0; 10,7), 5,13 d (1H, dd, J = 17,0; 3,0) e 4,89 d (1H, dd, J = 10,7) analisados juntamente com os sinais em 147,5 d (CH), 110,9 d (CH2), 73,7 d (C) e 29,3 d (CH3) observados no espectro de RMN de 13C indicaram a mesma cadeia lateral para os três diterpenos. Os sinais em torno de 72, 4 d (C-6) e 74,3 d (C-8) também são feições comuns as substâncias em análise. As diferenças observadas nas estruturas em discussão devem-se aos substituintes que estão esterificando o grupo hidroxílico em C-6. Análise detalhada de todos os dados espectrais conduziram as propostas estruturais 2-4 para os diterpenos. A determinação da configuração relativa do C-6 ainda carece de dados adicionais.