ANÁLISE QUANTITATIVA DE METABÓLITOS SECUNDÁRIOS DERIVADOS DO ESQUELETO FRIEDO-NOR-OLEANANO EM VARIEDADES MORFOLÓGICAS DE MAYTENUS ILICIFOLIA (CELASTRACEAE), POR CROMATOGRAFIA LÍQUIDA DE ALTA EFICIÊNCIA (CLAE).
Waldemar Buffa Filho (PG)1, Joaquim Corsino (PG)1, Alberto Camilo Alécio (PG)1, Ana Maria Soares Pereira (PQ)2, Suzelei Castro França (PQ)2, Vanderlan da Silva Bolzani (PQ)1 e Maysa Furlan (PQ)1
1 NuBBE - Núcleo de Bioensaio, Biossíntese e Ecofisiologia de Produtos Naturais, Departamento de Química Orgânica, Instituto de Química, Universidade Estadual Paulista, Araraquara, São Paulo, Brasil, 2 Departamento de Biotecnologia Vegetal, Universidade de Ribeirão Preto, Ribeirão Preto, São Paulo, Brasil
Palavras chave: Maytenus ilicifolia; variedades morfológicas; CLAE
Espécies da família Celastraceae e Hippocrateaceae tem mostrado o acumulo de um grupo particular de triterpenos insaturados, derivados do esqueleto friedo-nor-oleanano, com marcada atividade biológica [1-4]. Estes triterpenos, denominados de quinonametídeos, já foram submetidos a testes clínicos envolvendo pacientes com diferentes tipos de neoplasias [5]. Os resultados obtidos mostraram efetiva atividade in vivo de algumas substâncias em diferentes tipos de carcinomas, tais como epidermóide, do estômago e do sistema linfático. A espécie Maytenus ilicifolia (Celastraceae), conhecida popularmente como espinheira santa, apresenta sete especimens com variações morfológicas intrigantes. Estas particularidades morfológicas estão relacionadas as quantidades de espinhos presentes em suas folhas, espinhos estes que são responsáveis pela sua denominação popular. Como parte do estudo biossintético dos triterpenos quinonametídeos, análise química dos extratos hexânicos das raízes dos diferentes especimens, via CLAE, foi realizada a fim de verificar se o perfil dos triterpenos quinonametídeos se mantinham constantes. O material vegetal, de mesma faixa etária, foi coletado na fazenda experimental da UNAERP, em Ribeirão Preto, SP. O isolamento dos padrões a serem utilizados nas análises por CLAE, de cinco das sete variedades morfológicas, foi realizado utilizando-se métodos cromatográficos convencionais tais como, cromatografia em coluna e cromatografia em camada delgada preparativa. As condições cromatográficas de análise por CLAE foram estabelecidas utilizando-se coluna de RF (C18), fase móvel MeOH:H2O (8:2) (1% H3PO4) e fluxo de 1mL/min. Os cromatogramas foram obtidos utilizando-se detector Diode-Array a 420 nm e nestas condições maitenina (1), 22b-hidroximaitenina (2), 20a-hidroximaitenina (3), celastrol (4) e pristimerina (5) apresentaram tr de cerca de 7,015; 5,407; 4,514; 17,243 e 25,901 min., respectivamente. As curvas de calibração, dos padrões utilizados, foram preparadas a partir de soluções de diferentes concentrações 100, 50, 25 e 12,5 ppm e quando necessário foram feitas novas diluições; 40, 30, 20, 10, 5 e 2,5 ppm, a fim de poderem ser quantificados aqueles metabólitos que se apresentavam em concentrações menores. Através do tratamento gráfico foram obtidos os seguintes desvios para cada padrão utilizado: maitenina (1), 0,99909; 22b-hidroximaitenina (2), 0,9999 e 0,99973; 20a-hidroximaitenina (3), 0,9999; celastrol (4), 0,99999 e pristimerina (5), 0,99863. Estas curvas foram utilizadas para efetuar a determinação quantitativa das substâncias 1-5 nos diferentes especimens de M. ilicifolia estudados (Tabela 1). Com base nestes resultados foi possível concluir que os especimens III e IV mostram o acúmulo de todos os triterpenos quinonametídeos citados (1-5), enquanto que os especimens I, II e V estão restritos a presença de 1, 3 e 5. Com base nestes dados foi possível selecionar os especimens II e IV para o estabelecimento de cultura de células, as quais serão utilizadas em futuros estudos biossintéticos e/ou enzimológico relacionados ao metabolismo dos triterpenos quinonametídeos 20a-hidroximaitenina (3) e celastrol (4), ainda não encontrados em nenhuma matriz já estudada.

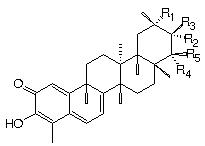
1. R1 = H; R2 = R3= O; R4 = R5 = H
2. R1 = H; R2 = R3= O; R4 = H; R5 = OH
3. R1 = OH; R2 = R3= O; R4 = R5 = H
4. R1 = COOH; R2 = R3= H; R4 = R5 = H
5. R1 = COOH3; R2 = R3= H; R4 = R5 = H
Tabela 1. Porcentagem, em relação ao peso seco do material vegetal, das substâncias 1-5 nos diferentes especimens I, II, III, IV, e V de M. ilicifolia.
|
Padrões |
1 |
2 |
3 |
4 |
5 |
|
Especimens |
|
|
|
|
|
|
I |
0,00035% |
-- |
0,00008% |
-- |
0,00035% |
|
II |
0,00040% |
-- |
0,00013% |
-- |
0,00054% |
|
III |
0,00150% |
0,00030% |
0,00029% |
0,00141% |
0,00070% |
|
IV |
0,00095% |
0,00026% |
0,00026% |
0,00034% |
0,00013% |
|
V |
0,00036% |
-- |
0,00008% |
-- |
0,00042% |
Bibliografia
1. Bavovada, R., et. al., Planta Med., 56, 380 (1990).
2. Corsino, J., et. al.,Phytochem. Anal. 9, 245 (1998)
3. Kupchan, S.M., et. al., J. Am. Chem. Soc., 94, 1354, (1972).
4. Marini Bettolo, G.B., Rev. Latinoamer. Quim., 10, 97, (1979).
5. Monache, F.D., et. al., Angew. Entomol., 97, 406, (1984).
FAPESP, CAPES, CnPQ