oxidação eletroquímica
de primaquina em meio ácido
Maria Lara Palmeira de Macedo Arguelho1 (PG) e Nelson
Ramos Stradiotto2 (PQ).
1Departamento
de Química - Universidade de São Paulo - Ribeirão
Preto, SP.
2Instituto
de Química - Universidade Estadual Paulista - Araraquara, SP.
palavras-chaves:
antimalárico, eletroxidação, voltametria
cíclica.
INTRODUÇÃO
Primaquina
(PQ) é um 8-aminoquinolínico empregado no tratamento da
malária em diferentes países. Esta droga impede a
transmissão da malária ao inibir a formação
de esporozoítos da malária nos mosquitos infectados,
diferindo do modo de ação dos demais compostos
aminoquinolínicos que agem como esquizonticida sanguíneo1.
Tendo em vista a
relevância das propriedades redox da primaquina para um melhor
entendimento de seu mecanismo de ação, o objetivo deste
trabalho foi a investigação do processo eletródico
de oxidação da primaquina utilizando as técnicas
de voltametria cíclica e cronoamperometria.
Parte
Experimental
O
composto dicloreto de primaquina foi fornecido pela Sigma Chemical
Co., sendo os reagentes utilizados na composição do
tampão Britton-Robinson provenientes da Aldrich Co. Os
experimentos eletroquímicos foram realizados utilizando-se
soluções com concentrações entre 0,1 e 10
mmol.L-1 de primaquina em diferentes valores de pH.
As
medidas eletroquímicas foram realizadas em um potenciostato /
galvanostato modelo 273 da PARC, acoplado a um microcomputador. O
sistema voltamétrico é formado por uma microcélula
(PARC, K O264) com capacidade para
5mL, um microeletrodo de
carbono vítreo de disco com diâmetro de 10 mm
(PARC, G 0226) usado como eletrodo de trabalho, um eletrodo
auxiliar de rede de platina (PARC, K 0033) e um eletrodo de
calomelano saturado (PARC, K 0077) usado como eletrodo de
referência.
Resultados e Discussão
Os
voltamogramas cíclicos obtidos para soluções 1 x
10–3 mol L-1 de primaquina no intervalo de pH entre 2
a 8, apresentaram um pico de oxidação com
características de processo irreversível (Figura 1). 0
gráfico de Epa vs pH apresenta duas relações
lineares com intersecção em valores de pH igual à
4,0, o qual poderia ser associado ao valor da constante de
dissociação da primaquina na forma protonada. No
intervalo de pH entre 2 a 4 observa-se um deslocamento de 55mV
(Figura 2), indicando um processo envolvendo um próton na
etapa determinante de velocidade de transferência eletrônica2.
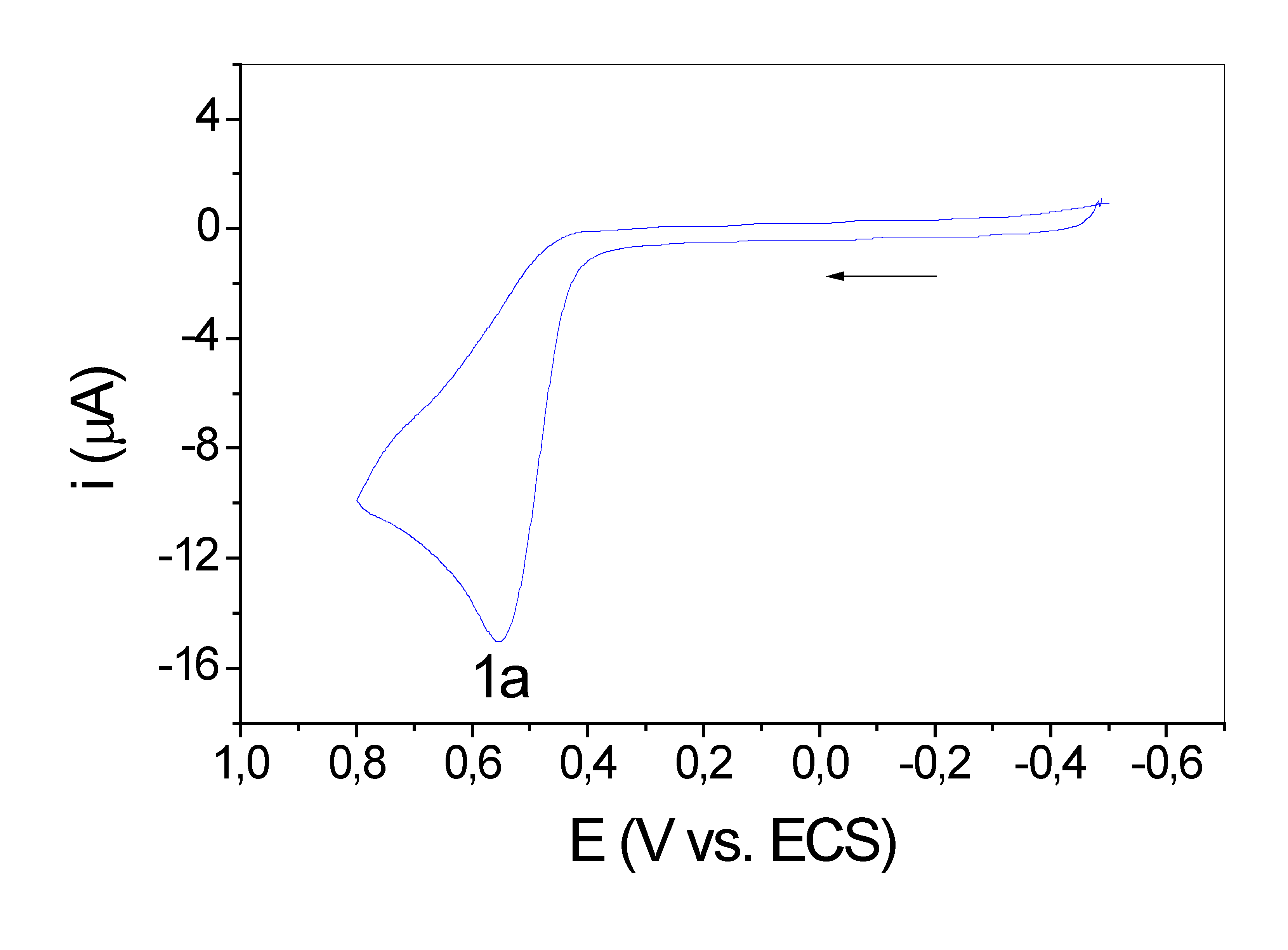
Figura
1. Ciclovoltamograma da primaquina (1X10-3 mol.L-1)
em pH 4,0,
n
= 0,1 V.S-1.
Figura
2. Comportamento do potencial de oxidação para
soluções de primaquina 1X10-3 mol.L-1,
n = 0,1 V.S-1.
O
processo caracteriza-se por uma variação linear da
corrente anódica em função da raiz quadrada da
velocidade de varredura (n1/2)
indicando que esta oxidação é controlada por
difusão.
A
função corrente apresenta-se constante em todo o
intervalo de velocidade de varredura estudado. O potencial de
oxidação apresenta um deslocamento para valores mais
positivos em função da velocidade de varredura e da
concentração da espécie eletroativa, indicando
que a irreversibilidade diagnosticada anteriormente pode ser
resultado da presença de reação química
acoplada à uma transferência eletrônica
reversível.
Resultados
cronoamperométricos no intervalo 0,5 < t < 5.0 para
primaquina 1x10-3 mol.L-1, indicam valores
constantes de i.t-1/2/C e um processo eletródico
envolvendo um elétron por molécula. Estudos
comparativos com os compostos análogos (8-aminoquinolina e
quinolina) indicam que a oxidação da primaquina ocorre
pela perda de um elétron do anel quinolínico, seguida
por uma possível reação de dimerização3.
REFERÊNCIAS BIBLIOGRÁFICAS
1.
Cohen, G. e Hochstein, P. Biochemistry 3 (1964) 895.
2.
Klinger, R. J. e Kochi, J. K. J. Am. Chem. Soc. 102 (1980)
4790.
3.
Savéant, J. M., Nadjo, L. e Andrieux C. P. J. Eletroanal.
Chem. 42 (1973) 223.
FAPESp

