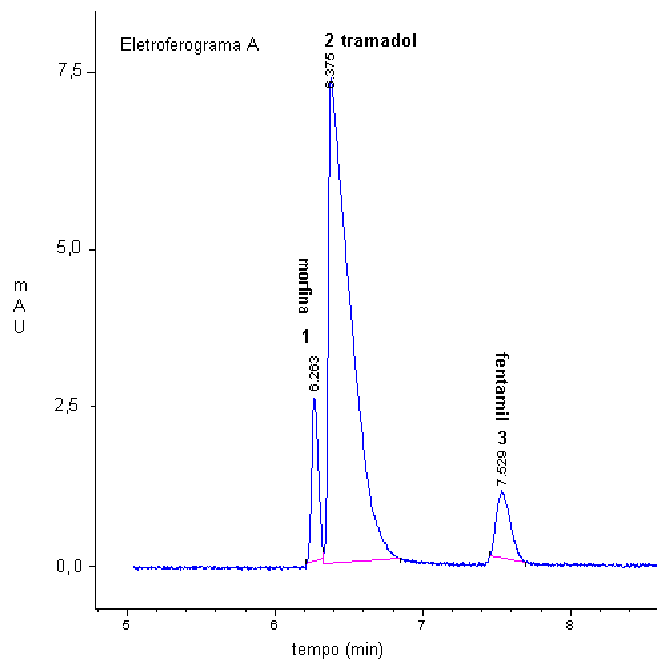
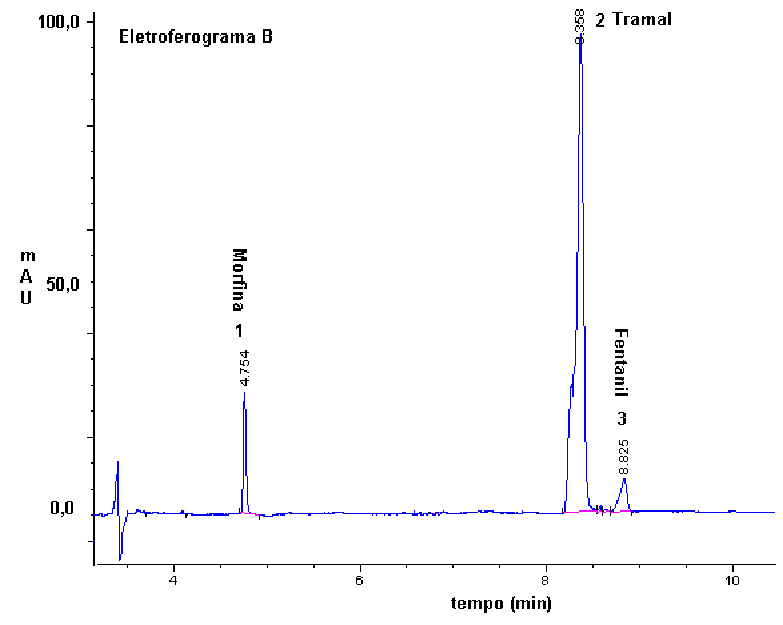
As análises foram conduzidas sob voltagem constante (30kV) com detecção em 200nm. Na figura 1 são mostrados os eletroferogramas obtidos em solução livre e meio micelar
SEPARAÇÃO DE DROGAS DE ABUSO (FÁRMACOS OPIÓIDES), DE INTERESSE CLÍNICO E FORENSE, POR ELETROFORESE CAPILAR (CE) EM SOLUÇÃO LIVRE E MEIO MICELAR
Elizabete Campos de Lima (PG)1, Marina F. M. Tavares (PQ)1,Bronislaw Polakiewcz (PQ)2 ; Adilson Alves Dias(PQ)1
1Instituto de Química da Universidade de São Paulo, CP 06083, CEP 05599-970
2Depto. de Tecnologia Bioquímica – Faculdade de Ciências Farmacêuticas da Universidade de São Paulo, CP 66083, CEP 05315-970
Introdução:
Drogas são substâncias que alteram as funções do corpo quando consumidas. Na medicina, as drogas são usadas para fins terapêuticos. Os opióides constituem um grupo de fármacos semelhantes à morfina, alcalóide natural extraído do ópio, e são empregados principalmente como analgésicos. Como estas drogas possuem um elevado efeito euforizante muitas vezes são abusadas pelo homem. 1
Os métodos cromatográficos, tais como HPLC (cromatografia líquida de alto desempenho) e CG/GC-MS (cromatografia gasosa acoplada à espectrometria de massas) são as técnicas mais utilizadas para a determinação e quantificação de drogas em indivíduos em seus fluídos e tecidos biológicos.2
Nas últimas décadas a eletroforese capilar surgiu como uma técnica analítica de separação alternativa para a análise de fármacos e uma gama de outros compostos. A eletroforese oferece inúmeras vantagens sobre as outras técnicas de separação: separações de alta eficiência, de alta sensibilidade, tempos de análise apreciavelmente curtos e gasto mínimo de solvente e amostra.3
Objetivos:
1 - Estudo da separação de uma mistura de opióides utilizados em clínica médica e uma mistura de opióides padrão por CE em solução livre e meio micelar.
2 - Avaliação do uso de modificadores orgânicos na separação em meio micelar.
Materiais e métodos:
Um sistema de eletroforese capilar P/ACE Beckman 5510 equipado com detector diode array e capilares de sílica fundida de 75mm de diâmetro interno com 47 cm de comprimento total e 40cm de comprimento efetivo, foram utilizados em todas as análises. Amostras dos opióides fentanil, morfina, tramadol em ampolas injetáveis diluídas para a concentração de 50 mg/mL foram analisadas em mistura. Padrões destes opióides em mistura na concentração de 50mg/mL também foram analisados. Na tabela 1 são mostradas as condições de análise realizadas para eletroforese em solução livre e micelar.
Tabela 1 – Condições de análise realizadas
|
Solução Livre |
Tampão |
SDS1 (mM) |
Aditivos orgânicos |
|||
|
b-CD2 (mM) |
MeOH3 (%) |
|||||
|
|
Nome |
Concentrção (mM) |
pH |
|||
|
|
Fosfato |
10 |
2,5 |
¾ |
¾ |
¾ |
|
Meio Micelar |
Borato |
10 |
9,0 |
10,15, 20,30 e 40 |
10, 15 e 20 |
0, 1 e 2 |
1)SDS = dodecil sulfato de sódop /2) - b-CD = b-ciclo dextrina/ 3) - MeOH = metanol


As
análises foram conduzidas sob voltagem constante (30kV) com
detecção em 200nm. Na figura 1 são mostrados os
eletroferogramas obtidos em solução livre e meio
micelar
Figura 1 – Eletroferogramas das misturas de opóides utilizados em clínica médica em solução livre
(eletroferograma A) e meio micelar (eletroferograma B)
Conclusões:
As separações em solução livre da mistura dos opóides tramal, fentanil e morfina (pH 2,5) ocorreram com sucesso; neste meio os componentes da mistura comportam-se como cátions cada qual possuindo uma mobilidade eletroforética única. Enquanto que em meio micelar (pH 9); para separação dos opióides tramal, fentanil e morfina é necessária a utilização de modificadores orgânicos pois a interação destes compostos com a micela é semelhante. A melhor separação ocorreu com a seguinte composição de eletrólito: Borato 10mM + SDS 50mM + b - ciclodextrina 20mM + metanol 2%. A próxima etapa do trabalho será aplicação da metodologia desenvolvida a amostras de cabelo de pacientes portadores de câncer, que estão sob efeito de medicação à base de opióides para controle da dor.
Referências Bibliográficas:
1- S. Oga, “Fundamentos de Toxicologia”, Atheneu Editora São Paulo Ltda., São Paulo, 1996.
2- S. Härter; B. Jensen; C. Hiemke; M. Leal; H. Weigman; K. Unger; J. Chromatogr. B, 712 (1998), 253-258.
3- D. R. Baker, “ Capillary electrophoresis”; New YorK, John Wiley, 1995.
FAPESP