COMPORTAMENTO LUMINESCENTE
DOS PRODUTOS
DE DECOMPOSIÇÃO
TÉRMICA DO Eu(C7H7SO3)3×2H2O
Arnaud
Victor dos Santos (PQ)1, Hermi Felinto de Brito (PQ)2,
Oscar L. Malta(PQ)3 e Jivaldo do Rosário Matos
(PQ)2.
1Departamento
de Química -Universidade Federal da Paraíba -–
João Pessoa – PB. 2Departamento de Química
Fundamental -Instituto de Química -USP São Paulo-SP.
3Departamento de Química Fundamental - UFPE-CCEN -
Recife - PE
e-mail:
avsantos@labpesq.quimica.ufpb.br
Palavras-chaves:
p-toluenossulfonato, luminescência, análise térmica
Introdução.
Os primeiros compostos de p-toluenossulfonatos de terras raras,
TR(pTS), foram estudados em solução por Nakani e
Giesekke 1982 [1]. Posteriormente, Ohki et al [2] sintetizaram
os compostos de fórmula geral TR(pTS)3.9H2O,
empregando o mesmo procedimento descrito na síntese dos
2-naftalenossulfonatos de TR3+ [3]. No entanto, não
foi citado na literatura artigos relacionados a estudos das etapas de
decomposição térmica ou que associem as
propriedades luminescente dessa classe de compostos a dados
termoanalíticos.
Objetivos.
Este trabalho se propõe à obtenção de
compostos luminescentes a partir dos produtos de decomposição
térmica utilizando o precursor Eu(pTS)3×2H2O.
Parte
Experimental. O sal de Eu foi preparado fazendo-se reagir uma
suspensão aquosa do respectivo hidroxicarbonato com ácido
p-toluenossulfônico na proporção molar 1:3. Esse
sal e os seus produtos de decomposição térmica,
isolados em diferentes temperaturas, foram caracterizados por análise
elementar, difração de raios X e espectroscopia de
absorção no infravermelho e avaliados quanto as suas
propriedades luminescentes. As curvas TG/DTG, foram obtidas na faixa
de temperatura de 30 à 1400 oC, sob atmosfera
dinâmica de ar (50 mL min-1), razão de
aquecimento de 10 oC min-1 e utilizando cadinho
de platina com massa em torno de 25 mg. Os espectros de emissão
e excitação do sal de partida e dos produtos de
decomposição térmica foram registrados à
temperatura de 298 e 77K.

m(%)
 Resultados
e Discussão. Os resultados de análise elementar e
de termogravimetria sugeriram a fórmula mínima:
Eu(C7H7SO3)3.2H2O.
Os espectros no infravermelho indicaram que a coordenação
do ânion ao íon Eu (III) ocorre através do átomo
de oxigênio do grupo sulfonato e que o composto foi obtido na
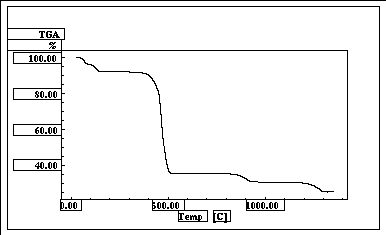
forma hidratada. Os dados de TG/DTG e DSC evidenciaram que a
desidratação ocorre entre 30 e 150oC e
apresentaram, respectivamente, os seguintes valores de perda de massa
e endoterma: 5,22% e DH
= 83 kJ/mol. Os difratogramas de raios X, método do pó,
do Eu(C7H7SO3)3,
hidratado e anidro, indicam que estes são cristalinos. Os
produtos da decomposição térmica do sal
precursor foram isolados nas temperaturas de 180, 650, 1000 e 1350 oC
e, respectivamente, correspondem as seguintes etapas do processo
térmico: (1) composto anidro [Eu(C7H7SO3)3],
(2) oxidissulfato de európio [Eu2O(SO4)2],
(3) dioxissulfato de európio (Eu2O2SO4)
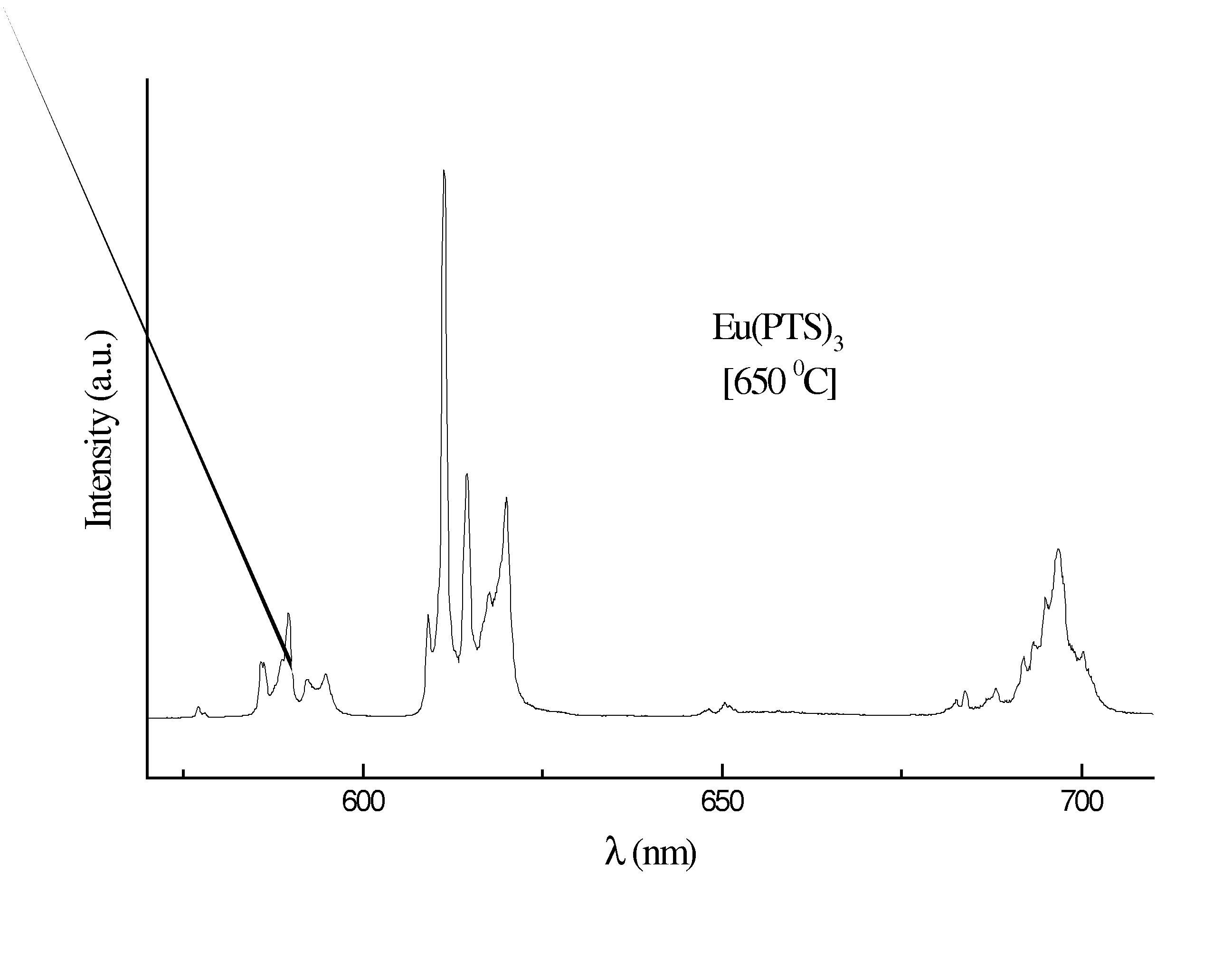
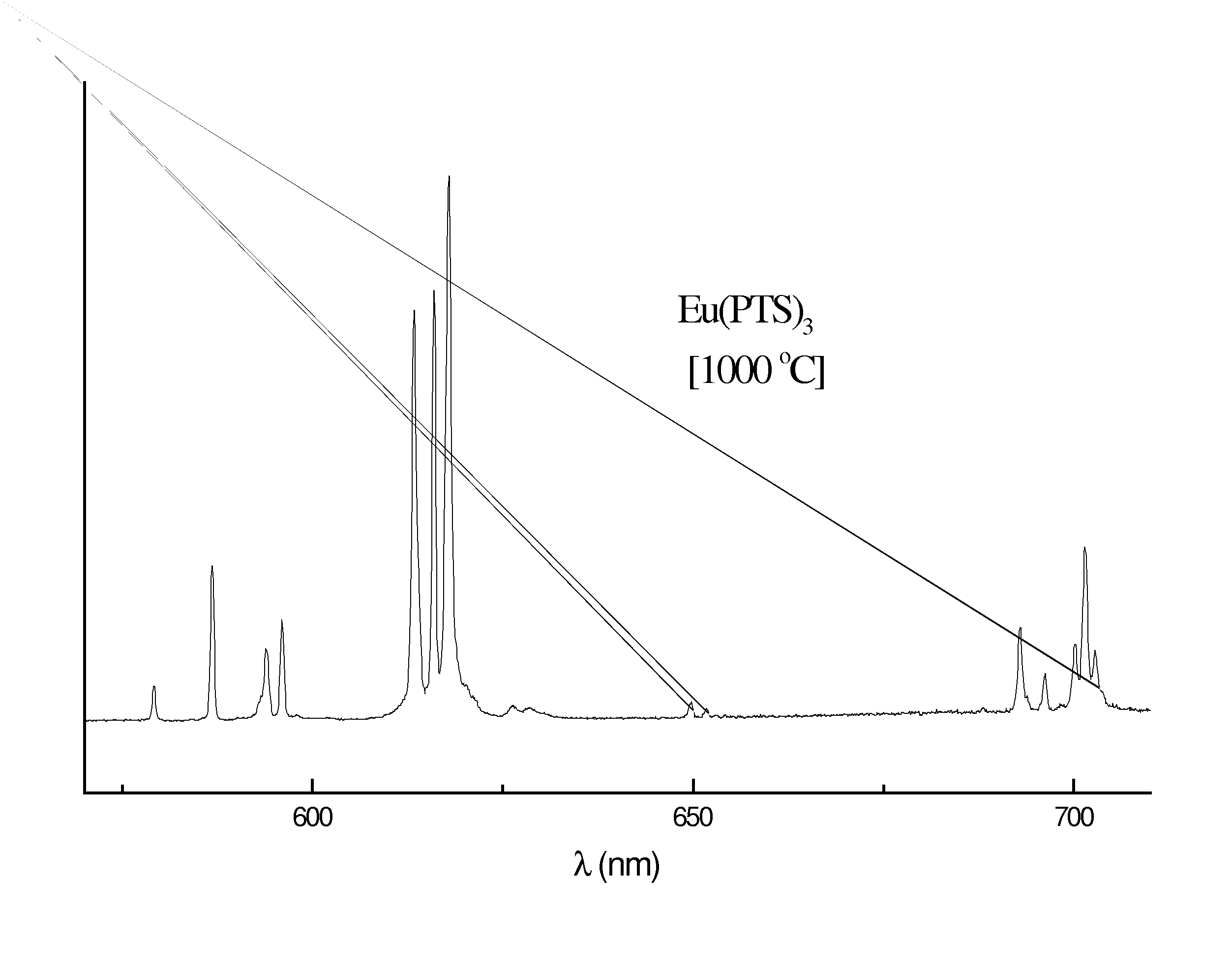
e (4) óxido de európio (Eu2O3). Os
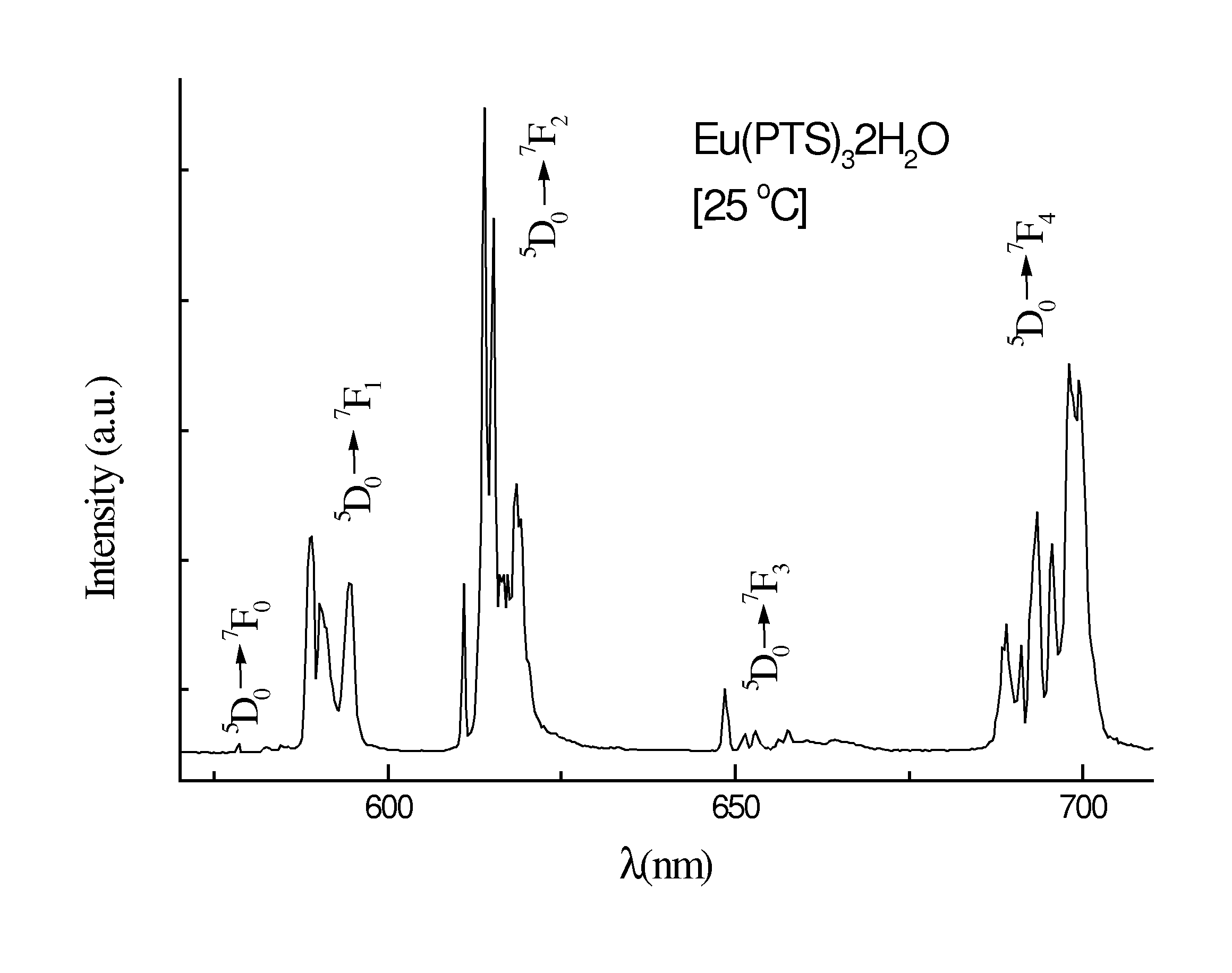
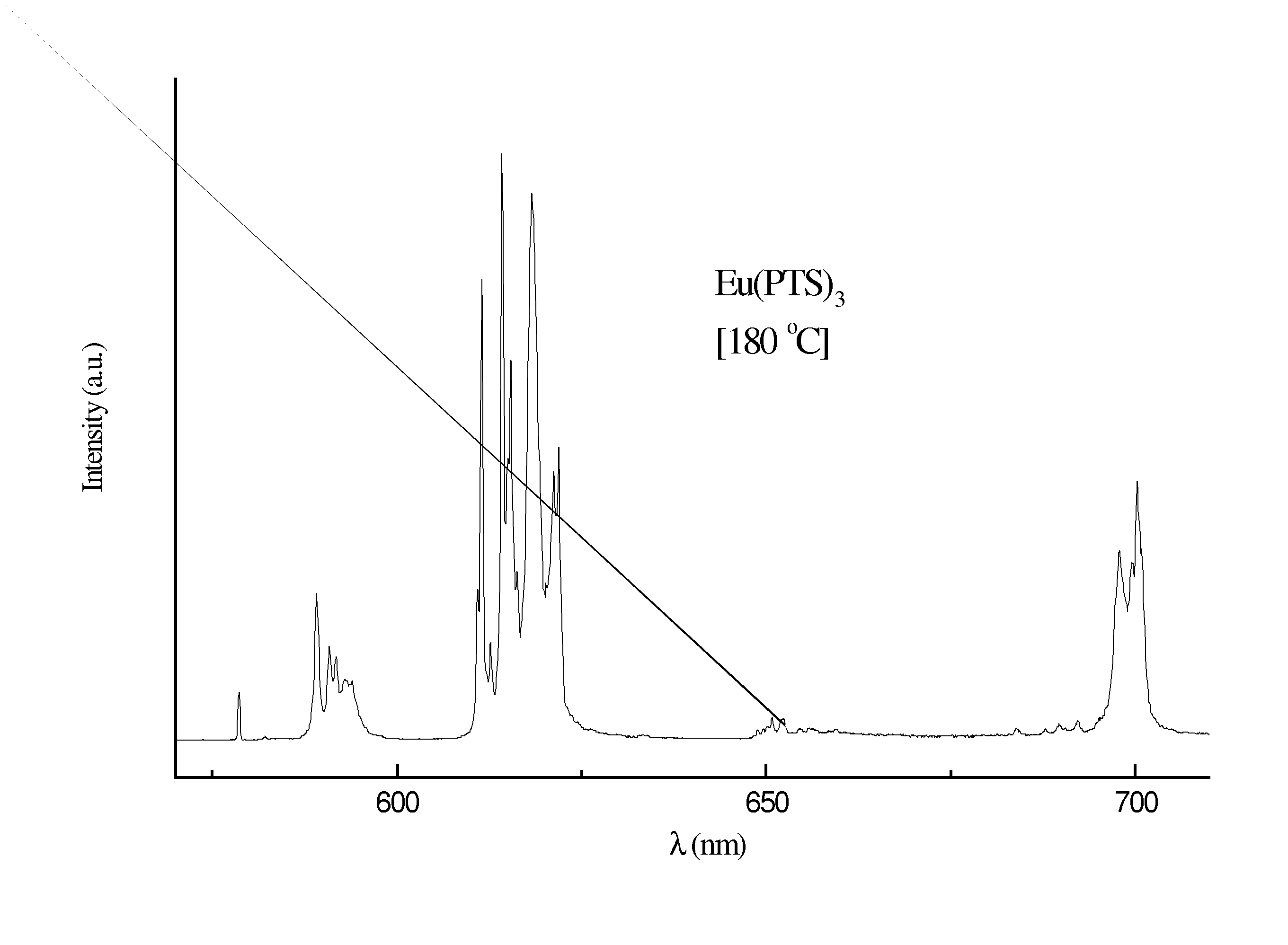
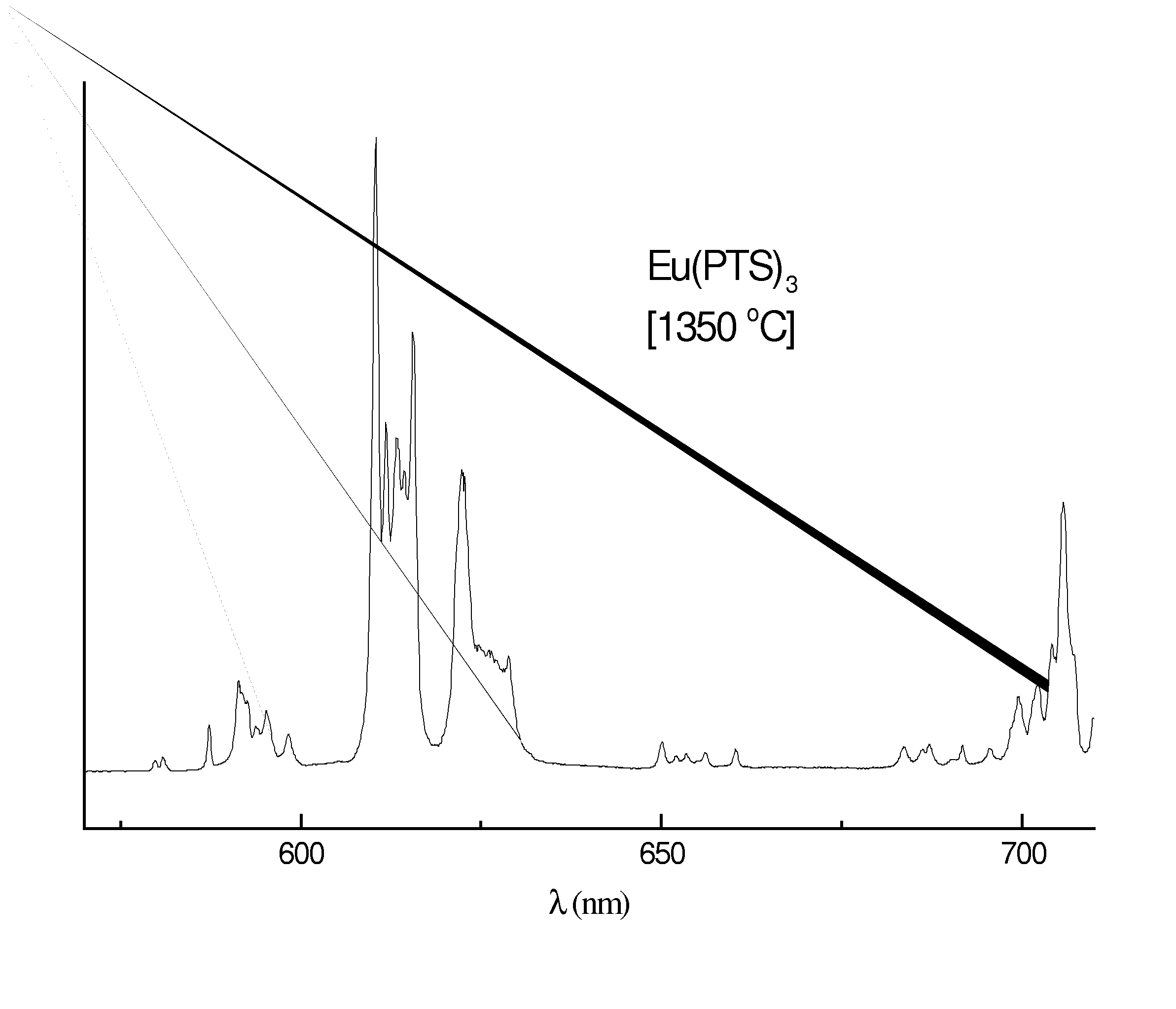
espectros de emissão dos Eu(C7H7SO3)3.2H2O, Eu(C7H7SO3)3,
Eu2O(SO4)2 e Eu2O3 (Figura) mostram desdobramentos para os níveis
5D0 ( 7FJ (J = 0 - 4) evidenciando que o íon Eu3+ encontra-se
em um ambiente químico com mais de um sítio de
simetria. Enquanto que para o composto Eu2O2SO4, isolado à
1000 oC, as transições obedecem a regra de seleção
(2J+1)-componentes, indicando que o íon Eu3+ encontra-se
somente em um sítio de simetria.
Resultados
e Discussão. Os resultados de análise elementar e
de termogravimetria sugeriram a fórmula mínima:
Eu(C7H7SO3)3.2H2O.
Os espectros no infravermelho indicaram que a coordenação
do ânion ao íon Eu (III) ocorre através do átomo
de oxigênio do grupo sulfonato e que o composto foi obtido na
forma hidratada. Os dados de TG/DTG e DSC evidenciaram que a
desidratação ocorre entre 30 e 150oC e
apresentaram, respectivamente, os seguintes valores de perda de massa
e endoterma: 5,22% e DH
= 83 kJ/mol. Os difratogramas de raios X, método do pó,
do Eu(C7H7SO3)3,
hidratado e anidro, indicam que estes são cristalinos. Os
produtos da decomposição térmica do sal
precursor foram isolados nas temperaturas de 180, 650, 1000 e 1350 oC
e, respectivamente, correspondem as seguintes etapas do processo
térmico: (1) composto anidro [Eu(C7H7SO3)3],
(2) oxidissulfato de európio [Eu2O(SO4)2],
(3) dioxissulfato de európio (Eu2O2SO4)
e (4) óxido de európio (Eu2O3). Os
espectros de emissão dos Eu(C7H7SO3)3.2H2O, Eu(C7H7SO3)3,
Eu2O(SO4)2 e Eu2O3 (Figura) mostram desdobramentos para os níveis
5D0 ( 7FJ (J = 0 - 4) evidenciando que o íon Eu3+ encontra-se
em um ambiente químico com mais de um sítio de
simetria. Enquanto que para o composto Eu2O2SO4, isolado à
1000 oC, as transições obedecem a regra de seleção
(2J+1)-componentes, indicando que o íon Eu3+ encontra-se
somente em um sítio de simetria.

 Conclusão
- O presente trabalho possibilitou a obtenção e
caracterização de materiais potencialmente
luminescentes monitorados por termogravimetria e espectroscopia
emissão. A associação destas técnicas
permitiu o estudo das propriedades luminescentes dos diferentes
produtos de decomposição, assim como inferir que o
intermediário isolado em 1000oC, Eu2O2SO4, poderá ser
um precursor para a preparação do fósforos
Y2O2S:Eu3+.
Conclusão
- O presente trabalho possibilitou a obtenção e
caracterização de materiais potencialmente
luminescentes monitorados por termogravimetria e espectroscopia
emissão. A associação destas técnicas
permitiu o estudo das propriedades luminescentes dos diferentes
produtos de decomposição, assim como inferir que o
intermediário isolado em 1000oC, Eu2O2SO4, poderá ser
um precursor para a preparação do fósforos
Y2O2S:Eu3+.
Referências
[1] Nakani, B. S. and Giesekke, W. (1982). Polyhedron. 1(3), 253.
[2] Ohki, Y.; Suzuki, Y.; Takeuchi, T. and Ouchi, A. (1988). Bull.
Chem. Soc. Japan. 61(2), 393. [3] Ohki, Y.; Suzuki, Y.; Nakamura,
M.; Shimoi M. (1985). Bull. Chem. Soc. Japan. 58(10), 2968.
[FAPESP,
CNPq, CAPES]




 Resultados
e Discussão. Os resultados de análise elementar e
de termogravimetria sugeriram a fórmula mínima:
Eu(C7H7SO3)3.2H2O.
Os espectros no infravermelho indicaram que a coordenação
do ânion ao íon Eu (III) ocorre através do átomo
de oxigênio do grupo sulfonato e que o composto foi obtido na
forma hidratada. Os dados de TG/DTG e DSC evidenciaram que a
desidratação ocorre entre 30 e 150oC e
apresentaram, respectivamente, os seguintes valores de perda de massa
e endoterma: 5,22% e DH
= 83 kJ/mol. Os difratogramas de raios X, método do pó,
do Eu(C7H7SO3)3,
hidratado e anidro, indicam que estes são cristalinos. Os
produtos da decomposição térmica do sal
precursor foram isolados nas temperaturas de 180, 650, 1000 e 1350 oC
e, respectivamente, correspondem as seguintes etapas do processo
térmico: (1) composto anidro [Eu(C7H7SO3)3],
(2) oxidissulfato de európio [Eu2O(SO4)2],
(3) dioxissulfato de európio (Eu2O2SO4)
e (4) óxido de európio (Eu2O3). Os
espectros de emissão dos Eu(C7H7SO3)3.2H2O, Eu(C7H7SO3)3,
Eu2O(SO4)2 e Eu2O3 (Figura) mostram desdobramentos para os níveis
5D0 ( 7FJ (J = 0 - 4) evidenciando que o íon Eu3+ encontra-se
em um ambiente químico com mais de um sítio de
simetria. Enquanto que para o composto Eu2O2SO4, isolado à
1000 oC, as transições obedecem a regra de seleção
(2J+1)-componentes, indicando que o íon Eu3+ encontra-se
somente em um sítio de simetria.
Resultados
e Discussão. Os resultados de análise elementar e
de termogravimetria sugeriram a fórmula mínima:
Eu(C7H7SO3)3.2H2O.
Os espectros no infravermelho indicaram que a coordenação
do ânion ao íon Eu (III) ocorre através do átomo
de oxigênio do grupo sulfonato e que o composto foi obtido na
forma hidratada. Os dados de TG/DTG e DSC evidenciaram que a
desidratação ocorre entre 30 e 150oC e
apresentaram, respectivamente, os seguintes valores de perda de massa
e endoterma: 5,22% e DH
= 83 kJ/mol. Os difratogramas de raios X, método do pó,
do Eu(C7H7SO3)3,
hidratado e anidro, indicam que estes são cristalinos. Os
produtos da decomposição térmica do sal
precursor foram isolados nas temperaturas de 180, 650, 1000 e 1350 oC
e, respectivamente, correspondem as seguintes etapas do processo
térmico: (1) composto anidro [Eu(C7H7SO3)3],
(2) oxidissulfato de európio [Eu2O(SO4)2],
(3) dioxissulfato de európio (Eu2O2SO4)
e (4) óxido de európio (Eu2O3). Os
espectros de emissão dos Eu(C7H7SO3)3.2H2O, Eu(C7H7SO3)3,
Eu2O(SO4)2 e Eu2O3 (Figura) mostram desdobramentos para os níveis
5D0 ( 7FJ (J = 0 - 4) evidenciando que o íon Eu3+ encontra-se
em um ambiente químico com mais de um sítio de
simetria. Enquanto que para o composto Eu2O2SO4, isolado à
1000 oC, as transições obedecem a regra de seleção
(2J+1)-componentes, indicando que o íon Eu3+ encontra-se
somente em um sítio de simetria.



 Conclusão
- O presente trabalho possibilitou a obtenção e
caracterização de materiais potencialmente
luminescentes monitorados por termogravimetria e espectroscopia
emissão. A associação destas técnicas
permitiu o estudo das propriedades luminescentes dos diferentes
produtos de decomposição, assim como inferir que o
intermediário isolado em 1000oC, Eu2O2SO4, poderá ser
um precursor para a preparação do fósforos
Y2O2S:Eu3+.
Conclusão
- O presente trabalho possibilitou a obtenção e
caracterização de materiais potencialmente
luminescentes monitorados por termogravimetria e espectroscopia
emissão. A associação destas técnicas
permitiu o estudo das propriedades luminescentes dos diferentes
produtos de decomposição, assim como inferir que o
intermediário isolado em 1000oC, Eu2O2SO4, poderá ser
um precursor para a preparação do fósforos
Y2O2S:Eu3+.