COMPORTAMENTO
VOLTAMÉTRICO DO BENZNIDAZOL UTILIZANDO-SE ELETRODO DE CARBONO
VÍTREO
MODIFICADO COM DNA
Mauro
Aquiles La-Scalea (PQ)1; Elizabeth Igne Ferreira (PQ)1;
Sílvia Helena Pires Serrano (PQ)2; Ana Maria
Oliveira Brett (PQ)3
1 -
Dep. de Farmácia - Faculdade de Ciências Farmacêuticas,
USP
2 - Dep. de Química
Fundamental - Instituto de Química, USP
3 - Dep. de Química
- Universidade de Coimbra, Portugal
palavras-chave: benznidazol,
eletrodo de DNA, hidroxilamina
INTRODUÇÃO
E OBJETIVOS
Os
nitroimidazóis são importantes por apresentarem amplo
espectro de atividade biológica e por selecionarem baixo nível
de resistência em microrganismos anaeróbicos. O
benznidazol (BZN) é comumente utilizado no tratamento da
doença de Chagas, infecção por Trypanosoma
cruzi, e único fármaco comercializado no Brasil. A
doença de Chagas atinge cerca de um quarto da população
da América e entre 16 a 18 milhões de indivíduos
encontram-se infectados. A ação biológica dos
nitrocompostos é dependente da redução do grupo
nitro. O nitro radical aniônico e o derivado hidroxilamínico
são os principais intermediários responsáveis
pela ação citotóxica dos nitroimidazóis e
acredita-se que o DNA seja o principal alvo destes produtos de
redução. Para os 2-nitroimidazóis, a
hidroxilamina seria a responsável principal pela atividade
biológica1.
Este
trabalho tem por objetivo estudar o comportamento voltamétrico
do BZN utilizando-se eletrodo de carbono vítreo modificado com
DNA (ECV-DNA) e avaliar a possibilidade de interação do
derivado hidroxilamínico gerado eletroquimicamente e o DNA
imobilizado na superfície do eletrodo de carbono vítreo.
PARTE EXPERIMENTAL
A
solução estoque de DNA Calf Thymus (sal sódico,
tipo I) desnaturado foi efetuada dissolvendo-se cerca de 3 mg de DNA
em 0,5 mL de HClO4 60%, seguida da adição de
0,5 mL de NaOH 9,0 mol/L e completou-se o volume a 50 mL com tampão
acetato pH 4,5. A solução estoque de BZN 0,01 mol/L foi
preparada com etanol 80%. Preparou-se o tampão universal a
partir da mistura de ácidos fosfórico, acético e
bórico com NaOH. Utilizou-se potenciostato mAutolab
acoplado a célula eletroquímica de 10 mL com sistema de
três eletrodos: carbono vítreo (ECV) e ECV-DNA como
eletrodos de trabalho, eletrodo Ag/AgCl referência e Pt como
eletrodo auxiliar. A aquisição e tratamento de dados
foi efetuada por meio do software GPES versão 4.1 da
Eco-Chemie, Holanda.
O
ECV-DNA foi preparado por recobrimento total da área de
carbono vítreo com 3 mg de DNA nativo em tampão acetato
pH 4,5. Após secagem, o eletrodo foi condicionado em solução
tampão com aplicação, por cinco minutos, de
potencial a 1,4 V seguido de registro de linha base entre 0,0 e 1,4
V, utilizando-se a voltametria de pulso diferencial. Em seguida,
transferiu-se o eletrodo para solução de DNA
desnaturado e este procedimento foi repetido até obtenção
de superfície modificada estável.
RESULTADOS E DISCUSSÃO
Utilizando-se ECV-DNA, o
voltamograma de pulso diferencial para BZN em pH 3,06 apresentou
única onda de redução, com potencial de pico (Ep
= -0,23 V), referente à redução do grupo nitro,
envolvendo quatro elétrons, para formar o intermediário
hidroxilamínico. Com o ECV a onda de redução
para o BZN foi ligeiramente mais negativa com Ep = -0,27 V. Em meio
ácido e com ambos os eletrodos, o valor de Ep para a onda de
redução do BZN é deslocado no sentido negativo
com aumento de pH, confirmando a participação de íons
H+ no mecanismo de redução do benznidazol.
Em meio básico a redução é independente
do pH e os valores de Ep registrados com os dois eletrodos são
semelhantes.
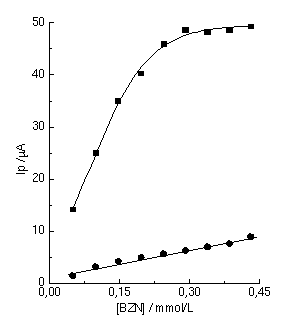
FIGURA 1
- Curvas de adição de padrão de BZN
correspondentes aos picos anódicos conseqüentes da
formação do derivado hidroxilamínico na
superfície do ECV-DNA em pH 4,5: (n)
pico I; (l)
pico II.
Efetuou-se a formação do derivado
hidroxilamínico por meio da pré-concentração
de BNZ por cinco minutos a -0,5 V, garantindo a redução
do fármaco na multicamada de DNA, seguido de redissolução
anódica. Após o período de deposição
do fármaco, iniciou-se a varredura em -0,2 V registrando-se
picos a 0,20 V (pico I),
correspondente à
oxidação da hidroxilamina ao derivado nitroso, e
0,53 V para o pico II,
atribuído à oxidação de ácido
desoxipurínico, produto da interação da
hidroxilamina e o DNA imobilizado na superfície do eletrodo2.
A adição padrão de BZN provocou aumento nos
valores de corrente para os dois picos (Fig.1). Esses resultados
corroboram a hipótese que para os 2-nitroimidazóis a
espécie reativa e responsável pela ação
citotóxica destes fármacos é o derivado
hidroxilamínico1.
Diante do exposto, o estudo do
comportamento voltamétrico do benznidazol utilizando-se o
ECV-DNA apresenta-se como excelente alternativa para compreensão
do mecanismo de ação biológica dos
2-nitroimidazóis, além de representar a possibilidade
de obtenção de importantes parâmetros para
estudos de relação entre estrutura química e
atividade biológica e a conseqüente contribuição
para desenvolvimento de novos fármacos para o tratamento da
doença de Chagas.
REFERÊNCIAS BIBLIOGRÁFICAS
La-Scalea, M.A, - Rev. Farm.
Bioquím. Univ. São Paulo, 34(2), 59, 1998.
Brett, A.M.O.; Serrano, S.H.P.; Gutz,
I.; La-Scalea, M.A.; Cruz, M.L. - Electroanalysis, 9(14),
1132, 1997.
FAPESP, CNPq, ICCT/Portugal
