COMPOSIÇÃO QUÍMICA E ATIVIDADE ANTIFÚNGICA DO ÓLEO ESSENCIAL DE Psychotria spectabillis L. (RUBIACEAE).
Paulo José Coelho Benevides1 (PG), Maria Claudia Marx Young2 (PQ), Vanderlan da Silva Bolzani (PQ)3.
1Instituto de Química - Departamento de Química Fundamental - Universidade de São Paulo, C.P. 26077, CEP 05599-970, SP. 2Departamento de Fisiologia e Bioquímica de Plantas - Instituto Botânico, C.P. 4005, EP 01161-970, SP. 3Instituto de Química - Departamento de Química Orgânica - Universidade Estadual Paulista, C.P. 355, CEP 14800-900, Araraquara- SP.
Palavras-chave: Psychotria spectabillis, Rubiaceae, óleo essencial, atividade antifúngica.
A espécie Psychotria spectabillis pertence a família Rubiaceae, sensu Cronquist1, uma das maiores de Angiospermae, constituída por 40 tribos, 637 gêneros e cerca de 10.700 espécies. As espécies do gênero Psychotria (original do grego: psique = alma e trophos = alimento) tem despertado interesse tanto do ponto de vista etnobotânico como farmacológico. P. viridis2,3 é uma planta medicinal muito utilizada em rituais religiosos, onde é preparada uma bebida alucinógena conhecida como ayahuasca, caapi, yagê ou daime. As atividades biológicas atribuídas as espécies deste gênero estão relacionadas à presença de alcalóides indólicos e poliindolêninicos; espécies como P. beccarioides, P. forsteriana e P. olenoides são conhecidas por biossintetizar esses alcalóides, altamente citotóxicos4,5. A ação alucinógena de espécies desse gênero deve-se a presença de triptaminas3.
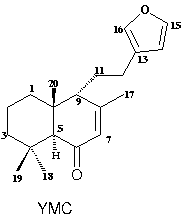
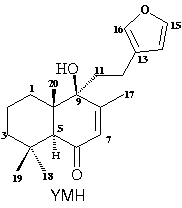
Dando continuidade ao estudo químico e biológico de P. spectabillis, foi feita a extração do óleo essencial de folhas com o objetivo de se determinar a sua composição e atividade biológica. Para tal, folhas de um espécimen adulto (7m) foram coletadas na floresta próxima a Barragem Dormente no Estado do Amapá, em outubro de 1996 (Exsicata depositada no herbário do Instituto Botânico, SP, cód. Lopes-27). As folhas secas (34 g) foram hidro-destiladas em um aparelho do tipo Clevenger, obtendo-se 0,16 mL do óleo essencial o que correspondeu a 0,45% de rendimento. O óleo essencial foi submetido a análise por CG, e os componentes desse óleo, identificados pelo índice de Kovats de cada componente e por co-injeção com padrões. Para ajuste dos tempos de retenção foi usado o tempo de retenção do gás butano na coluna. Foram usados um cromatógrafo gasoso modelo HP-5890 Série II, com injetor de divisão de fluxo, detetor de ionização de chama (FID), integrador HP-3396 e uma coluna de polaridade média HP-5 de 30mX0,2mmX0,33m. Foram injetados na forma de uma mistura homogênea os hidrocarbonetos da série homóloga C9 - C20 da marca Aldrichi. Esta série foi usada para o cálculo dos índices de retenção. O óleo essencial e os padrões foram analisados nas seguintes condições: temperatura inicial: 600C, temperatura final: 2900C/10min, programação: 30C/min, temperatura do injetor: 2200C, temperatura do detetor: 3000C, volume de injeção: 1 mL, vazão do gás de arraste (H2): 2 mL/min. Os diterpenos labdânicos YMC e YMH foram isolados em mistura por cromatografia em coluna de sílica, e identificados através dos dados de RMN 1H e 13C, e também pela comparação com os dados desses diterpenos isolados e identificados anteriormente do extrato hexânico e clorofórmico de folhas de P. spectabillis. Para a averiguação da atividade antifúngica foi feito bioautografia com os fungos Cladosporium cladosporioides e C. sphaerospermum7. Amostra do óleo foi aplicada em cromatoplacas marca Merck, (Si gel F254) e eluidas com solvente apropriado, seguido de evaporação completa do solvente. Uma suspensão de esporos dos fungos reveladores foi adicionada a uma solução de glicose e sais minerais e em seguida pulverizada sobre as placas que foram incubadas a temperatura de 250C em câmara úmida escura, durante 48h.
A tabela 1 apresenta os principais componentes identificados e/ou isolados do óleo essencial de P.spectabillis, o qual apresentou exclusivamente sesquiterpenos e diterpenos. Não foram constatados monoterpenos, provavelmente devido ao material analisado ter sido folhas coletadas há três anos. Os diterpenos representam mais de 50% do óleo total. O óleo analisado mostrou atividade antifúngica potente, determinada pela CIM (concentração inibitória mínima) de 5 mg para as duas cepas, comparável a do antibiótico usado como padrão (nistatina) nas mesmas condições.
Tabela 1. Principais sesquiterpenos e diterpenos constituintes do óleo
essencial de P. spectabillis.
|
Substância |
IK |
Ikliteratura (6) |
% no óleo essencial |
|
cariofilano |
1424 |
1425 |
5,93 |
|
cariofileno |
1428 |
1428 |
3,48 |
|
humuleno |
1438 |
1437 |
3,71 |
|
copaeno |
1445 |
1445 |
4,60 |
|
cedreno |
1446 |
1446 |
7,13 |
|
bisabolano |
1449 |
1448 |
3,75 |
|
bisabolol |
1668 |
1666 |
3,60 |
|
farnesol |
1747 |
1745 |
7,87 |
|
YMC |
2089 |
- |
2,67 |
|
YMH |
2269 |
- |
5,05 |
|
|
|
|
|


Referências Bibliográficas
|
|
Robbrecht, E. (1988) Opera Botânica. v.1, 271. |
|
|
Libot, F. et al. (1987) J. Nat.Prod., 50, 468-473.. |
|
|
Roth, A. et al. (1985) Planta Medica, 3, 298-301 |
|
|
Hart, N.K., et al. (1974) Aust. Chem., 27, 639-643. |
|
|
Adjibadé, y., et al. (1992) J. Ethnopharmacology, 29, 127-136. |
|
|
Homans, L.A., Fuchs, A. (1970) J. Chromatog., 51, 327-329. |
|
|
Johnson, R.K., et al. (1986) In Vitro and in vivo Models for Detection of the New Antitumor Drugs, ed. por Hanka, L.J., Kondo, T. e White, R.J., 15-26. |
CNPq, PADCT, FAPESP.