
SDBS – dodecil benzenosulfonato de sódio
SEPARAÇÃO DE ÁCIDOS GRAXOS NO ÓLEO DE CASTANHA-DO-PARÁ POR ELETROFORESE CAPILAR UTILIZANDO PLANEJAMENTO FATORIAL
Marcone Augusto Leal de Oliveira * (PG), Gustavo A. Micke * (PG), Marina Franco Maggi Tavares * (PQ), Bronislaw Polakiewicz. ** (PQ), Luiz A. Gioielli. ** (PQ), Roy E. Bruns *** (PQ)
*Instituto de Química, Universidade de São Paulo, C.P 26077, 05599-970, São Paulo, SP, **Dep. de Tecnologia Bioquímica-Farmacêutica, Faculdade de Ciências Farmacêuticas, Universidade de São Paulo, C.P 66083, 05315-970, São Paulo, SP, ***Dep. Química, Universidade de Campinas, C.P 6154, 13083-970, Campinas, SP.
Palavras-chave: ácidos graxos, eletroforese capilar, planejamento fatorial
Introdução
Ácidos graxos constituem uma classe de compostos relevantes encontrados em plantas e animais. A determinação destes é de grande importância na caracterização química de óleos comestíveis e no controle de qualidade de produtos derivados do leite. A rancidez oxidativa dos óleos e viscosidade das margarinas estão diretamente relacionadas com a presença de insaturações e isomerização das cadeias alifáticas. Em geral, a análise de ácidos graxos livres (free fatty acids – FFAs) é realizada por cromatografia gasosa (GC) ou cromatografia líquida (LC). Essas técnicas envolvem, freqüentemente, passos de derivatização dos grupos carboxílicos, em espécies mais voláteis, no caso de GC, ou de derivados capazes de absorver no UV-vis no caso de LC. Uma alternativa bastante atraente é a eletroforese capilar (CE) a qual é uma técnica de separação baseada na migração diferenciada de compostos iônicos ou ionizáveis, em um campo elétrico. Nesta técnica a amostra do óleo é saponificada antes da injeção. Além disso, o uso de CE dispensa passos de derivatização, pois a detecção é feita de modo indireto.
Objetivos
Estudar a separação por eletroforese capilar em solução livre de ácidos graxos presentes no óleo de castanha-do-Pará, utilizando planejamento fatorial, monitorando a resolução do par crítico.
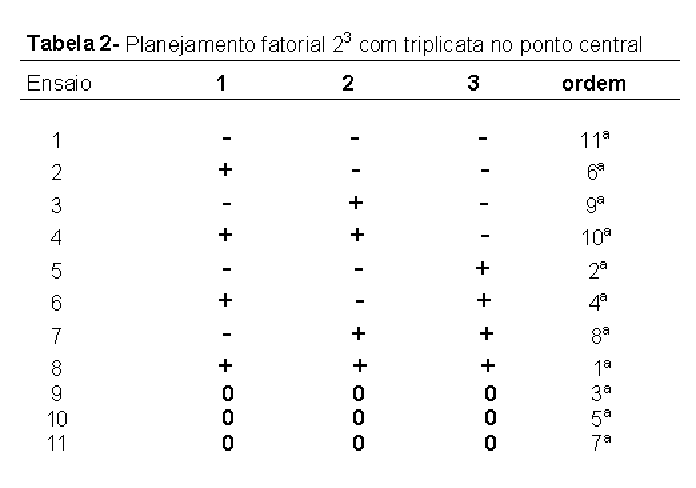
Os experimentos foram realizados no equipamento de eletroforese capilar modelo 270-HT da Applied Biosystems/PE com programa de aquisição de dados turbochromTM software. Um capilar de sílica fundida (75 mm d.i. x 77cm comp.) foi usado como coluna de separação. A amostra foi injetada por pressão 5” Hg durante 1 seg. A separação eletroforética foi conduzida sob voltagem constante de + 30 kV, com 5 mmol L-1 de tampão borato em pH ~ 9, contendo aditivos listado na tabela 1, e detecção indireta por UV em 224 nm. Estas condições foram obedecidas para todos os ensaios. A tabela 1 ainda mostra o nível dos fatores e a tabela 2 mostra o planejamento dos experimentos.


SDBS
– dodecil
benzenosulfonato de sódio
ACN - acetonitrila
D-bCD – dimetil beta ciclodexrtrina

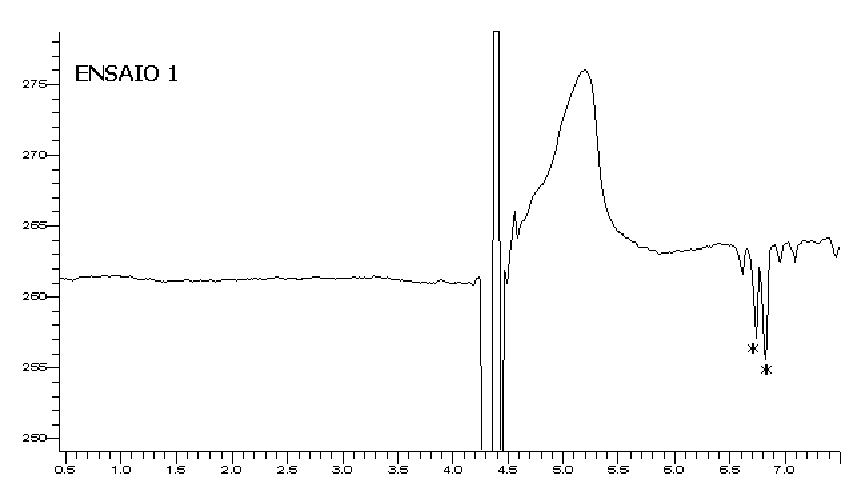
Resultados
e Discussão
considerado na separação com asteríscos.
De acordo com a tabela 3, pode-se observar quais são os efeitos que tem interação positiva e quais tem interação negativa no sentido de obter uma melhor separação dos ácidos graxos. O efeito negativo da ACN pode ser explicado, pois o aumento da mesma diminui o fluxo eletroosmótico e pode ocasionar formação de bolhas interrompendo a corrente. O efeito negativo apresentado pelo aumento da concentração de SDBS ocorre devido ao fato de que o mesmo só atua como cromóforo, uma vez que as micelas não chegam a se formar devido a presença de ACN. O efeito positivo determinado a partir do aumento da concentração da D-bCD ocorre porque essa substância é a única responsável pela maior discriminação entre as moléculas. O resíduo obtido está abaixo de 10%, ou seja, a modelagem proposta apresentou resultados satisfatórios.
Foi possível obter a separação completa dos FFAs do óleo de castanha-do- Pará sendo identificados como componentes majoritários C18:1 e C18:2 e como minoritários C16:0 e C18:0. Constatando-se que aumentos da concentração de SDBS e ACN causam efeitos negativos e aumento da concentração de D-bCD efeitos positivos, será feito um novo planejamento, com níveis adequados, para se obter melhores resultados.
Tavares, M. F. M., Química Nova 1997, 20, 493
Barros Neto, B., Scarminio, I. S, Bruns, R. E., Planejamento e otimização de experimentos, 2a Edição, Ed. Unicamp, 2a Edição, Campinas.