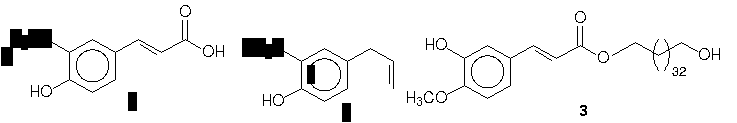
SÍNTESE TOTAL DO ÁCIDO FERÚLICO E DO FERULATO DE 34-HIDROXI-TETRATRIACONTANILA A PARTIR DO EUGENOL
Hélio Alexandre Stefani (PQ), Claudéte Justina Valduga (PG), Iguatemi Melo Costa (PG) e André José Araújo Gabriel (PG)
Faculdade de Ciências Farmacêuticas, Departamento de Farmácia
Universidade de São Paulo
Av. Professor Lineu Prestes, 580 Butantã São Paulo SP 05508-900
e-mail: agabriel@usp.br
palavras-chave: ácido ferúlico, eugenol, antitumorais
O ácido ferúlico 1 e seus derivados estão presentes em pequenas quantidades em um vasto número de espécies de plantas. É um dos constituintes da parede celular do trigo, e possui pronunciada atividade antioxidante, podendo ser utilizado como coadjuvante em tratamentos de processos inflamatórios. Uma outra utilização é como conservante em alimentos. Seus derivados são encontrados em plantas utilizadas na medicina indiana. Os ésteres ferúlicos possuem potencial atividade antitumoral, atuando em linhagens de células cancerosas de pulmão, cólon, mama e melanoma.1
A síntese do ácido ferúlico é relatada a partir da vanilina. Neste trabalho é feita a sua síntese através do eugenol 2, um produto natural abundante, e também a síntese do éster ferulato de 34-hidroxitetratricontanila 3, extraído da casca de plantas da espécie Plumeria rubra, L.
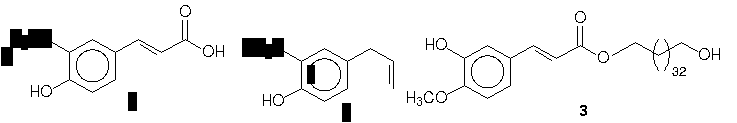
A partir da isomerização do eugenol catalisada por base, seguido de reação oxidativa alílica com SeO2, obteve-se o álcool 5.2 O ácido ferúlico foi obtido pela reação de 5 com MnO2 produzindo o aldeído correspondente, e oxidação posterior com Ag2O.3
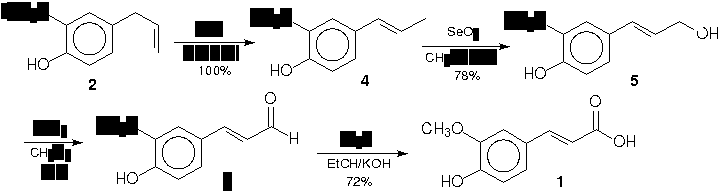
Para a obtenção da cadeia de 34 carbonos presente no ferulato 3 utilizou-se como material de partida o ácido undecilênico 7, construindo-se dois fragmentos principais, 10 e 13, que foram posteriormente acoplados através da reação de Grignard catalisada por Li2CuCl4. Posterior tratamento com ácido e proteção com DHP em presença de resina de troca iônica resultou no 1,34-tetratriacontanodiol monoprotegido com THP 14,4 que através de reação de esterificação com o ácido ferúlico resultou no composto 3, com rendimento de 82%.
O fragmento 10 foi obtido através de uma reação de hidroformilação, homologando-se um carbono,5 com posterior redução com LiAlH4 e dibromação do diol 9 com Br2/trifenilfosfina. Já o fragmento 13 pôde ser obtido pela redução do ácido undecilênico com LiAlH4 e reação de bromação anti-Markovnikov em presença de peróxido orgânico.
Assim, tendo-se como precursor o eugenol, puderam ser obtidos o ácido ferúlico com rendimento global de 36% e seu éster ferulato de 34-hidroxi-tetratriacontanila com rendimento global de ~27%.
Referências Bibliográficas:
1- Dobhal, M.P; Sharma, M.C; Joshi, B.C. Phytochemistry 1999, 51, 319.
2- Toomey, J.E Chem Abstr. 1986, 105, 215760v.
3- Kienzle,F.; Mayer, H.; Minder, R.E. Helv. Chim. Acta 1978, 61, 2616.
4- Suzuki, S.; Shiono, m.; Fujita, y. Synthesis 1983, 804.
5- Valduga, C. J., Paganelli, S., Botteghi, C., Marchetti, M., Hydroformylation: A Powerful Tool for the Synthesis of Pharmaceuticals, First European Catalysis Symposium (Valencia, 1999).