Hélio A. Stefania (PQ); Iguatemi de Melo Costaa (PG);
Paulo Henrique Menezesb (PQ)
aFaculdade de Ciências Farmacêuticas – Universidade de São Paulo – SP
bDepartamento de Química Fundamental – Universidade Federal de Pernambuco– PE
Palavras-Chave: Virol C, álcoois acetilênicos, sulfóxidos quirais
O (+)-Virol C, 1 é um álcool poliacetilênico análogo da Cicutoxina isolado da planta Cicuta virosa (Umbelliferae) e que apresenta interessantes propriedades químicas e farmacológicas1.
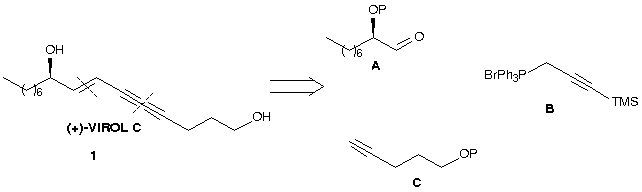
Neste trabalho, descrevemos a síntese total de 1 utilizando metodologias como o uso de sulfóxidos quirais para a formação do estereocentro de configuração S e reações de acoplamento para a síntese da unidade diínica presente na molécula. De acordo com a análise retrossintética, o (+)-Virol C foi dividido em três fragmentos principais (Figura 1).

Figura 1: Análise retrossintética
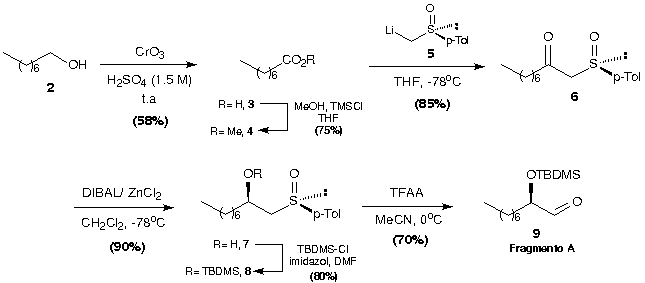
O Fragmento A foi preparado a partir da oxidação do 1-octanol, 2 ao ácido octanóico, 3 seguida de reação de esterificação levando ao éster 4. Ao éster 4 foi adicionado o ânion de lítio do R-(+)-metil-p-toluil-sulfóxido 5, que levou ao b-ceto-sulfóxido 6 em bom rendimento. A redução distereoseletiva2 de 6 utilizando DIBAL e ZnCl2 levou ao álcool 7 em 97% de excesso diastereomérico. Posterior proteção, 8 e rearranjo de Pummerer3 levou ao aldeído desejado 9 (Fragmento A, Esquema 1).
Esquema 1
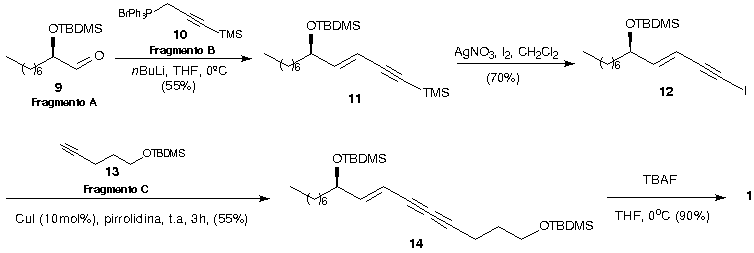
A reação de Wittig4 com o sal de fosfônio 10 (Fragmento B) levou ao trimetilsilil-enino correspondente, que então é convertido ao iodeto 12 para ser posteriormente acoplado ao acetileno 13 (fragmento C), levando ao diíno 14. Uma reação de múltipla desproteção com fluoreto de tetrabutilamônio, levou ao (+)-Virol C, 1 (Esquema 2).
Esquema 2
Como conclusão, pode-se afirmar que a síntese do (+)-Virol C é convergente e eficiente. Do ponto de vista de utilização de novas metodologias, a síntese demonstra novas aplicações para o uso de sulfóxidos quirais e acoplamentos.
CNPq, FAPESP, FACEPE
Oshima, Y.; Uwan, K.; Sugihara, T.; Ohta, T. Tetrahedron 1999, 55, 9469.
Solladié, G.; Greck, C.; Solladié-Cavallo, A. Tetrahedron Lett. 1982, 23, 5047
Sugihara, H.; Tanikaga, R.; Kaji, A. Synthesis 1978, 881.
Corey, E. J.; Ruden, R. Tetrahedron Lett. 1973, 17, 1495.