SISTEMA AMPEROMÉTRICO PARA DETERMINAÇÃO DE DIPIRONA EM FORMULAÇÕES FARMACÊUTICAS USANDO ELETRODO DE OURO A PARTIR DE CDs GRAVÁVEIS
Rodrigo Alejandro A. Muñoz (IC), Renato C. Matos (PG) e Lúcio Angnes (PQ)
Departamento de Química Fundamental, Instituto de Química, Universidade de São Paulo, USP, São Paulo, SP.
palavras-chaves: dipirona, formulações farmacêuticas e eletrodo de ouro.
O desenvolvimento de metodologias rápidas, confiáveis e de baixo custo para o monitoramento de espécies químicas tem evoluído de maneira muito acentuada. O interesse por tais metodologias abrange os mais variados campos, podendo ser destacadas as áreas clínica, ambiental e industrial, cujas aplicações têm expandido rapidamente. A detecção amperométrica em fluxo tem sido bastante utilizada como técnica para determinação de traços de compostos orgânicos devido a facilidade no uso, a alta sensibilidade e em diversos casos, boa seletividade.
O objetivo deste trabalho foi desenvolver um método amperométrico em fluxo para determinação de dipirona usando eletrodos de ouro obtidos a partir de CDs graváveis. A principal matriz estudada foram formulações farmacêuticas que possuem na sua composição este analito.


Foi
utilizado como eletrodo de trabalho um eletrodo de ouro obtido a
partir de CDs graváveis [1]. Como eletrodo de referência
um eletrodo mimiaturizado de Ag/AgCl(sat.) construído
em nosso laboratório e como eletrodo auxiliar um tubo de aço
inoxidável. A detecção eletroquímica em
fluxo foi feita com base em um sistema de linha única, usando
uma cela eletroquímica construída no laboratório,
a qual é mostrada na figura 1. As medidas foram feitas usando
um potenciostato PGSTAT 20 (Ecochemie). Através do sistema FIA
foram feitas determinações ondas de oxidação
apresentaram uma melhor resolução numa faixa de pH de
4,0 a 7,0. Também foram realizados testes para encontrar a
faixa linear de trabalho, o limite de detecção e a
eliminação da interferência do ácido
ascórbico na determinação de dipirona em
formulações farmacêuticas. Com os estudos
realizados foi obtida uma faixa linear de trabalho para concentrações
de dipirona variando de 1x10-7 mol.L-1 a 1x10-5
mol.L-1, assim para a análise das amostras reais
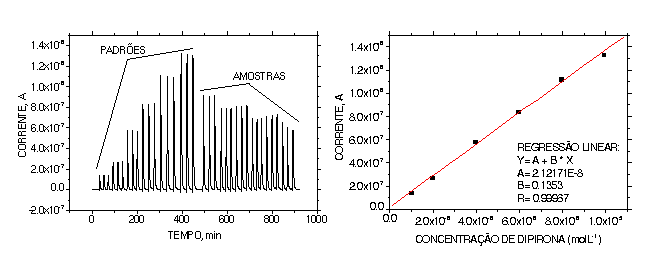
foi construída uma curva analítica na faixa de 1x10-6
mol.L-1 a 1x10-5 mol.L-1, a qual
pode ser vista na figura 2. A eliminação da
interferência do ácido ascórbico presente em uma
das amostras foi feita através do uso de ascorbato oxidase
encontrada na polpa do pepino. As amostras foram analisadas pela
detecção amperométrica em fluxo e pela titulação
iodométrica. A tabela 1 relaciona os resultados encontrados
para a dipirona pelos métodos citados e os valores indicados
pelos fabricantes, mostrando uma boa concordância entre os
resultados, uma vez que os erros variaram entre 0,6 e 9 %.
Figura 2. Respostas amperométricas em fluxo e curva analítica para a determinação de dipirona em formulações farmacêuticas.
Tabela 1. Determinação de dipirona em formulações farmacêuticas.
AMOSTRAMASSA DE DIPIRONA – SISTEMA AMPEROMÉTRICO (g)MASSA DE DIPIRONA – TITULAÇÃO IODOMÉTRICA (g)MASSA DE DIPIRONA – INDICADA PELO FABRICANTE (g)Novalgina0.4570.4510.500Anador0.5030.5030.500Conmel0.2980.2970.320Dipirona0.4620.4610.500Lisador0.4910.5010.500Apracur*0.1020.1060.100* Originalmente continha ácido ascórbico, que foi enzimaticamente consumido.
BIBLIOGRAFIA
[1]. Richter, E. M.; Kume, G. H.; Mioshi, R. N.; Augelli, M. A.; Angnes, L.; XI Simpósio Brasileiro de Eletroquímica e Eletroanalítica, Maragogi-AL (1999), 72-75.
[FAPESP, CNPq]