BIOSSÍNTESE DE (+)-CONOCARPANO EM PIPER REGNELLII
Patrícia Sartorelli (PG), Ricardo M. Ellensohn (PG),
Paulo R. H. Moreno (PQ), Massuo J. Kato (PQ)
Instituto de Química, Departamento de Química Fundamental
Universidade de São Paulo C. P. 26077, CEP 05513-970 São Paulo -SP
palavras-chave: Piper regnellii, conocarpano, biossíntese.
Considera-se que a biossíntese de lignanas e neolignanas envolve o acoplamento oxidativo mediados por enzimas estereoespecíficas visto que a maioria das que ocorrem naturalmente são opticamente ativas. A definição de lignanas/neolignanas têm sido ponto de controvérsia. O termo lignana foi primeiramente aplicado para dímeros de unidades de fenilpropanóides ligados pelos carbono b-b’ da cadeia lateral [1]. O termo neolignana foi concebido por Gottlieb para designar dímeros de fenilpropanóides ligados por outras posições que não as b-b’ [2]. Em 1978 Gottlieb redefiniu o termo neolignana sob o ponto de vista quimiotaxonômico, onde neolignanas poderiam ser consideradas dímeros de propenil ou alilfenóis [3], visto que a sua ocorrência é restrita em taxons aparentados Magnoliiflorae e Piperales. No entanto esta definição não tem sido completamente aceita por falta de dados biossintéticos, prevalecendo a definição de neolignanas como dímeros ligados por outras posições diferentes das b-b’.
A família Piperaceae é classificada entre as mais primitivas famílias entre as angiospermas, é constituída por cerca de 10 a 12 gêneros e cerca de 1400 espécies [4]. Muitas dessas espécies têm sido utilizadas na alimentação e na medicina tradicional, o que levou ao isolamento de diferentes classes de produtos naturais biologicamente ativos tais como alcalóides, flavonóides e lignóides [5].
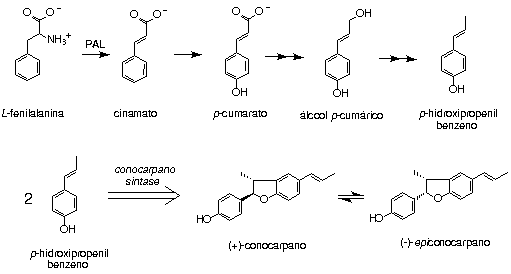
A investigação fitoquímica em raízes de P. regnellii resultou no isolamento de vários fenilpropanóides e neolignanas benzofurânicas incluindo (+)-conocarpano e (-)-epi-conocarpano como componentes majoritários [6]. A partir desse conjunto de metabólitos secundários foi proposta uma rota biossintética onde o conocarpano e seu estereoisômero são derivados do acoplamento oxidativo de p-hidroxipropenilbenzeno (Figura 1). A investigação da biossíntese de neolignanas benzofurânicas em P. regnellii constituiu-se no objetivo do presente trabalho.
Uma fração enzimática de membranas (solubilizada em tampão fosfato contendo 1% de Triton X-100) obtida de folhas, foi capaz de converter estereoespecificamente p-hidroxipropenilbenzeno em (+)-conocarpano. A enzima, denominada conocarpano sintase, foi então parcialmente purificada por filtração em gel (Sephacril S 200 HR) e as frações foram ensaiadas quanto a capacidade de converter p-hidroxipropenilbenzeno em conocarpano. A especificidade desta conversão foi avaliada através de um método em CLAE para separar formas antipodais do (±)-conocarpano em coluna quiral. A especificidade da enzima ao substrato foi investigada utilizando-se o ácido p-cumárico, álcool p-cumárico e E-isoeugenol e, nestes casos, não foram observadas suas conversões em dímeros.
Este resultado constitui-se na primeira demonstração da presença de uma enzima específica envolvida na biossíntese de uma neolignana. A conversão do p-hidroxipropenilbenzeno foi específica (e estereoespecífica) à neolignana benzofurânica, pois não se observou a formação de outros tipos de dímeros. Desta maneira, a definição do termo neolignana como sendo dímeros de alil/propenilfenóis, poderia ser reconsiderada a luz desses dados.

Figura 1 : Biossíntese de (+)-conocarpano em P. regnellii
[1] Haworth, R. D. (1942). The chemistry of the lignan group of natural products. Journal of Chemical Society, 448.
[2] Gottlieb, O.R. (1974). Lignans and neolignans. Revista Latinoamericana de Química, 5, 1.
[3] Gottlieb, O. R. (1978). Neolignans in: Herz W.; Grisebach, H.; Kirbi, G. W. (Eds.) Progress In Chemistry Of Organic Natural Products, Springer Verlag, Viena, 35: 1.
[4] Joly, A. B. (1985). Introdução à Taxonomia vegetal, Ed. Nacional, São Paulo - SP, Brasil.
[5] Parmar, V. S., Jain, S. C., Bisht, K. S., Jain, R., Taneja, P., Jha, A., Tyagi, O. M., Prasad, A. K., Wengel, J., Olsen, C. E. e Boll, P. M. (1997). Phytochemistry of genus Piper. Phytochemistry, 46, 597.
[6] Benevides, P. J. C., Sartorelli P. e Kato, M. J. (1999). Phenylpropanoids and Neolignans from Piper regnellii. Phytochemistry 52, 339.
(CAPES, FAPESP e PADCT/CNPq)