SENSOR
DE GLICOSE BASEADO NA IMOBILIZAÇÃO DE GLICOSE OXIDASE
(GOD) POR ELETROPOLIMERIZAÇÃO DE PIRROL EM
MICRO-CÉLULA.
Pablo Fiorito (PG), Susana Córdoba de Torresi (PQ)
Departamento de Química Fundamental, Instituto de Química,
Universidade de São Paulo, CEP 05513-970, São Paulo,
Brasil.
Palavras Chave: Biosensor, Glicose,
Poli(pirrol)
Na última década
o desenvolvimento de biosensores tem despertado um interesse sem
precedentes, particularmente a construção de sensores
de glicose que permitam o autocontrole da glucemia em pessoas
diabéticas.
Uma forma simples de
elaborar um sensor de glicose é a imobilização
de GOD durante o crescimento de polímeros gerados pela
oxidação eletroquímica de um monômero a
partir de uma solução que também contêm a
enzima. As principais vantagens deste método é que o
sensor pode ser preparado rapidamente, envolvendo
uma etapa só e outorgando resolução espacial.
Porém, o método apresenta
uma severa limitação, já
que para que a imobilização
da enzima ocorra durante a polimerização, precisam-se
de altas concentrações de proteína no eletrólito
aquoso. A utilização de micro-células
eletroquímicas permite a formação de películas
poliméricas desde pequenos volumes de electrólito
(50-100 ml), reduzindo notavelmente
a quantidade de enzima requerida [1].
O objetivo deste
trabalho é a elaboração de um sensor de glicose
imobilizando GOD e ferroceno numa matriz de poli(pirrol) gerado
sobre um eletrodo de platina em micro-célula eletroquímica
e a sua caracterização.
O biosensor foi feito da
seguinte maneira: preparou-se uma solução aquosa de
enzima e pirrol à qual foi adicionada uma solução
de ferroceno em etanol, resultando uma suspensão de enzima em
H2O/etanol (1:1) contendo 10 mg/ml de enzima, 0,1 M de
pirrol e 10-3 M de ferroceno. Têm sido reportada a
preparação de suspensões de GOD em H2O/etanol
sem perda significativa da atividade da enzima [2]. Uma alíquota
de 100 ml da suspensão foi
colocada na micro-célula (Fig. 1), onde foi feita a
polimerização por voltametria cíclica, variando
o potencial entre –600 e 800 mV, durante 5 ciclos.
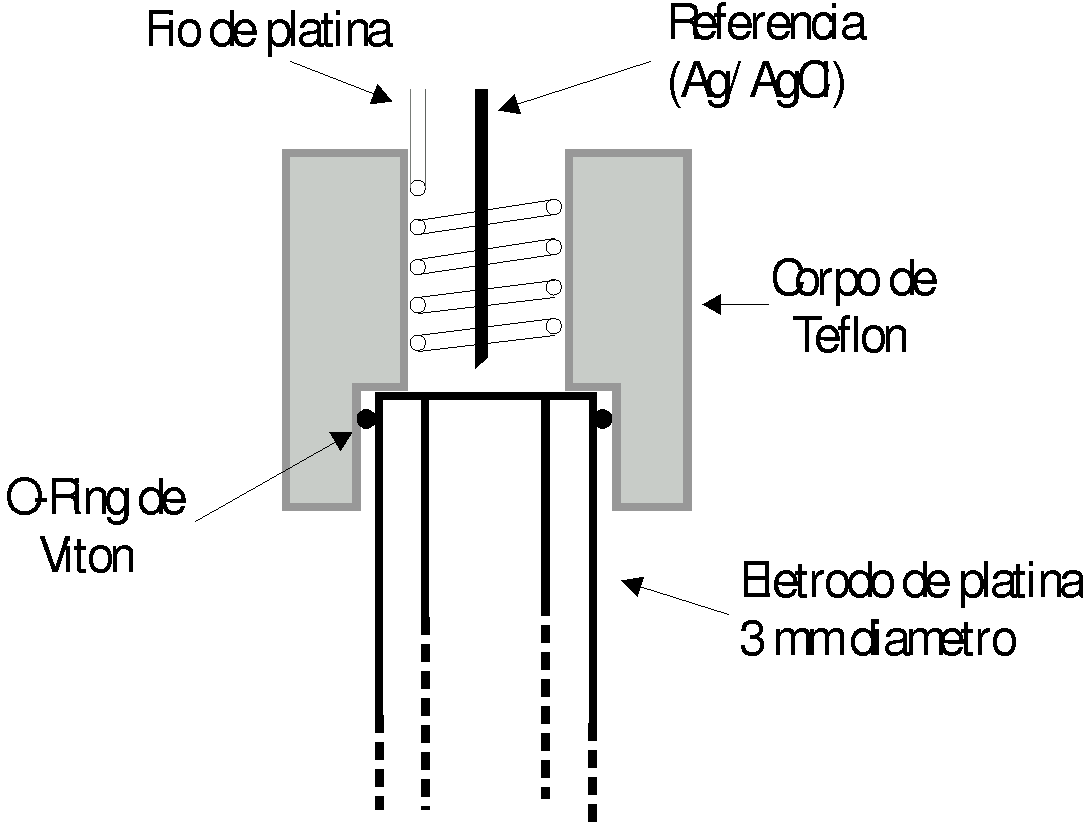
Fig. 1
O eletrodo foi lavado com água ultra
pura (UHQ, Elga System) e acondicionado
numa solução tampão de fosfato (pH 7) até
sua utilização. O procedimento de elaboração
foi repetido para o eletrodo previamente recoberto com um filme de
Nafionâ. Os
testes de sensibilidade do sensor à glicose e possíveis
interferentes (ascorbato e ureato) foram feitos numa célula
eletroquímica convencional de três eletrodos (5 ml),
utilizando-se como eletrólito suporte uma solução
agitada de tampão fosfato de pH 7 e polarizando a 0.65 V.
Todos os potenciais estão referidos ao eletrodo de Ag/AgCl.
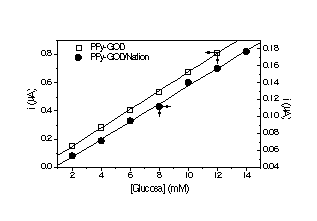
Fig. 2
Na
Fig. 2 são mostradas as curvas de calibração
obtidas para os dois biosensores preparados. Pode-se observar uma
resposta lineal até aproximadamente 10mM de glicose, com uma
sensibilidade de 9,14D10-7
A
M-1cm-2 para o sensor sem Nafion e de 1,48D10-7
A M-1cm-2 para o sensor previamente recoberto
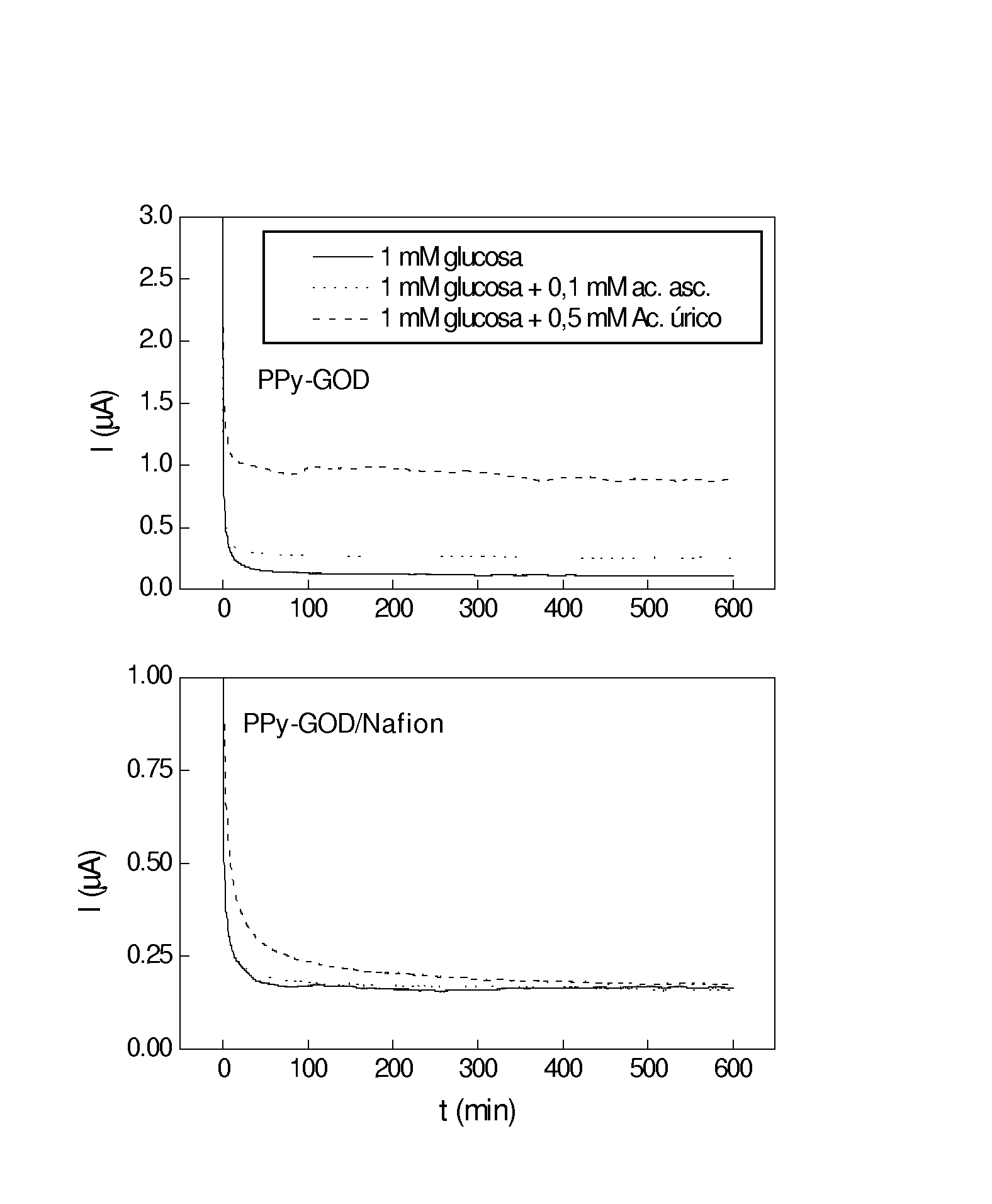
com Nafion. Embora o eletrodo com Nafion apresenta uma sensibilidade
menor, a inclusão do fluoropolímero permite a
eliminação total da interferência provocada pelos
íons ascorbato e ureato nas concentrações
fisiológicas máximas (Fig. 3).
Fig. 3
Apresenta-se um método para a elaboração
de um biosensor de glicose que permite a inclusão de ferroceno
como mediador na etapa de transducção sem a necessidade
de modificar a enzima ou o monômero, que apresenta bom
desempenho e eliminação total das interferências
produzidas pelos íons ascorbato e ureato devido à
inclusão do Nafion no sensor.
REFERÊNCIAS:
[1] K. Habermüller and W. Shuhmann,
Electroanalysis 10 (1998) 1281-1284
[2] A. Karyakin, E. Kanyakiva, L. Gorton, Sensors
and Actuators B 44 (1997) 356-360
FAPESP


